Рекомендации по лечению миастении и миастенического синдрома Ламберта-Итона в период эпидемии COVID-19
Коронавирусное заболевание 2019 г. (COVID-19) – это новое заболевание, причиной которого является новый коронавирус 2-го типа, вызывающий тяжелый острый респираторный синдром (SARS-CoV-2). Симптомы заболевания могут быть различными; как правило, они включают в себя лихорадку, кашель, симптомы со стороны органов дыхания, диарею, снижение обоняния и вкуса. Тяжесть заболевания варьирует от легкой до тяжелой, и у некоторых пациентов вирус может привести к пневмонии, острому респираторному дистресс-синдрому и смерти. Почти каждая страна мира охвачена этим вирусом, и в настоящее время оно расценивается Всемирной организацией здравоохранения как пандемия. На данный момент не существует доказанных методов лечения этого вируса и вакцины для предотвращения инфекции.
В настоящее время нет данных о том, как COVID-19 влияет на пациентов с миастенией/миастеническим синдромом Ламберта-Итона (МСЛИ) или на пациентов с другими заболеваниями, у которых проводится иммуносупрессивная терапия. Однако, поскольку большинство пациентов с миастенией получают иммуносупрессивную или иммуномодулирующую терапию, и у них может иметь место слабость дыхательной мускулатуры, то существует теоретическая обеспокоенность тем, что у пациентов с миастенией/МСЛИ риск инфицирования или более тяжелого течения COVID-19 может быть выше.
Пациенты с миастенией и МСЛИ обратились за рекомендациями по применению терапии во время пандемии COVID-19. Существуют многочисленные документы, в которых делается попытка внести ясность в этот вопрос и дать рекомендации по лечению, однако различия между этими рекомендациями вызывают путаницу. В том, что касается иммунотерапии, мнения значительно варьируют в зависимости от страны: где-то предписывается в основном ориентироваться на позицию конкретной организации и врача, проводящего лечение, а где-то предлагается модель совместного принятия решений. Приведенные ниже рекомендации были разработаны группой экспертов по миастении. Мы признаем, что на сегодняшний день отмечается дефицит рецензируемых публикаций, касающихся COVID-19 у пациентов с миастений или с иммунодефицитом.
Экспертная группа по миастении считает, что решения в отношении лечения миастении должны приниматься в индивидуальном порядке лечащим врачом совместно с пациентом. На основании этой экспертной рекомендации (23 марта 2020 г.) предлагается следующее:
1 Пациенты с миастенией должны следовать соответствующим национальным рекомендациям1 и любым дополнительным рекомендациям для лиц в группе риска тяжелого течения COVID-19.
Пациенты, уже получающие лечение миастении/МСЛИ
2 Пациенты с миастенией/МСЛИ должны продолжать текущее лечение, и мы рекомендуем не прекращать лечение какими-либо текущими препаратами, если обратное не обсуждалось отдельно и не рекомендовано лечащим врачом.
3 Отсутствуют научные доказательства того, что симптоматическая терапия, такая как применение пиридостигмина или 3,4-диаминопиридина, увеличивает риск инфекции, и лечение этими препаратами не должно прекращаться, если для этого нет других клинических причин.
4 Несмотря на отсутствие убедительных доказательств, рекомендуется, чтобы пациенты с миастенией, которые уже получают иммуносупрессивную терапию2,3, крайне ответственно подходили к соблюдению социального дистанцирования, в том числе избегали общественных мест, скопления людей, переполненного общественного транспорта и, по возможности, использовали альтернативы очным консультациям (например, телемедицинские консультации), если это допустимо с клинической точки зрения.
5 При принятии решения об изменении или прекращении текущей иммуносупрессивной терапии3, что сопряжено с риском повышения активности заболевания и/или развития обострения или миастенического криза, пациенты с миастенией и их лечащие врачи должны соотносить специфические риски (например, возраст, сопутствующие заболевания, местоположение) и пользу от такого решения.
Инфузионная терапия, внутривенные иммуноглобулины и плазмообмен
6 Инфузионная терапия некоторыми препаратами при миастении может потребовать поездок в стационар или центр инфузионной терапии, и мы настоятельно рекомендуем принимать решение об этом, основываясь на распространенности COVID-19 в данном регионе и соотношении «риск/польза» от терапии для конкретного пациента. Врач должен иметь возможность дать пациенту рекомендации с учётом ситуации в данном регионе и, по возможности, рассмотреть вопрос о переходе на инфузии на дому.
7 В настоящее время нет доказательств того, что лечение внутривенным иммуноглобулином (ВВИГ)4 или терапевтический плазмообмен сопряжены с каким-либо дополнительным риском инфицирования COVID-19. Тем не менее, лечение ВВИГ должно основываться на индивидуальных потребностях пациента, и следует избегать неизбирательного применения иммуноглобулина. Как правило, плазмообмен и ВВИГ назначаются при обострении. Тем не менее, рабочая группа понимает, что у некоторых пациентов они применяются в качестве поддерживающего лечения, которое следует продолжать, однако при этом могут потребоваться дополнительные меры предосторожности, связанные с необходимостью поездок в медицинское учреждение и обратно.
8 В настоящее время нет доказательств того, что ингибирование комплемента с помощью моноклонального антитела экулизумаба увеличивает восприимчивость к COVID-19 или влияет на исход инфекции.
Анализы крови для контроля текущего лечения
9 Следует соотнести риск и пользу от рутинного мониторинга показателей крови в данный период. Некоторые методы лечения миастении требуют частого контроля показателей крови, и решения о необходимости продолжения проведения анализов, что требует от пациента покидать свой дом, следует принимать индивидуально, основываясь на распространенности COVID-19 в данном регионе.
Что следует учитывать, начиная иммуномодулирующую терапию у пациентов с миастенией/МСЛИ в данный период?
10 Перед началом лечения препаратами, снижающими количество B-лимфоцитов2 (например, ритуксимабом), врачи должны учитывать риск ухудшения течения миастении или развития криза, а также риск заражения вирусной инфекцией. Может быть целесообразным отложить начало лечения препаратами, снижающими количество B-лимфоцитов, до тех пор, пока пик вспышки в данном регионе не пройдёт. В то же время риск откладывания лечения этими препаратами у отдельных пациентов может превзойти риск развития тяжелой инфекции COVID-19, и это необходимо подробно обсудить с пациентом.
Рекомендации для пациентов, участвующих в текущих клинических исследованиях
11 В настоящее время проводится множество клинических исследований у пациентов с миастенией, и мы настоятельно рекомендуем, чтобы любое решение, касающееся очной оценки и лечения пациента в рамках клинического исследования, учитывало наилучшие интересы пациента. В настоящее время нет доказательств того, что ингибиторы комплемента или блокаторы неонатальных Fc-рецепторов могут увеличить риск заражения вирусной инфекцией, однако рабочая группа рекомендует соблюдать дополнительные меры предосторожности (как в пункте 4 выше), чтобы свести этот риск к минимуму. В клинических исследованиях это также должно обсуждаться и утверждаться спонсором исследования, Экспертным советом организации и медицинским монитором.
Есть ли обоснованные доказательства в пользу применения каких-либо препаратов для лечения COVID-19?
12 В новостях и социальных сетях упоминаются различные лекарственные препараты, которые, как утверждается, могут принести пользу при лечении COVID-19 (например, хлорохин, азитромицин, противовирусные препараты и т.д.), однако в настоящее время их эффективность не была показана или не было проведено их систематического изучения. Пациенты должны быть осведомлены, что некоторые из этих препаратов могут ухудшить течение миастении, и не должны применять их без специального разрешения врача. Если будут получены новые данные и появятся предположения о пользе применения тех или иных препаратов при COVID-19, то эти препараты следует использовать под строгим медицинским наблюдением, взвесив риск и пользу от их применения для каждого конкретного пациента.
Должны ли пациенты с миастенией или МСЛИ вакцинироваться?
13 Вакцинация может защитить от различных инфекций/инфекционных агентов. Однако в текущей ситуации у данной группы пациентов рекомендуется использовать только инактивированные вакцины. Для COVID-19 в настоящее время доступных вакцин нет.
Что если пациенты уже заразились COVID-19?
14 В большинстве случаев у пациентов с COVID-19 заболевание протекает в легкой форме, и они должны продолжить лечение миастении/МСЛИ в соответствии с наилучшей текущими стандартами. Может возникнуть необходимость в увеличении дозы кортикостероидов, как предусмотрено стандартным протоколом в случае развития инфекции. Однако, если симптомы инфекции являются тяжёлыми (требуют госпитализации), то, возможно, стоит рассмотреть вопрос о временной приостановке текущей мощной иммуносупрессивной терапии, особенно если у пациента развились сопутствующие суперинфекция/сепсис. В этом случае не следует применять препараты, снижающие клеток иммунной системы; применение иммуносупрессивных препаратов с менее сильным действием (азатиоприн, микофенолат), вероятно, следует продолжать, так как их действие сохраняется дольше, для выведения препарата требуется больше времени, а восстановление их эффекта занимает несколько месяцев.
15 В большинстве случаев решения об эскалации терапии должны приниматься в индивидуальном порядке в зависимости от относительной тяжести COVID-19 и миастении.
Решения относительно применения иммунотерапии должны приниматься в индивидуальном порядке пациентом с миастенией и лечащим врачом. По дополнительным вопросам следует обратиться к лечащему врачу.
Мы продолжаем следить за быстро меняющейся ситуацией, и эти рекомендации могут быть изменены по мере поступления данных.
Примечания
1 Этот список не является исчерпывающим, в нем приведены лишь примеры рекомендаций. Ознакомьтесь с последними рекомендациями для каждой страны/региона:
2 Препараты, снижающие количество B-лимфоцитов, включают в себя ритуксимаб, окрелизумаб.
3 Препараты для иммунотерапии, отмена которых сопряжена с риском развития серьезное повышения активности заболевания, развития рецидива и обострения/миастенического криза, включают в себя кортикостероиды, азатиоприн, микофенолата мофетил, метотрексат, циклоспорин, такролимус и другие.
4 Иммуномодулирующие препараты: внутривенный иммуноглобулин (ВВИГ), подкожный иммуноглобулин.
Миастения
Симптомы
Мышечная слабость вызванная миастенией увеличивается в больных мышцах при повторных нагрузках на эти мышцы. Так как симптомы обычно уменьшаются после отдыха, мышечная слабость может появляться и исчезать. Симптомы миастении прогрессируют с течением времени и, как правило, наибольшего пика достигают через несколько лет после дебюта заболевания. Несмотря на то, что миастения может поразить любые из поперечно-полосатых мышц, определенные группы мышц вовлекаются в процесс чаще, чем другие.
Глазные мышцы
У более чем половины пациентов, у которых развилась миастения, первые симптомы связаны со зрением:
Примерно у 15 процентов пациентов с миастенией, первые симптомы затрагивают мышцы лица, и гортани что будет проявляться:
Мышцы конечностей и шеи
Причины
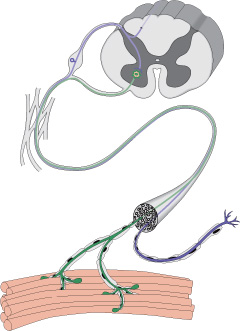
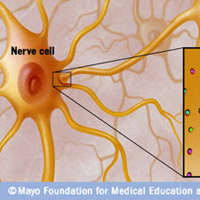
Нервы передают импульсы мышцам с помощью выброса химических веществ, называемых нейротрансмиттерами, которые попадают точно в рецепторы на мышечных клетках. При миастении, иммунная система вырабатывает антитела, которые блокируют или уничтожают много мышечных рецепторов нейротрансмиттера ацетилхолина. С уменьшением количества действующих рецепторов, мышцы получают меньше нервных сигналов, в результате это приводит к мышечной слабости.
Факторы, которые могут ухудшить течение миастении
Осложнения
Осложнения миастения обычно поддаются лечению, но некоторые из них могут быть опасны для жизни.
Миастенический криз
Миастенический криз является угрожающим жизни состоянием, которое возникает, когда мышцы, которые контролируют дыхание, становятся слишком слабыми для выполнения своих функций. В таких случаях требуется неотложная помощь для обеспечения дыхания и с использованием аппаратного дыхания. Медикаментозное лечение и фильтрация крови помогают пациентов выйти из миастенического криза и тогда они могут дышать самостоятельно
Опухоли тимуса
У приблизительно 15 процентов пациентов с миастенией отмечается наличие опухоли в вилочковой железы. Большинство этих опухолей доброкачественные.
Другие нарушения
У пациентов с наличием миастении, также нередко встречаются следующие проблемы:
Диагностика
Прежде всего, при подозрение на миастению пациента направляют на консультацию невролога. Врача-невролога могут интересовать подробное описание симптомов, наличие в анамнезе приема лекарств (дозировок), связь симптомов с физическими нагрузками. Врач-невролог проведет изучение неврологического статуса (рефлекторную активность, мышечную силу, мышечный тонус, координацию, зрение и осязание).
Основным признаком того, что указывает на возможность миастении, является слабость мышц, которая регрессирует после отдыха. Тесты, которые могут помочь подтвердить диагноз могут включать:
КТ или МРТ может быть назначено для исключения опухоли вилочковой железы.
Лечение
Врачи используют различные методы лечения, по отдельности или в комбинации, чтобы уменьшить симптомы миастении.
Лекарственные препараты
Хирургическое лечение
У 15 процентов людей, у которых есть миастения, также отмечается наличие опухоли в вилочковой железе. В таких случаях рекомендуется оперативное лечение и удаление опухоли.
Для пациентов с миастенией, у которых нет опухоли в вилочковой железе, удаление железы является достаточно спорным методом лечения.
Хирургическое вмешательство не рекомендуется большинством врачей, если:
Образ жизни
Использование материалов допускается при указании активной гиперссылки на постоянную страницу статьи.
Лечение тяжелой миастении. Часть 3
» data-image-caption=»» data-medium-file=»https://unclinic.ru/wp-content/uploads/2020/12/lechenie-tjazheloj-miastenii-900×600.jpg» data-large-file=»https://unclinic.ru/wp-content/uploads/2020/12/lechenie-tjazheloj-miastenii.jpg» title=»Лечение тяжелой миастении. Часть 3″>
Галина Кучма, врач УЗИ. Редактор А. Герасимова
В первую очередь для лечения тяжелой миастении применяются медикаментозные препараты.
Лекарства для симптоматического лечения
Все подгруппы тяжелой миастении реагируют на ингибирование ацетилхолинэстеразы.
Тяжелая миастения с применением антител к мышечно-специфической киназе хуже реагирует на симптоматические лечебные препараты, чем другие подгруппы миастении. Ювенильная миастения характеризуется отличным ответом на лечение пиридостигмином.
Доза пиридостигмина подбирается с учетом влияния на мышечную силу, дозозависимых побочных реакций, и чаще всего мешает работе желудочно-кишечного тракта. Типичные побочные эффекты включают диарею, боль в животе, судороги, метеоризм, тошноту, повышенное слюноотделение, задержку мочи и повышенное потоотделение. Поэтому для каждого пациента следует подбирать индивидуальную дозу, которая может меняться в разные дни. Эффекты пиридостигмина остаются неизменными в течение многих лет. Пациентам с легкой формой заболевания, достигшим полной ремиссии с помощью симптоматических лекарств, никакие другие лекарства не рекомендуются
Иммуносупрессивная терапия
Большинству пациентов с миастенией требуется иммуносупрессивная терапия для полного или частичного восстановления физических функций и полного качества жизни. Иммунодепрессанты назначают всем пациентам, которые не реагируют адекватно на лечение только симптоматическими препаратами.
» data-medium-file=»https://unclinic.ru/wp-content/uploads/2020/12/immunosupressivnaja-terapija.jpg» data-large-file=»https://unclinic.ru/wp-content/uploads/2020/12/immunosupressivnaja-terapija.jpg» loading=»lazy» src=»https://unclinic.ru/wp-content/uploads/2020/12/immunosupressivnaja-terapija.jpg» alt=»Иммуносупрессивная терапия» width=»900″ height=»563″ srcset=»https://unclinic.ru/wp-content/uploads/2020/12/immunosupressivnaja-terapija.jpg 900w, https://unclinic.ru/wp-content/uploads/2020/12/immunosupressivnaja-terapija-768×480.jpg 768w» sizes=»(max-width: 900px) 100vw, 900px» title=»Лечение тяжелой миастении. Часть 3″> Иммуносупрессивная терапия
Иммуносупрессивная терапия первой линии – преднизолон с азатиоприном. Изменение дозировки преднизолона в разные дни часто снижает побочные эффекты глюкокортикоидов, но клинических исследований на эту тему мало. Чтобы болезнь не усугубилась, дозу обычно увеличивают постепенно – с 60 мг до 80 мг в разные дни.
По достижении контроля над симптомами дозу глюкокортикоидов следует постепенно снижать до минимальной эффективной поддерживающей дозы с добавлением симптоматического лечения. которая обычно составляет от 10 мг до 40 мг в разные дни.
Основная цель лечения глазной миастении гравис – предотвратить генерализацию заболевания. Ретроспективные и наблюдательные клинические исследования показали, что монотерапия преднизолоном снижает этот риск. Многие специалисты рекомендуют лечение низкими дозами глюкокортикоидов пациентам с глазной миастенией гравис, у которых есть стойкие симптомы и факторы риска, такие как установленные антитела к рецепторам ацетилхолина, увеличенный тимус, нейрофизиологические доказательства повреждения других мышц (не только глаза).\
Большинству пациентов, получающих преднизолон, дополнительно назначают азатиоприн, поскольку эта комбинация препаратов приводит к лучшим функциональным результатам и меньшему количеству побочных эффектов, чем монотерапия преднизолоном.
Если глюкокортикоиды противопоказаны или пациент отказывается их принимать, может быть назначена монотерапия азатиоприном. Рекомендуемая доза составляет 2-3 мг на килограмм массы тела. Азатиоприн подавляет синтез пурина, тем самым подавляя пролиферацию клеток, особенно В- и Т-клеток. Если возможно, перед лечением азатиоприном следует проверить активность тиопуринметилтрансферазы, поскольку слабая активность этого фермента увеличивает риск побочных эффектов азатиоприна. Этот фермент неактивен всего для 0,3% всего населения, а низкая активность обнаруживается у 10% населения.
Азатиоприн не рекомендуется пациентам, у которых нет активной тиопуринметилтрансферазы, а пациентам с низким уровнем этого фермента следует назначать более низкую дозу азатиоприна. Воздействие азатиоприна на мышечную слабость часто проявляется всего через несколько месяцев после начала лечения, и в этот период пациентам следует назначать другие иммунодепрессанты. Длительное лечение азатиоприном безопасно для пациентов любого возраста.
Многие руководящие принципы рекомендуют для лечения миастении легкой и средней степени тяжести микофенолата мофетил, хотя польза этого препарата не была продемонстрирована в двух краткосрочных проспективных исследованиях=. Этот препарат блокирует синтез пурина и останавливает пролиферацию В- и Т-клеток.
Метотрексат, циклоспорин и такролимус – это иммунодепрессанты второго ряда. Эффекты этих препаратов аналогичны эффектам азатиоприна.
Ритуксимаб – потенциально многообещающий препарат для лечения миастении. Это моноклональное антитело специфически связывается с поверхностным антигеном CD20 в В-лимфоцитах и поэтому эффективно при лечении опосредованных антителами заболеваний, таких как тяжелая миастения. Ритуксимаб также влияет на Т-клетки.
» data-medium-file=»https://unclinic.ru/wp-content/uploads/2020/12/rituksimab.jpg» data-large-file=»https://unclinic.ru/wp-content/uploads/2020/12/rituksimab.jpg» loading=»lazy» src=»https://unclinic.ru/wp-content/uploads/2020/12/rituksimab.jpg» alt=»Ритуксимаб» width=»900″ height=»578″ srcset=»https://unclinic.ru/wp-content/uploads/2020/12/rituksimab.jpg 900w, https://unclinic.ru/wp-content/uploads/2020/12/rituksimab-768×493.jpg 768w» sizes=»(max-width: 900px) 100vw, 900px» title=»Лечение тяжелой миастении. Часть 3″> Ритуксимаб
Группа экспертов, которая одобрила последние рекомендации по миастении, не смогла прийти к единому мнению о месте ритуксимаба в лечении этого заболевания. Хотя в небольших клинических испытаниях две трети пациентов с тяжелой миастенией, которые не ответили должным образом на преднизолон и азатиоприн, показали значительное улучшение при применении ритуксимаба. Рекомендуемая индукционная доза не установлена. Лечение следует повторить через несколько месяцев, если симптомы повторяются.
При лечении других аутоиммунных заболеваний обнаружен положительный эффект моноклональных антител. Они влияют на функции В- и Т-клеток, комплемента и других иммуноактивных элементов.
У пациентов с миастенией, появившейся в пожилом возрасте или у которых есть антитела к тимоме или мышечно-специфической киназе, с большей вероятностью разовьются наиболее тяжелая форма заболевания. Обычно они требуют длительной иммуносупрессивной терапии, хотя у некоторых пациентов с поздней миастенией гравис течение заболевания более легкое, больше похоже на раннюю миастению.
Показание для иммуносупрессивной терапии – обнаружение антител к мышечно-специфической киназе, тайтину, рецепторам рианодина или Kv1.4. Миастения, характеризующаяся появлением мышечно-специфических антител к киназе, лучше поддается лечению ритуксимабом.
Тимэктомия – еще один метод лечения миастении
Пациентам с миастенией и тимомой следует сделать тимэктомию – операцию по удалению тимуса. Преимущества тотальной тимэктомии продемонстрированы даже у пациентов с ранней миастенией, у которых не была диагностирована тимома.
Основным механизмом патогенеза тимуса при миастении является выработка антител к рецепторам ацетилхолина. В большинстве клинических испытаний сравнивали результаты у пациентов, которым удалили вилочковую железу, и которые не перенесли эту операцию. Результаты почти всех исследований показали, что результат был лучше у пациентов, перенесших тимэктомию. Международное рандомизированное исследование 126 пациентов с ранней или поздней миастенией. подтвердили преимущество ранней тимэктомии у пациентов с генерализованной миастенией, с длительностью заболевания до 3–5 лет, до 60–65 лет и симптомами, плохо контролируемыми препаратами, блокирующими холинэстеразу.
В европейских руководствах рекомендуется ранняя тимэктомия пациентам с ранней миастенией. У таких пациентов обычно наблюдается гиперплазия щитовидной железы. Также следует рассмотреть возможность тимэктомии у детей с миастенией.
Большинство пациентов с поздней миастенией имеют атрофический тимус. Однако гиперплазия щитовидной железы может развиться у более молодых пациентов в группе поздней миастении. Тимэктомию следует рассматривать у пациентов с генерализованной миастенией, у которых есть антитела к рецепторам ацетилхолина и у которых развиваются симптомы в возрасте от 50 до 65 лет, особенно если биомаркеры заболевания аналогичны биомаркерам ранней миастении.
Тимэктомия не проводится в следующих случаях:
Тяжелая миастения: особенности лечения
Пациентов с развивающейся прогрессирующей мышечной слабостью и требующих интубации или неинвазивной вентиляции легких, следует лечить быстродействующими иммунодепрессантами. Тяжелый миастенический криз, проявляющийся быстрым ухудшением состояния пациента и прогрессирующей мышечной слабостью, требует аналогичного лечения.
Нарастающая общая слабость, респираторная, сердечная недостаточность, тяжелая инфекция и сопутствующие патологии приводят к решению о показаниях для лечения миастенического криза в отделении интенсивной терапии. В этом случае мониторинг жизненно важных функций, параметров газов крови имеет ограниченное значение, так как ухудшение состояния пациента может быть очень внезапным и неожиданным, проявляясь в результате миастенического истощения.
Эффективны при лечении тяжелой миастении внутривенные иммуноглобулины и плазмаферез. Выбор между этими методами лечения зависит от индивидуальных факторов пациента, клинического опыта и доступности. Внутривенные иммуноглобулины более удобны для пациентов из-за более легких побочных эффектов.
Иногда для пациента может быть эффективным только один метод лечения, а другой – нет. Лечение этими методами следует сочетать с длительной иммуносупрессивной терапией. У некоторых пациентов эффект от лечения может быть отсроченным. Иммуносупрессивная терапия должна сочетаться с интенсивной терапией до тех пор, пока это необходимо для достижения ремиссии.
Миастенический криз с дыхательной недостаточностью в настоящее время является редким заболеванием, а смертность от миастенического криза невысока.
Поддерживающая терапия миастении и последующее наблюдение за пациентами
Пациентам с миастенией, в зависимости от состояния, рекомендуются физические нагрузки низкой и средней интенсивности и программы систематических тренировок. Следует избегать лишнего веса. При появлении глазных симптомов можно использовать глазные средства.
» data-medium-file=»https://unclinic.ru/wp-content/uploads/2020/12/glaznye-sredstva-900×600.jpg» data-large-file=»https://unclinic.ru/wp-content/uploads/2020/12/glaznye-sredstva.jpg» loading=»lazy» src=»https://unclinic.ru/wp-content/uploads/2020/12/glaznye-sredstva.jpg» alt=»Глазные средства» width=»900″ height=»600″ srcset=»https://unclinic.ru/wp-content/uploads/2020/12/glaznye-sredstva.jpg 900w, https://unclinic.ru/wp-content/uploads/2020/12/glaznye-sredstva-768×512.jpg 768w» sizes=»(max-width: 900px) 100vw, 900px» title=»Лечение тяжелой миастении. Часть 3″> Глазные средства
По возможности не следует назначать пациентам с миастенией миорелаксанты, пеницилламин, некоторые антибиотики – фторхинолоны, макролиды, аминогликозиды. Статины могут усугубить миастению, но миастения не является противопоказанием к назначению статинов по мере необходимости. Показания к применению статинов у пациентов с миастенией такие же, как у пациентов без этого заболевания. Если показаны статины, их можно назначить, но требуется бдительность из-за прогрессирования мышечной слабости.
Дыхательная недостаточность из-за слабости диафрагмальных и межреберных мышц представляет собой наибольший риск. Но пациентам с миастенией следует уделять особое внимание дыхательной функции во время любых хирургических вмешательств, в том числе тимэктомии.
Важная часть лечения миастении – оптимальное лечение всех сопутствующих патологий. Это серьезная проблема при лечении пожилых пациентов с сопутствующими заболеваниями.
Пероральный прием пиридостигмина и преднизолона во время беременности безопасен. Новые исследования предоставляют информацию о том, что лечение азатиоприном и циклоспорином также безопасно для беременных. Между тем, микофенолят мофетил и метотрексат противопоказаны беременным из-за риска тератогенных эффектов.
Женщинам после прекращения лечения ритуксимабом рекомендуется избегать беременности в течение 1 года.
Пациенткам с обострением во время беременности можно назначать внутривенные иммуноглобулины и плазмаферез. Следует поощрять грудное вскармливание. Транзиторная миастения встречается у новорожденных в 15% случаев из-за антител IgG к ацетилхолину, мышечно-специфической киназе, кроссовер рецептора LRP4 через плаценту.
Резюме
Тяжелая миастения – это аутоиммунное заболевание, характеризующееся связыванием аутоантител с рецепторами ацетилхолина в нервно-мышечном соединении постсинаптической мембраны и, как следствие, слабостью скелетных мышц.
Всех пациентов с миастенией следует разделить на подгруппы в соответствии с различными симптомами заболевания, и эта классификация определяет выбор тактики лечения.
Лечение первой линии для симптоматического лечения – пиридостигмин, а для иммуносупрессивного лечения – преднизолон с азатиоприном. Тимэктомия должна выполняться пациентам с миастенией, леченным тимомой.
Симптоматическое, иммуносупрессивное, хирургическое и поддерживающее лечение имеют очень хорошие эффекты, поэтому прогноз заболевания с точки зрения мышечной силы, функциональных возможностей, качества жизни и выживаемости хороший.