Аутоиммунный тиреоидит. Первый шаг к консенсусу
(по материалам I Всероссийской конференции «Актуальные проблемы заболеваний щитовидной железы»)
Фадеев В.В., Мельниченко Г.А., Герасимов Г.А.
Кафедра эндокринологии ММА им. И.М. Сеченова (зав. – академик РАМН Дедов И.И.), Международный совет по контролю за йоддефицитными заболеваниями (ICCIDD). Статья будет опубликована в №4 – 2001 журнала «Проблемы эндокринологии»
ЙОД И АУТОИММУННЫЙ ТИРЕОИДИТ
Хотя этой проблеме мы уже посвящали ряд ранних публикаций [3], к ней приходится возвращаться вновь и вновь. Так может ли повышенное поступление йода способствовать развитию АИТ? Все зависит от уровня потребления этого микроэлемента. Имеются физиологические дозы йода. Всемирная Организация Здравоохранения (ВОЗ) совместно с другими международными организациями установили, что суточная потребность в йоде составляет 100-200 мкг (мкг – это миллионная доля грамма). Полностью безопасной является суточная доза йода до 1000 мкг (1 мг). Более высокие дозы йода называются фармакологическими. Как правило, такое количество йода человек может получить только с лекарственными препаратами. Например, смазывая царапину спиртовым раствором йода, или используя в качестве наружного средства раствор Люголя. Некоторые отхаркивающие средства содержат огромное количество йода (граммы!). Каждая таблетка амиодарона (кордарона) содержит 60 мг йода, что эквивалентно годовой физиологической потребности в этом микроэлементе. Много йода в рентгенокнтрастных средствах, используемых, в частности при коронарографии.
В целом йод обладает очень низкой токсичностью и лишь в довольно редких случаях и только в фармакологических дозах способен вызвать реакцию, подобную аллергической. В экспериментальных исследованиях на линейных животных, имеющих генетическую предрасположенность к развитию аутоиммунной патологии щитовидной железы, было показано, что фармакологические дозы йода способны индуцировать аутоиммунный процесс. Есть сведения, что у лиц с генетической предрасположенностью к развитию аутоиммунных заболеваний щитовидной железы избыточное поступление йода (в фармакологических дозах!) также способно индуцировать аутоиммунные реакции в щитовидной железе, стимулировать образование антител и даже развитие гипотиреоза. Однако риск этого побочного явления сравнительно невелик. Так, развитие гипотиреоза зарегистрировано лишь примерно у 3% пациентов, постоянно и длительно получающих фармакологические дозы йода при приеме амиодарона (кордарона). При этом, в большинстве случаев после отмены данного препарата функция щитовидной железы восстанавливается [14].
Что же касается физиологических доз йода (100-300 мкг в день), то они не способны вызвать развитие аутоиммунного гипотиреоза. С другой стороны, если гипотиреоз на фоне АИТ уже развился, то физиологические дозы йода не способны принести дополнительного вреда. Разумеется, нет никакого смысла назначать препараты йода при увеличении щитовидной железы, вызванном АИТ. Это лечение не будет эффективным. Но нет ни малейшей необходимости ограничивать потребление продуктов, потенциально более богатых йодом (например, морскую рыбу или йодированную соль). Ведь в большинстве стран мира (уже не только развитых, но и самых бедных) более не существует йодного дефицита и потребление йода с продуктами питания (в том числе йодированной солью) находится на оптимальном уровне. При этом нет никакх доказательств того, что это как либо негативно отразилось на здоровье пациентов с аутоиммунной патологией щитовидной железы.
Итак, физиологические дозы йода не способны индуцировать развитие АИТ и не влияют отрицательно на функцию щитовидной железы при уже существующем гипотиреозе. Что касается фармакологических доз йода, то риск всегда следует соотносить с пользой. Следует ли отказаться от использования таких мощных и доступных антиспетиков как спиртовый раствор йода или раствор Люголя ради призрачной цели «профилактики АИТ»? При назначении препаратов, содержащих большое количество йода, следует помнить о возможном риске развития гипотиреоза и контролировать функцию щитовидной железы.
Беззащитная щитовидная железа: профилактика и лечение заболеваний
Проблемы с щитовидной железой начинаются с необычных симптомов, которые не всегда связаны с дефицитом йода. Если вам всегда холодно и сонливо, волосы стали выпадать, а характер изменился не в самую лучшую сторону — возможно, стоит проверить щитовидную железу. Как понять, что с ней не все в порядке? Что делать для профилактики тиреотоксикоза (гипертериоза) и гипотериоза? Опасны ли узлы и токсические зобы? Мы решили узнать ответы на эти вопросы у нашего ведущего эндокринолога Либеранской Натальи Сергеевны!
1. Профилактика заболеваний щитовидной железы йодом
Дефицит йода действительно характерен для жителей России, особенно это касается маленьких детей, подростков и беременных женщин. Щитовидная железа страдает в первую очередь, а когда это происходит, артериальное давление падает, кожа сохнет, волосы выпадают, человек испытывает сильную слабость и апатию, сонливость и озноб.
Картина следующая — дефицит йода приводит к тому, что тиреоидная пероксидаза выходит из тиреоцита. Организм начинает активно продуцировать антитела, которые атакуют щитовидную железу, и она начинает работать как попало — нарушается синтез важных гормонов: тироксина (Т4) и трийодтиронина (Т3).
Распространенность йододефицитных заболеваний щитовидной железы крайне велика. По примерным подсчетам ВОЗ, свыше 650 миллионов людей на планете живут с увеличенной щитовидной железой, а 43 млн страдают когнитивными расстройствами из-за нехватки йода. В профилактических целях имеет смысл покупать в магазинах только йодированную соль и включить морепродукты в дневной рацион. Чего делать точно не стоит, так это пить йод. Его избыток не лучше дефицита.
Проверить, нет ли у вас дефицита йода, можно в домашних условиях — нанесите йод на кожу. Если полоска исчезла ранее чем через 24 часа, то у вас скорее всего не хватает этого микроэлемента.
В клиническом анализе мочи содержание йода должно быть не менее 150 мкг/л. Дозировки определяются индивидуально от 150-1000 мкг считаются безопасными, иногда требуется прием более высоких доз. Йод лучше всего усваивается вместе с селеном. И это далеко не все микроэлементы, которые нужны щитовидке.
2. Микроэлементы для щитовидной железы
Селен
Помогает йоду усваиваться правильно, является отличным антиоксидантом. Рекомендованная суточная норма для взрослого человека — 200-400 мкг селен метионина или хелата. Доказано, что селен снижает уровень антител при аутоиммунном тиреоидите.
Железо
Является основополагающим компонентом. Его дефицит приводит к нарушению работы щитовидной железы и наоборот, нарушение функции ЩЖ, а именно, гипотиреоз, приводит к развитию дефицита железа. В группе риска — все менструирущие и беременные женщины, вегетарианцы, пациенты с пониженной секрецией соляной кислоты в желудке. Дефицит железа снижает уровень Т3 на 43% и Т4 на 67% и приводит к самому распространенному заболеванию — гипотериозу. Целевые показатели — 80-100 мкг/л.
Витамин D
D-гормон необходим для иммунной системы и правильной работы вообще всех эндокринных желез. Низкий уровень витамина D в разы повышает риск аутоиммунного тиреоидита. Целевые показатели витамина D — 65-100 нг/мл, но если у вас уже диагностировали АТ, то не менее 100.
Какие еще микроэлементы и витамины важны для щитовидной железы?
Магний, цинк, витамины А, В1, 12, тирозин — их дефицит необходимо восполнить.
3. Препараты, которые нарушают работу щитовидной железы
Отказаться от этих медикаментов не всегда представляется возможным, но если вы их принимаете, то нужно иметь в виду, что они влияют и на щитовидную железу:
Некоторые антиаритмические препараты могут содержать слишком высокие дозы йода, что повышает вероятность гипер- или гипотериоза.
Препараты, содержащие литий — чаще всего используются для лечения депрессии и биполярных расстройств. Накапливаются в щитовидной железе и блокируют синтез тиреоидных гормонов.
Фторсодержащие препараты — снижают функцию щитовидной железы. К ним относятся некоторые антидепрессанты, антибиотики, статины, противогрибковые и медикаменты для лечения артрита. Избыточное количество фтора мы можем получать и с зубной пастой.
Препараты для снижения кислотности желудка.
Бета-блокаторы — замедляют конверсию Т4 в Т3
Ботокс — в меньшей степени, однако не рекомендован при аутоиммунном тиреоидите.
4. Как понять, что с щитовидной железой не все в порядке?
Симптомы заболеваний щитовидной железы, которые должны насторожить:
5. Как проверяем щитовидную железу?
Шаг 1 — делаем температурный тест
Шаг 2 — сдаем анализы на гормоны щитовидной железы, делаем УЗИ
Ориентируемся на следующие показатели лабораторных анализов:
6. Что делать, если на УЗИ обнаружены узлы щитовидной железы?
1. Не паниковать. Хорошо, что вы вообще о них узнали. Большинство узлов не опасны. По статистике, у каждой 2 женщины они есть.
2. Если размер узла превышает 1 см, то нужно сделать пункционную биопсию. Только после лабораторного исследования образца ткани врач сможет определить, состоит ли узел из доброкачественных клеток, или существует онкологический риск. Доброкачественный узел не перерождается в рак.
3. Сдать анализ на гормоны щитовидной железы, чтобы понять, не нарушена ли ее функция. При гиперфункции (гипертериозе) и наличии узлов нужно точно определить источник избытка гормонов, потребуется сцинтиграфия с технецием.
Хорошо, а что дальше делать с узлами?
Доброкачественные — наблюдаем у врача
7. Гипертериоз (тиреотоксикоз, гиперфункция щитовидной железы)
При тиреотоксикозе беспокоят:
Кроме того, гипертериоз — это наследственное заболевание, которому часто сопутствуют и другие аутоиммунные патологии.
8. Токсический зоб — это опасно?
Нет, но это очень и очень неприятное аутоиммунное заболевание. Переизбыток тиреоидных гормонов отравляет организм, а проблема заключается даже не в щитовидной железе, а в иммунной системе.
Контролировать его и бороться с симптомами очень не просто. Сердцебиение, потеря веса, тремор, выраженная слабость, утомляемость, раздражительность, дискомфорт, жжение, давление в глазах — диагноз можно поставить с порога.
При этом на УЗИ часто выявляют гиперплазию щитовидной железы, диффузные изменение, усиление кровотока. В некоторых случаях опухоль может быть настолько большой, что увидеть ее легко и без УЗИ — она приводит к деформации шеи, мешает глотать и дышать.
Пациенту назначается консервативная медикаментозная терапия (1-1,5 года). Помогает она не всегда — после отмены препаратов только в 30% случаев наступает ремиссия.
Если терапия не помогла, щитовидную железу полностью удаляют. Другой вариант — лечение радиоактивным йодом.
9. Операция на щитовидной железе — это опасно?
При наличии пограничных опухолей, опасных онкогенных узлов и токсических зобов, которые не поддаются консервативному лечению, операция по удалению щитовидной железы или ее части может быть единственным способом восстановить здоровье и даже сохранить жизнь.
Операции на щитовидной железе у многих до сих пор ассоциируются с рубцом на шее, который приходится скрывать, чтобы никого не пугать и не провоцировать лишние вопросы. Сегодня такие операции выполняются с применением эндовидеохирургической техники:
Гормонозаместительная терапия, и тем более пожизненная, назначается не всегда!
10. Гипотиреоз
Когда в организме слишком мало Т4, развивается гипотиреоз — противоположность гипертериоза. Обмен веществ замедляется, лишняя жидкость и продукты распада хуже выводятся, человек набирает вес. Причин для его возникновения много, в том числе и недостаток йода. Еще одна важная и коварная — аутоиммунный тиреоидит: в этом случае иммунитет принимает щитовидную железу за опасное инородное тело и начинает разрушать её. Клеток становится мало, и уровень тироксина снижается.
Причины гипертериоза (стараемся их избегать):
Влияние йодной профилактики на активность аутоиммунного тиреоидита при беременности
ГБОУ ВПО Пермская государственная медицинская академия им. академика Е.А. Вагнера Минздрава России; ООО «Консультативно-диагностический центр «Профимед», Пермь, Россия
Цель исследования. Оценка тиреоидного статуса у беременных с аутоиммунным тиреоидитом, проживающих в условиях йодного дефицита, в зависимости от длительности приема препаратов йода.
Материал и методы. Обследована группа беременных с аутоиммунным тиреоидитом в количестве 64 человек. Изучен тиреоидный статус (уровень тиреотропного гормона, свободного тироксина, антител к тиреопероксидазе и тиреоглобулину, ультразвуковая характеристика щитовидной железы) у пациенток с ранним и поздним началом йодной профилактики.
Результаты. Не выявлено достоверных различий в динамике тиреоидного статуса на протяжении беременности у пациенток с аутоиммунным тиреоидитом в группах с ранним и поздним началом йодной профилактики. Отмечена тенденция к меньшей потребности в заместительной терапии L-тироксином среди беременных, рано начавших йодную профилактику. Заключение. Прием физиологических доз йода во время беременности не только не оказывает негативного влияния на активность аутоиммунного процесса, но и способствует более стабильному функциональному состоянию щитовидной железы как при беременности, так и в послеродовом периоде у пациенток с аутоиммунным тиреоидитом.
Роль йода в патогенезе аутоиммунных заболеваний щитовидной железы (ЩЖ) является предметом многолетних дискуссий в мировом научном сообществе. Известные данные по этому вопросу крайне противоречивы. Многочисленные исследования свидетельствуют о потенцирующем действии йода в отношении аутоиммунных тиреопатий. Так, отмечена высокая частота аутоиммунного тиреоидита (АИТ) в регионах с высоким потреблением йода [1]. Установлен факт повышения заболеваемости тиреотоксикозом после массовой йодной профилактики в эндемичных районах [2]. Выявлено, что введение йода с пищей пациентам с нетоксическим зобом приводит к повышенной заболеваемости АИТ [3]. Доказано, что введение фармакологических доз йода может приводить к появлению тиреоидных антител у генетически предрасположенных лиц. В экспериментах на мышах была показана возможность йод-индуцированного тиреоидита [4]. В научном мире обсуждаются также механизмы, посредством которых йод может потенцировать развитие АИТ. Ранее считалось, что избыточное потребление йода приводит к усиленному йодированию тиреоглобулина, который в результате этого становится более иммуногенным. Предполагалось также, что избыток йода вызывает образование активных радикалов йода, разрушающих мембраны эпителиальных клеток ЩЖ. Последние исследования продемонстрировали, что высокие дозы йода усиливают апоптоз клеток ЩЖ, что может ускорять гибель тироцитов под действием аутоиммунной агрессии [5]. В то же время ряд исследований не выявил негативного влияния физиологических доз йода на аутоиммунные процессы в ЩЖ [6, 7]. Более того, некоторые авторы считают, что дефицит йода может являться предиктором гипофункции ЩЖ у пациентов с АИТ [8]. Как подчеркивает Н.А. Петунина [9], риск развития или прогрессирования АИТ определяется тремя факторами: дозой йода, исходным уровнем его потребления (регионом проживания) и генетической предрасположенностью к аутоиммунным заболеваниям ЩЖ. С практической точки зрения важно понять, может ли коррекция йодного дефицита до физиологической нормы (йодная профилактика) вызывать или усугублять тиреоидные аутоиммунные реакции. В частности, этот вопрос актуален для беременных с АИТ, проживающих в условиях йодного дефицита и нуждающихся в йодной профилактике в интересах плода.
Целью нашего исследования стала оценка тиреоидного статуса у беременных с АИТ, проживающих в условиях йодного дефицита, в зависимости от длительности приема препаратов йода.
Материал и методы исследования
Обследовано 64 беременных с сопутствующим АИТ, состоявших на диспансерном учете в женских консультациях Перми (основная группа). Данная группа была разделена на две подгруппы (по 32 человека в каждой): IА – с ранним началом йодной профилактики (на этапе прегравидарной подготовки или до 12 недель беременности) и IБ – с поздним началом йодной профилактики (после 12 недель беременности или совсем не получавшие йодной дотации). Группу сравнения составили 25 беременных, не имевших анамнестических и клинических данных о заболеваниях ЩЖ и получавших препараты йода с раннего срока беременности. Все беремен.
Коррекция йодной недостаточности: влияние физиологических доз йода на функциональное состояние щитовидной железы и активность аутоиммунных процессов
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Эндокринологический научный центр РАМН, Москва
Д ефицит йода и связанные с ним заболевания (ЙДЗ) в последние годы приобрели острую социальную значимость и стали одной из приоритетных проблем отечественного здравоохранения.
Во многих регионах Российской Федерации сегодня вводится программа йодной профилактики. В качестве ее основного метода используется йодированная пищевая поваренная соль – эффективный и экономичный способ восполнения дефицита йода на уровне всей популяции [3, 28].
В районах с легкой и умеренной йодной недостаточностью массовая йодная профилактика в большинстве случаев способна обеспечить достаточное поступление йода в организм. Но в определенные периоды жизни, когда потребность в йоде значительно возрастает (подростковый период, беременность, грудное вскармливание), вводимого с солью йода может не хватать, и тогда для восполнения дефицита йода требуется проведение групповой и индивидуальной йодной профилактики препаратами, содержащими физиологическую дозу йода [16, 17]. Регулярное поступление стандартной дозы йода в составе таблетированных препаратов позволяет поддерживать постоянную концентрацию микроэлемента в организме.
Использование физиологических доз йода для компенсации дефицита этого микроэлемента приводит в отдельных случаях к развитию йодиндуцированного тиротоксикоза (ЙИТ). ЙИТ чаще развивается у лиц с автономными образованиями в щитовидной железе [21]. В целом же физиологические дозы йода для организма безвредны (рекомендации Международного Комитета по контролю ЙДЗ, ЮНИСЕФ, ВОЗ ) [25, 40].
С момента проведения йодной профилактики среди ученых обсуждается вопрос о возможной роли йода в индукции и/или манифестации аутоиммунных процессов в щитовидной железе [10,31]. На сегодняшний день имеются лишь косвенные доказательства роли йода в развитии аутоиммунной патологии. Они получены в ходе экспериментов на животных и при проведении эпидемиологических исследований, в которых сравнивалась частота аутоиммунных заболеваний щитовидной железы в районах с нормальным и недостаточным потреблением йода.
Доказано, что введение фармакологических доз йода может приводить к появлению тиреоидных антител у генетически предрасположенных лиц [33]. Развитие неблагоприятных побочных эффектов после введения фармакологических доз йода закономерно поставило вопрос, может ли коррекция йодной недостаточности привести к развитию аутоиммунных заболеваний щитовидной железы? Теоретически такая возможность обсуждалась [11,12]. Однако исследования взаимосвязи между проведением йодной профилактики и последующим развитием аутоиммунных заболеваний не дали убедительных результатов [9].
С учетом вышеизложенного представлялось важным провести изучение возможных эффектов физиологических доз йода на активность аутоиммунных процессов и функцию щитовидной железы у лиц, проживающих в йоддефицитных районах.
Материалы и методы
Для проведения исследований были отобраны два учреждения Юго–западного округа г. Москвы: швейная фабрика (ШФ) и профессионально–техническое училище (ПТУ). Всего был обследован 1301 человек (645 учащихся ПТУ и 656 сотрудников ШФ). Данные пальпации оценивались по классификации ВОЗ (1994) [39].
Для более детального обследования были сформированы 2 группы женщин, имеющих пальпаторное увеличение щитовидной железы:
1–я группа – 70 человек, в возрасте от 20 до 55 лет (сотрудницы ШФ),
2–я группа – 50 человек, в возрасте от 16 до 20 лет (учащиеся ПТУ).
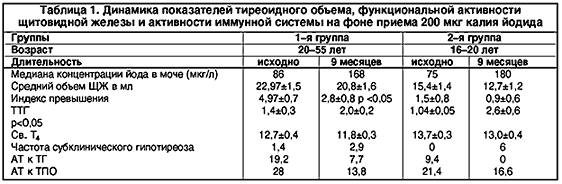
Программа исследования включала ультразвуковое исследование щитовидной железы, определение концентрации йода в моче, исследование содержания тиреотропного гормона гипофиза (ТТГ), свободного тироксина (св. Т4), антител к тиреоглобулину (АТ к ТГ), антител к пероксидазе (АТ к ТПО).
Тиреоидная сонография осуществлялась с использованием портативного сканера ALOKA 500 с датчиком 7,5 мгц. Измерения проводились в продольной и поперечной плоскости для правой и левой доли. Объем щитовидной железы рассчитывался по формуле Bruno:
[(шп x дп x тп)] + [(шл x дл x тл)] x 0,479 = объем,
где: шп, дп, тп, шл, дл, тл – соответственно ширина, длина и толщина правой и левой долей железы; 0,479 – коэффициент поправки на эллипсоидность. Полученные данные оценивались по нормативам F. Delang (1997) [18], рассчитанным относительно площади поверхности тела (ППТ).
Площадь поверхности тела (ППТ) рассчитывалась по формуле:
где В – вес в кг и Р – рост в см.
У женщин старше 18 лет объем щитовидной железы не должен превышать 18 мл.
За частоту зоба в популяции принимали все случаи превышения фактического объема щитовидной железы над верхней границей нормы (97 перцентиль). В процессе исследования для оценки величины зоба использовали показатель – индекс превышения (ИП) – среднее превышение объема щитовидных желез над верхним пределом нормы.
Концентрацию йода определяли в разовой порции мочи церий–арсенитовым методом в лаборатории клинической биохимии ЭНЦ РАМН (руководитель – д.м.н. Б.П. Мищенко).
Определение базального уровня ТТГ, св. Т4, в сыворотке крови проводилось в лаборатории гормонального анализа ЭНЦ РАМН (руководитель – проф. Н.П. Гончаров) с использованием автоматической иммунотест–системы Vitros. Границы нормы для базального уровня ТТГ – от 0,3 до 3,5 мЕ/л, св. Т4 – от 10 до 20 пмоль/л. АТ к ТГ и ТПО были определены иммуноферментным методом с использованием наборов фирмы «DRG» (США). Границы нормы для антител к ТГ и к ТПО Результаты исследования
До приема препарата в 1–й группе средний объем щитовидной железы по данным УЗИ составил 22.97±1,5 мл, при колебаниях от 18,8 до 28,2 мл. У 1,4% лиц выявлен субклинический гипотиреоз. 19,2% лиц имели повышенные титры АТ к ТГ и 28% – АТ к ТПО.
Во 2–й группе средний объем щитовидной железы составил 15.4±1,4 мл, при колебаниях от 5,0 до 28,5 мл. АТ к ТГ выявлены у 9,4% подростков, АТ к ТПО – у 21,4%. Функциональное состояние щитовидной железы по данным исследования тиреоидных гормонов и ТТГ расценено, как эутиреоидное. Данные исследования представлены в таблице 1.
Район считается свободным от йодного дефицита, если медиана концентрации йода в моче в популяции превышает 100 мкг/л.
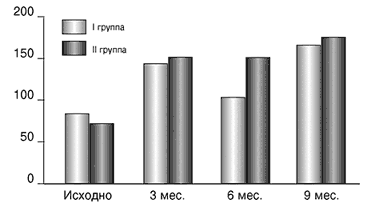
В 1–й группе медиана концентрации йода в моче до и на фоне приема 200 мкг калия йодида варьировала от 86 до 168 мкг/л. Во 2–й группе – от 75 до 180 мкг/л. На рисунке 1 представлены данные исследования экскреции йода в разные периоды наблюдения.
Рис. 1. Медиана концентрации йода в моче на фоне приема калия йодида 200 мкг в разные периоды наблюдения
В 1–й группе средний объем щитовидной железы через 9 месяцев уменьшился от 22,97±1,5 мл до 20,8±1,6 мл (p > 0,5). Индекс превышения (ИП) – среднее отклонение объема щитовидной железы от верхней границы нормы (97 перцентили) уменьшилось от 4,97±0,7 мл до 2,8±0,8 мл (p 0,1), при колебаниях от 0,5 до 6,7 мЕ/мл до лечения и от 0,3 до 8,9 мЕ/мл через 9 месяцев. Уровень св. Т4 уменьшился от 12,7±0,4 до 11,8±0,3 пмоль/л (p > 0,1), но недостоверно, при колебаниях от 9,8 до 16,9 и от 9,1 до 15,2 пмоль/л, соответственно. По данным лабораторного исследования субклинический гипотиреоз был выявлен у 2,9% лиц.
АТ к ТГ были обнаружены только у 7,7% женщин. Уровень антител варьировал от 24 до 106 UV/ml до лечения и от 10 до 1400 UV/ml через 9 месяцев. Высокий уровень антител имела больная с клиникой аутоиммунного тиреоидита (диагноз был поставлен до начала лечения).
Через 9 месяцев антитела к ТПО были выявлены у 13,8% лиц. Уровень антител варьировал от 14 до 126 Uv/ml до лечения и от 10 до 316 Uv/ml через 9 месяцев.
Во 2–й группе объем железы уменьшился от 15,4±1,4 до 12,7±1,2 мл (p > 0,5). Индекс превышения уменьшился от 1,5±0,8 до 0,9±0,6. У 16,3% подростков объем щитовидной железы нормализовался.
Уровень ТТГ достоверно увеличился от 1,04 ±0,05 до 2,6±0,6 мЕ/мл (p Обсуждение
Методом групповой и индивидуальной йодной профилактики является назначение стандартной дозы йода в виде йодсодержащих препаратов. В своем исследовании для восполнения йодной недостаточности в районах с легким дефицитом йода мы использовали препарат калия йодид 200, содержащий физиологическую дозу йода.
Проанализировав результаты исследования, мы не выявили существенного влияния физиологических доз йода на функциональное состояние щитовидной железы, но отметили снижение частоты встречаемости антител к тиреоидной ткани.
Средний уровень ТТГ и тиреоидных гормонов существенно не изменился на фоне лечения. Развитие субклинического гипотиреоза у лиц с исходно повышенным титром тиреоидных антител могло быть обусловлено прогрессированием аутоиммунного процесса вследствие естественного течения заболевания.
Обращает на себя внимание снижение частоты встречаемости и титров антител к ТГ и ТПО в процессе приема препарата, что свидетельствует об отсутствии стимулирующего влияния физиологических доз йода на активность аутоиммунных процессов. С другой стороны данные подтверждают, что тиреоидные антитела в невысоких титрах большого клинического значения не имеют.
Медиана концентрации йода в моче, как показатель йодной обеспеченности, варьировала в диапазоне 100 – 200 мкг/л, т.е. была в пределах установленной нормы.
Объем щитовидной железы на фоне лечения уменьшился, но не достоверно: у лиц старше 20 лет на 9,8%, у подростков – на 17,5%.
Однако на фоне лечения отмечено значительное уменьшение объема железы у пациентов, имеющих зоб. Индекс превышения, т.е. среднее отклонение объема железы от верхнего предела нормы, уменьшился на 43,7% у лиц в возрасте от 20 до 59 лет (p 0,5).
В предыдущих исследованиях [2,4] мы показали высокую эффективность использования физиологических доз йода 100–150 мкг для профилактики и лечения эндемического зоба у детей школьного возраста в районах с легкой и умеренной степенью йодной недостаточности: частота зоба через 6 месяцев от начала приема препарата снизилась в 2 раза, объем щитовидной железы уменьшился на 18,2%. В настоящем исследовании прием калия йодида 200 оказался более эффективным у подростков по сравнению с лицами детородного возраста.
Во время проведения йодной профилактики следует принимать во внимание вероятность увеличения частоты ЙИТ в популяции, особенно у лиц старше 45 лет, имеющих узловые образования в щитовидной железе, даже при относительно небольшом возрастании потребления йода [13,14]. Наибольшая встречаемость ЙИТ в старших возрастных группах определяет и клинику заболевания: у больных преобладают кардиальные симптомы и депрессивное состояние.
О случаях ЙИТ сообщено из разных стран: США, Голландии, Австрии, Югославии и Австралии. После введения йодной профилактики в этих странах увеличение случаев тиреотоксикоза носило транзиторный характер и несмотря на продолжающуюся йодную профилактику снижалось к исходному [6,27,35].
Важно подчеркнуть, что проведение йодной профилактики предупреждает развитие диффузной и узловой автономии щитовидной железы и, следовательно, ЙИТ в дальнейшем. В этой связи ЙИТ в настоящее время рассматривают, как одно из проявлений йоддефицитной патологии [37]. ЙИТ может иметь тяжелые последствия в основном со стороны сердечно–сосудистой системы, и приводить к недостаточности кровообращения, фибрилляции предсердий, ухудшению течения сопутствующих сердечных заболеваний [20]. Диагностика ЙИТ нередко затруднена, особенно в случаях «субклинических» форм заболевания и у лиц пожилого возраста, в то время как раннее выявление и своевременное лечение ЙИТ может предотвратить серьезные осложнения.
Возможность развития ЙИТ требует повышенного внимания работников здравоохранения к состоянию здоровья лиц, подверженных риску заболеть явным тиреотоксикозом. Важнейшей мерой по предупреждению ЙИТ является организация мониторинга йодного потребления и его биологического действия. Если йодная профилактика осуществляется посредством йодирования поваренной соли, необходимо контролировать другие источники йода, особенно различные пищевые добавки, доза йода в которых не нормирована.
Высокие уровни йода в моче и в соли предполагают, что у ряда лиц обязательно разовьется ЙИТ. Для выявления ЙИТ необходимо следить за регистрацией всех случаев тиреотоксикоза в амбулаторных и стационарных учреждениях. Кроме того, необходимо повышать уровень знаний медицинского персонала. Полная информация о ЙИТ должна включаться в программы обучения в медицинских институтах и на курсах усовершенствования врачей.
Тем не менее многие люди регулярно принимают огромные дозы йода – от 6 до 200 мг в день без каких–либо побочных эффектов. Например, в составе амиодарона, йодсодержащих рентгеноконтрастных препаратов [23].
Лица, не имеющие патологии щитовидной железы в анамнезе, как правило, сохраняют толерантность к приему больших доз йода и остаются эутиреоидными. Мировой опыт, накопленный в течение многих лет, свидетельствует о безопасности проведения йодной профилактики, что отмечено в Заявлении Всемирной Организации Здравоохранения в 1996 году [38].
Введение йода как в органической, так и в неорганической форме может приводить к неблагоприятным реакциям со стороны щитовидной железы, которые включают не только развитие тиреотоксикоза, но и гипотиреоза с увеличением или без тиреоидного объема, а также к запуску аутоиммунных реакций [1].
Эксперименты на животных показали, что йод стимулирует или усиливает проявления тиреоидита как за счет увеличения иммуногенности тиреоглобулина, так и за счет повреждения щитовидной железы свободными радикалами [36]. Введение йода чувствительным линиям цыплят и крыс (BB/W, Obese – strain), предрасположенным к развитию тиреоидита, приводит к увеличению титров АТ к ТГ и ТПО, а также лимфоидной инфильтрации щитовидной железы. То же количество йода не оказывает соответствующего эффекта у особей нормальной линии. Из этого следует, что йодиндуцированные тиреоидиты развиваются у генетически предрасположенных животных. В то же время назначение пищевого рациона с низким содержанием йода или препаратов, блокирующих поступление йода в щитовидную железу или органификацию йода (метимазол, пропилтиоурацил), предупреждает синтез АТ к ТГ и ТПО, лимфоидную инфильтрацию и сохраняет эутиреоидный статус у чувствительной линии крыс и цыплят, в то время как у нелеченных особей выраженная лимфоидная инфильтрация и гипотиреоз развиваются в первые 5 недель жизни.
Другие исследования показали, что высокойодированный тиреоглобулин более иммуногенен, чем низкойодированный, и это непосредственно связано с формированием йодированных тиронинов в молекуле тиреоглобулина, т.к. иммунизация высокойодированным тиреоглобулином увеличивала содержание антител к Т3 и Т4 [15,19].
Хорошо известно, что йод может повреждать тиреоциты при определенных условиях. Высокие дозы йода могут вызывать некроз гиперплазированных тиреоцитов у нормальных животных и тиреоидных фолликулов человека in vitro [29]. Если же активность пероксидазы блокирована, повреждение может не произойти, что указывает на оксидант–опосредованный механизм йодиндуцированного повреждения. Кроме того, для развития йодопосредованного окислительного повреждения у животных необходимой предпосылкой является высокая стимуляция щитовидной железы эндогенным ТТГ.
Изучение эффектов антиоксидантов показало, что разрушение, вызванное йодом, опосредуется кислородными радикалами. Так, например, введение экзогенных антиоксидантов или дефицит внутриклеточных антиоксидантов могут ослаблять либо потенцировать эффекты йода, уменьшая или усиливая тяжесть тиреоидитов [7].
Первичное повреждение щитовидной железы является важным фактором в развитии аутоиммунных тиреоидитов у генетически предрасположенных животных.
В то время как роль йода в запуске или обострении аутоиммунной патологии у животных доказана в экспериментах, участие его в патогенезе аутоиммунных заболеваний щитовидной железы человека все еще обсуждается. Имеются лишь косвенные доказательства, что длительный избыток йода может провоцировать развитие аутоиммунных заболеваний щитовидной железы у предрасположенных лиц.
Так, в недавнем исследовании, проведенном в различных районах Англии и Уэльса [32], не было установлено связи между уровнем АТ к ТГ, ТПО, распространенностью зоба и уровнем потребления йода. Авторы пришли к выводу, что генетическая предрасположенность к заболеваниям щитовидной железы, а не различия в потреблении йода, является главной причиной появления тиреоидных антител.
Несмотря на то, что в большинстве эпидемиологических исследований установлена взаимосвязь между уровнем потребления йода и частотой аутоиммунной патологии щитовидной железы, некоторые работы свидетельствуют, что у лиц с эндемическим зобом также распространены аутоиммунные феномены. В частности, более высокая частота АТ к ТГ, ТПО была обнаружена в районах с умеренной йодной недостаточностью по сравнению с йодобеспеченными районами [22].
Переоценка проблемы была произведена после обследования, проведенного в Сардинии, целью которого было изучение распространенности и географическое распределение АТ к ТГ и ТПО и зоба у школьников 6–14 лет в 28 населенных пунктах острова [30]. Дополнительно исследовались антитела к островковым клеткам поджелудочной железы (АОК), так как распространенность диабета I типа в Сардинии высока. Результаты исследования показали колебания уровня АТ к ТГ и ТПО (0–8.7%) и зоба (11–48%) в разных районах. Корреляция между этими показателями отсутствовала. Не было корреляции между АТ к ТГ и ТПО, АОК и тяжестью зобной эндемии. Исследователи пришли к выводу, что в запуске аутоиммунных реакций главную роль играют генетические и/или факторы окружающей среды независимо от уровня потребления йода.
По аналогии с экспериментальными моделями на животных можно предположить, что введение йода способно модулировать активность и/или клинические проявления аутоиммунных заболеваний щитовидной железы у генетически предрасположенных людей.
После введения йодной профилактики в США [34] ремиссия аутоиммунного тиреотоксикоза на фоне приема антитиреоидных препаратов наступала в более отдаленные сроки. Частота рецидивов аутоиммунного тиреотоксикоза после тиреоидэктомии была выше в районах с избыточным потреблением йода, чем в районах с нормальным его потреблением. Одинаковые дозы антитиреоидных препаратов чаще вызывали развитие гипотиреоза у пациентов, проживающих в йоддефицитных районах, чем в йодобеспеченных. За последние 50 лет после введения йодной профилактики было отмечено увеличение распространенности тиреоидита Хашимото (с другой стороны, это можно объяснить появлением новых методов обследования и улучшением качества диагностики).
В эндемичных районах Греции после введения йодной профилактики увеличилась частота встречаемости АТ к ТГ и ТПО, в то время как введение йодной профилактики в Финляндии не привело к увеличению частоты гипотиреоза и аутоиммунного тиреоидита [8,26].
Изучая эффекты введения 400 мг йода в составе пролонгированного препарата йодированного масла (липиодола) у лиц детородного возраста без патологии щитовидной железы, мы не выявили его влияния на функцию щитовидной железы и активность аутоиммунных процессов [5,24].
В настоящем исследовании мы показали, что назначение физиологических доз йода в составе препарата калия йодида 200 с целью профилактики и лечения диффузного эндемического увеличения щитовидной железы у лиц старше 16 лет, проживающих в районах с легкой степенью йодной недостаточности, оправдано и эффективно. Риск развития йодиндуцированных состояний при введении физиологических доз йода лицам без узловых образований в щитовидной железе практически отсутствует.
Однако в настоящее время у населения нет достаточной мотивации проведения индивидуальной йодной профилактики, что сказывается на результатах профилактических мероприятий. Лица, включенные в настоящее исследование, принимали препарат нерегулярно, особенно подростки, ссылаясь на забывчивость, безразличие к своему состоянию, отсутствие возможности приобрести препарат.
1. Групповая и индивидуальная йодная профилактика в районах с легкой степенью йодной недостаточности с использованием калия йодида в дозе 200 мкг в сутки приводит к снижению частоты зоба и уменьшению объема щитовидной железы, а также обеспечивает нормальную экскрецию йода с мочой у подростков и лиц детородного возраста.
2. Физиологические дозы йода у лиц без патологии щитовидной железы не оказывают существенного влияния на ее функциональное состояние и активность аутоиммунных процессов. У лиц с исходно повышенным титром тиреоидных антител отмечается снижение их уровня в процессе коррекции йодной недостаточности.
3. Профилактические дозы йода в составе калия йодида 200 не провоцируют манифестацию аутоиммунных процессов в щитовидной железе, однако у лиц с доказанной аутоиммунной патологией не исключено обострение заболевания.
4. Проведение групповой и индивидуальной йодной профилактики не требует предварительного обследования с целью исключения аутоиммунной патологии.
Список литературы Вы можете найти на сайте http://www.rmj.ru
Калия йодид 200 Берлин–Хеми (торговое название)
1. Герасимов Г.А., Петунина Н.А. Йод и аутоиммунные заболевания щитовидной железы // Пробл. эндокринол. – 1993.– № 3 – С.52– 54.
2. Дедов И.И., Герасимов Г.А., Свириденко Н.Ю. и др. Использование таблетированных препаратов йода для профилактики эндемического зоба // Пробл. эндокринол.– 1998.–N 1.– С. 24–27
3. Дедов И.И., Юденич О.Н., Герасимов Г.А., Смирнов Н.П. Эндемический зоб. Проблемы и решения // Пробл. эндокринол. – 1992.– T.38 – N З. – С. 6–15.
4. Петеркова В.А., Герасимов Г.А., Свириденко Н.Ю. и др. Альтернативные методы проведения йодной профилактики с целью компенсации йодной недостаточности у детей. Применение в качестве йодной профилактики поливитаминного препарата юникап М и йодида калия // Педиатрия.– 1996.– N6.– С. 72–75
5. Свириденко Н.Ю., Майорова Н.М., Назаров А.Н. и др. Использование препарата иодированного масла (липиодол) в районах с умеренной йодной недостаточностью // Проб. эндокринол.- 1995.- №6.- С. 8- 11.
6. Свириденко Н.Ю., Майорова Н.М., Назаров А.Н. и др. Использование препарата иодированного масла (липиодол) в районах с умеренной йодной недостаточностью // Пробл. эндокринол.– 1995.– №6.– С. 8 – 11.
8. Adams D., Kennedy T., Stewart J. Hyperthyroidism in Tasmania following iodide supplementation: measurments of thyroid– stimulating autoantibodies and thyrotropin // J. Clin. Endocrinol. Metab. – 1975. – Vol.41 – N. 2.– P.221–228.
9. Bagchi N, Brown TR, Herdegen DM, Dhar A et al. Antioxidants delay the onset of thyroiditis in Obese strain chickens. // Endocrinol. – 1990 – Vol.127 – P.1590–1595.
10. Boukis M.A., Koutras D.A., Souvatzoglou A. Thyroid Hormone and Immunological Studies in Endemic Goiter//J. Clin. Endocrinol. Metab. – 1983. – Vol.57 – N. 4. – P.859–862.
11. Bourdoux P., Mahangaiko E., Batende J. et al. Iodine–induced thyrotoxicosis five years after iodine supplementation // J. Endocrinol. Invest.– 1999.–Vol.22, Suppl. №6.–P.120
12. Boyages S.C., Bloot A.M., Maberly G.F. Thyroid autoimmunity in endemic goitre caused by excessive iodine intake // Clin. Endocrinol. – 1989.– Vol.31 – N. 4 – P.453–465.
13. Braverman L. Adequate iodine intake: the good far outweighs the bad //Eur.J. Endocrinol.–1998.–Vol.139,№1.–P.14–15.
14. Bravermann L. Iodine induced thyroid disease // AMA. – 1990. – Vol. 17 – P. 29–33
15. Corvilain B., Sande J., Dumont J. Autonomy in endemic goiter // Thyroid. – 1998. – Vol.8. – N.1. – P. 107–113.
16. Galofre J., Fernandez–Calvet L., Rios M., Garcia–Mayor R. Increased incidence of thyrotoxicosis after iodine supplementation in an iodine sufficient area //J. Endocrinol. Invest. – 1994 – Vol. 17. – P. 23–27
17. Champion BR, Rayner DC, Byfield PGH, Page CTJ et al. Critical role of iodization for T cell recognition of thyroglobulin in experimental murine thyroid autoimmunity. // J. Immunol. – 1987. – Vol. 139. – P.3665–3670.
18. Glinoer D. Maternal and neonatal thyroid function in mild iodine deficiency // In: The thyroid and iodine. – Stuttgart, New York – 1996 – P. 129–143.
19. Glinoer D., De Nayer P., Delange F., Lemone M., et al. A randomized trial for the treatment of mild iodine deficiency during pregnancy: maternal and neonatal effects //J. Clin. Endocrinol. Metab. – 1995. – V. 80 – P. 258–269
20. Delange F, Benker G., Caron P. et al. Thyroid and urinary iodine in European schoolchildren: standardization of values for assessment of iodine deficiency //Eur. J. Endocrinol. – 1997. – Vol. 136. – P. 180–187.
21. Ebner SA, Lueprasitsakul W, Alex S, Fang SL et al. Iodine content of rat thyroglobulin affects its antigenicity in inducing lymphocytic thyroidits in the BB/W or rat. //Autoimmunity. – 1992. – Vol.13. – P. 209–14.
22. Dunn J., Semigran M., Delange F. The prevention and management of iodine–induced hyperthyroidism and its cardiac features // Thyroid. – 1998. – Vol.8. – N.1. – P. 101–106.
23. Dremier S., Coppee F., Delange et al. Thyroid autonomy: mechanism and clinical effects //J. Clin. Endocrinol. Metab.–1996.–N.– 81.–P. 4187–4193.
24. Fenzi G.F., Bartalena L, Lombardi A. Thyroid Autoimmunity and Endemic Goiter // Endocr. Exp. – 1986.–Vol.20 – N.1. – P.49–56.
25. Franklyn J., Sheppard M. Amiodarone and thyroid dysfunction // Trends Endocrinol. Metab. – 1993 – Vol. 4. – P. 128–131.
26. Gerasimov G., Sviridenko N., Delange F. // Iodine in Pregnancy / Eds. J. Stanbury. et al.– New Delhi, 1998.– P. 171–180.
27. ICCIDD. Guidelines for assessment of progress towards IDD elimination // IDD Newsletter.– 1996.– Vol. 12.– P.64.
28. Lamberg B.A. Endemic goitre in Finland and changes duiring 30 of iodine prophilaxis.//Endocrinol. Exper.– 1986. –Vol.20. – P.35–47.
29. Lima N., Medeiros–Neto G. Transient thyrotoxicosis in endemic goiter patients following exposure to a normal iodine intake // Clin. Endocrinol. – 1984. – Vol.21 – N.6. – P.631–637.
30. Mannar M. The iodization of salt the elimination of Iodine Deficiency Disorders // Hetzel B., Pandav C. S.O.S for a Billion. – New Delhi, 1996. – P.99 – 119.
31. Many MC, Mestdagh C, Hove MFVD, Denef JF. In vitro study of acute toxic effects of high iodine doses in human thyroid follicles. // Endocrinol. – 1992. – N. 131. – P. 621–30.
32. Mariotti S., Loviselli A., Cambosu A., Velluzi F. et al. The role of iodine in autoimmune thyroid disease in humans /In: The thyroid and iodine //Stuttgart, New York. – 1996. – P.155–168.
33. Pennington J. A review of iodine toxicity reports // J. Amer. Diet. Assoc. – 1990. – Vol. 90 – P.1571–1581.
34. Prentice L., Phillips D., Sarsero D. et al. Geographical distribution of subclinical autoimmune thyroid disease in Britain: a study using highly sensitive direct assays for autoantibodies to thyroglobulin and thyroid peroxidase // Acta Endocr. (Copenh) – 1990. – Vol.123 – P.493–498.
35. Roti E., Braverman L. Iodine excess and thyroid function. In: The thyroid and iodine //Stuttgart, New York. – 1996. – P. 7 – 17.
36. Roti E., Gardini E., Minelli R., Bianconi L. et al. Effects of chronic iodine administration on thyroid status in euthyroid subjects previously treated with antithyroid drugs for Graves’ Hyperthyroidism //J. Clin. Enocrinol. Metab. – 1993. – Vol. 26. – P. 928 – 932
37. Stanbury J., Ermans A., Bourdoux P. et al. Iodine–induced hyperthyroidism: occurrence and epidemiology //Thyroid. – 1998. – Vol.8. – N.1. – P. 83–100.
38. Sundick R., Bagchi N., Brown T. The role of iodine in experimental thyroiditis. /In: The thyroid and iodine //Stuttgart, New York. – 1996. – P. 148 – 154.
39. WHO: Assessment of Iodine Deficiency Disorders and Monitoring their Elimination. – Geneva, 2001.
40. WHO. Eliminationg Iodine Deficiency Disorders Safely Through Solt Iodization: A WHO Statement.– 1994.–WHO/NUT/94.4
41. WHO: Indicators for Assessing Iodine Deficiency Disorders and their Control Programmes: Report of a Joint WHO/UNICEF/ICCIDD Consultation.– Geneva, 1993.
42. WHO: Recommended iodine levels in salt and guidelines for monitoring their adequacy and effectiveness. – Geneva, WHO/NUT/96.13
43. Wilson R., Mckillop J., Thomson J. The effect of pre–operative potassium iodide therapy on antibody production //Acta Endocr. (Copenh.) – 1990 – Vol. 123 – P. 531 – 534.