Хондрогард®
Инструкция
Торговое название
Хондрогард®
Международное непатентованное название
Лекарственная форма
Раствор для внутримышечного введения 100 мг/мл
Состав
вспомогательные вещества: бензиловый спирт, натрия метабисульфит,
натрия гидроксид, вода для инъекций.
Описание
Прозрачный бесцветный или со слегка желтоватым оттенком раствор с запахом бензилового спирта
Фармакотерапевтическая группа
Нестероидные противовоспалительные препараты другие.
Фармакологическое действие
Фармакокинетика
После внутримышечного введения хондроитина сульфат быстро распределяется. Уже через 30 мин после инъекции он обнаруживается в крови в значительных концентрациях. Максимальная концентрация (Cmax) хондроитина сульфата в плазме достигается через 1 ч, затем постепенно снижается в течение 2 суток.
Хондроитина сульфат накапливается, главным образом, в хрящевой ткани суставов. Синовиальная оболочка не является препятствием для проникновения препарата в полость сустава. В экспериментах показано, что через 15 мин после внутримышечной инъекции хондроитина сульфат обнаруживается в синовиальной жидкости, затем проникает в суставной хрящ, где его Cmax достигается через 48 ч. Выводится из организма в течение 24 часов. Элиминируется преимущественно почками.
Фармакодинамика
При лечении препаратом уменьшается болезненность и улучшается подвижность пораженных суставов. При лечении дегенеративных изменений
суставов с развитием вторичного синовита, положительный эффект может
наблюдаться уже через 2-3 недели после начала введения препарата уменьшается боль в суставах, исчезают клинические проявления реактивного
синовита, увеличивается объем движений в пораженных суставах.
Терапевтический эффект сохраняется длительное время после окончания
Показания к применению
Дегенеративно-дистрофические заболевания суставов и позвоночника:
— остеоартроз с преимущественным поражением крупных суставов
Способ применения и дозы
Препарат назначают внутримышечно по 100 мг через день. При хорошей переносимости дозу увеличивают до 200 мг, начиная с четвертой инъекции.
Побочное действие
Аллергические реакции (кожный зуд, эритема, крапивница, дерматит),
геморрагии в месте инъекции
Противопоказания
— повышенная чувствительность к препарату или к его компонентам
— кровотечения и склонность к кровоточивости
— беременность и период лактации
— детский возраст до 18 лет
Лекарственные взаимодействия
При сочетанном применении с нестероидными противовоспалительными средствами Хондрогард позволяет снизить дозу нестероидных противовоспалительных средств. Препарат усиливает действие непрямых антикоагулянтов, антиагрегантов, фибринолитиков, что требует более частого контроля показателей свертывания крови при совместном применении.
Особые указания
Для достижения стабильного клинического эффекта необходимо не менее 25 инъекций Хондрогарда. Для предупреждения обострений показаны повторные курсы лечения.
Использование в педиатрии
Данные об эффективности и безопасности применения хондроитина сульфата у детей в настоящее время отсутствуют.
Особенности влияния лекарственного средства на способность управлять
транспортным средством или потенциально опасными механизмами
Передозировка
В настоящее время о случаях передозировки хондроитина сульфата не
Форма выпуска и упаковка
Раствор для внутримышечного введения 100 мг/мл.
По 1 мл в ампулы бесцветного нейтрального стекла с цветным кольцом
разлома или с цветной точкой и насечкой и/или с дополнительными
цветными идентификационными кольцами или иной кодировкой.
По 5 ампул в контурной ячейковой упаковке из пленки поливинилхлоридной
и фольги алюминиевой, или пленки полимерной, или без фольги и пленки.
По 2 контурные ячейковые упаковки вместе с инструкцией по медицинскому
применению на государственном и русском языках в пачке из картона.
Условия хранения
Хранить в защищённом от света месте при температуре не выше 25°С.
Хранить в недоступном для детей месте!
Срок хранения
Не использовать по истечении срока годности.
Условия отпуска из аптек
Производитель
Закрытое акционерное общество «ФармФирма «Сотекс», Россия
141345, Московская обл., Сергиево-Посадский муниципальный район,
сельское поселение Березняковское, пос. Беликово, д. 11
Тел./факс: (495) 956-29-30.
Наименование и страна владельца регистрационного удостоверения
Закрытое акционерное общество «ФармФирма «Сотекс», Россия
Адрес организации, принимающей на территории Республики Казахстан
претензии от потребителей по качеству продукции (товара)
ТОО «EL Company (ЕЛ компани)», Республика Казахстан,
Исследование эффективности, переносимости и безопасности препарата Хондрогард у пациентов с остеоартрозом
Л.И. Алексеева, С.Г. Аникин, Е.М. Зайцева, Н.Г. Кашеварова, Т.А. Короткова, Е.П. Шарапова, Н.В. Чичасова, Г.Р. Имаметдинова, Н.В. Бадокин, С.А. Колова
ФГБУ НИИР РАМН, Москва
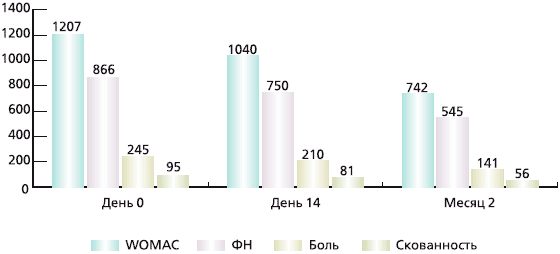
Представлены результаты исследования по оценке эффективности, переносимости и безопасности внутримышечного введения хондроитина сульфата (ХС) больным остеоартрозом (ОА) коленных суставов. В 2-месячном проспективном исследовании приняли участие 70 человек, 67 (96 %) женщин и 3 (4 %) мужчины в возрасте 45-70 лет с первичным ОА коленных суставов II (79 %) и III (21 %) рентгенологических стадий по Kellgren-Lawrence, нуждавшихся в приеме нестероидных противовоспалительных средств (НПВС). Препарат ХС Хондрогарт вводили внутримышечно через день (всего 30 инъекций), исследование завершили 66 (94 %) человек. Результаты исследования показали, что терапевтический эффект наступал в среднем на 23-й день от начала лечения. Таким образом, Хондрогард обладает достоверным симптоматическим эффектом, уменьшая боль, скованность и улучшая функциональные показатели. Преимуществом препарата являются быстрое наступление эффекта, возможность отмены или снижения дозы НПВС на фоне лечения и хорошая переносимость. Препарат Хондрогард может быть рекомендован лицам, страдающим ОА, в качестве первого средства, дающего более быстрый эффект с последующей заменой его на пероральные формы.
Ключевые слова: остеоартроз, нестероидные противовоспалительные средства, хондроитина сульфат
The results of the study aimed to evaluation the efficacy, tolerability and safety of intramuscular administration of chondroitin sulfate (CS) in patients with osteoarthrosis (OA) of the knee are presented. The 2-month prospective study involved 70 patients, 67 (96 %) women and 3 (4 %) men aged 45-70 years with primary OA of knee joints II (79 % ) and III (21 %) radiographic stages by Kellgren-Lawrence, who were in need of administration of nonsteroidal anti-inflammatory drugs (NSAIDs). The drug Chondrogard was administered intramuscularly each alternate day (a total of 30 injections); 66 (94 %) patients have completed the study. The results showed that the therapeutic effect occurred at the 23th day of treatment on average. Thus, Chondrogard has significant symptomatic effect, reducing pain, stiffness, and improving functional performance. The advantages include the rapid onset of drug effect, potential for the withdrawal or reducing the NSAID dose during treatment, and good tolerability. The drug Chondrogard can be recommended to the OA patients as a first-line drug with a more immediate effect, with subsequent replacement by oral forms of drug.
Key words: osteoarthrosis, nonsteroidal anti-inflammatory drugs, chondroitin sulfate
Фармакокинетика и биологическая активность ХС в значительной степени определяются массой молекулы и степенью сульфатирования [10]. В качестве исходного сырья для получения ХС используется хрящевая ткань крупного рогатого скота, свиней, цыплят или рыб 14. Разные источники получения ХС определяют особенности молекулярной структуры ХС, что в свою очередь помимо степени очистки оказывает влияние на эффективность применения того или иного препарата.
Большая часть ХС выпускается в виде форм для перорального применения. При попадании в ЖКТ происходит разрушение большинства молекул ХС, и в системный кровоток, как правило, попадают низкомолекулярные дериваты, обладающие небольшой терапевтической активностью. По некоторым данным, доля нативных молекул в системном кровотоке при пероральном приеме составляет всего 10 %. Максимальная концентрация препарата в крови достигается через 3-4 часа после приема, а в синовиальной жидкости — через 4-5 часов. В целом же биодоступность ХС при пероральном приеме составляет в среднем от 10 до 20 % 16.
При внутримышечном введении ХС выявляется в значительных концентрациях в системном кровотоке уже через 30 минут, а максимальная концентрация достигается через час. В синовиальной жидкости препарат выявляется через 15 минут после внутримышечной инъекции, а максимальная концентрация в хрящевой ткани достигается через 48 часов [18]. Внутримышечный способ введения ХС увеличивает биодоступность и долю нативных молекул в системном кровотоке, благодаря чему может повышаться как эффективность проводимой терапии, так и более быстрое развитие симптоматического эффекта.
Целью исследования явилась оценка эффективности, переносимости и безопасности ХС (Хондрогарда) для пациентов с ОА коленных суставов при внутримышечном применении.
Материал и методы
В 2-месячное проспективное когортное исследование были включены 70 человек с диагнозом ОА коленных суставов, среди них были 67 (96 %) женщин и 3 (4 %) мужчины. Диагноз остеоартроза устанавливался на основе классификационных критериев Американской коллегии ревматологов (АКР) 1986 г. [5].
В исследование не включали лиц с вторичным гонартрозом, внутрисуставным введением любых препаратов за последние 6 недель до начала исследования, наличием хондрокальциноза, асептического некроза мыщелков бедренных и большеберцовых костей, оперативных вмешательств на коленном суставе, а также с известной повышенной чувствительностью к ХС, тяжелыми сопутствующими заболеваниями, язвой желудка или двенадцатиперстной кишки в течение последнего месяца, кровотечениями в анамнезе, тромбофлебитами, беременностью и периодом лактации, принимавшими препараты с симптоматическими и структурно-модифицирующими свойствами. Разрешалось использование НПВС, которые пациенты принимали на момент включения в исследование. Не допускались внутрисуставные инъекции, в т. ч. глюкокортикоидов и препаратов гиалуроновой кислоты, прием антикоагулянтов, антиагрегантов, фибринолитиков, проведение физиотерапевтических процедур.
Характеристика участников исследования представлена в табл. 1.
Таблица 1
Характеристика участников исследования
| Параметры | Мин. | Макс. | Среднее | SD | ||||
| Возраст, годы | 45 | 70 | 61 | 6,4 | ||||
| Рост, м | 1,5 | 1,77 | 1,63 | 0,06 | ||||
| Масса тела, кг | 54 | 110 | 81,6 | 12,9 | ||||
| ИМТ, кг/м 2 | 22 | 40 | 31 | 4,6 | ||||
| Длительность болезни |
| 1 мл | |
| хондроитина сульфат натрия | 100 мг |
Раствор для в/м и внутрисуставного введения прозрачный, бесцветный или со слегка желтоватым оттенком, с запахом бензилового спирта.
| 1 мл | 1 амп. | |
| хондроитина сульфат натрия | 100 мг | 200 мг |
× пачка с двух сторон с наклейками из самоклеящегося материала для контроля вскрытия или без наклеек.
* шприцы с иглой, с защитным колпачком или без иглы, с защитной пробкой и дополнительным колпачком или без дополнительного колпачка, или с дополнительным колпачком с контролем первого вскрытия.
Шприцы с иглой могут комплектоваться дополнительным автоматическим или неавтоматическим устройством для защиты иглы после использования шприца.
В пачку со шприцами без игл может дополнительно вкладываться комплект из 5 или 10 игл.
Фармакологическое действие
Высокомолекулярный мукополисахарид, влияющий на обменные процессы в гиалиновом хряще. Уменьшает дегенеративные изменения в хрящевой ткани суставов, ускоряет процессы ее восстановления, стимулирует синтез протеогликанов.
При лечении препаратом уменьшается болезненность и улучшается подвижность пораженных суставов. При лечении дегенеративных изменений суставов с развитием вторичного синовита, положительный эффект может наблюдаться уже через 2-3 недели после начала введения препарата: уменьшается боль в суставах, исчезают клинические проявления реактивного синовита, увеличивается объем движений в пораженных суставах. Терапевтический эффект сохраняется длительное время после окончания курса лечения.
Фармакокинетика
После в/м введения Cmax хондроитина сульфата в плазме достигается через 1 ч, затем постепенно снижается в течение 2 сут. При однократном внутрисуставном введении препарата в дозе 200 мг Cmax хондроитина сульфата в плазме наблюдается через 1-2 ч и составляет 52.5-86.9 нг/мл.
После в/м введения хондроитина сульфат быстро распределяется. Уже через 30 мин после инъекции он обнаруживается в крови в значительных концентрациях.
Хондроитина сульфат накапливается, главным образом, в хрящевой ткани суставов. Синовиальная оболочка не является препятствием для проникновения препарата в полость сустава. В экспериментах показано, что через 15 мин после в/м инъекции хондроитина сульфат обнаруживается в синовиальной жидкости, затем проникает в суставной хрящ, где его Cmax достигается через 48 ч.
При внутрисуставном введении наблюдается удерживание хондроитина сульфата в тканях сустава и его постепенный выход в кровоток.
Т1/2 при внутрисуставном введении составляет 2.5 ч.
Показания препарата Хондрогард ®
Дегенеративно-дистрофические заболевания суставов и позвоночника:
Для ускорения формирования костной мозоли при переломах.
Оценка эффективности препарата Хондрогард в терапии остеоартроза при различных режимах введения
*Пятилетний импакт фактор РИНЦ за 2020 г.
Введение
Читайте в новом номере
Остеоартроз (остеоартрит) – гетерогенная группа заболеваний различной этиологии со сходными биологическими, морфологическими и клиническими проявлениями и исходом, в основе которых лежит поражение всех компонентов сустава, в первую очередь хряща, а также субхондрального участка кости, синовиальной оболочки, связок, капсулы, периартикулярных мышц [1]. Основу патогенеза остеоартроза составляют нарушения физиологических процессов деградации и синтеза хондроцитов, внеклеточного матрикса и субхондральной кости [2–4]. Одним из ведущих механизмов патогенеза остеоартроза является дефицит хондроитина сульфата [5, 6]. Европейская антиревматическая лига (EULAR – The European League Against Rheumatism) отдельно выделила группу лекарственных средств, определяемых как препараты замедленного действия для симптоматической терапии остеоартроза (SYSADOA – symptomatic slow acting drugs for osteoarthritis). Хондроитина сульфат является типичным представителем группы лекарственных средств замедленного действия [1, 5, 7].
Оптимальным препаратом для терапии первичного остеоартроза является Хондрогард (хондроитина сульфат для внутримышечного введения в концентрации 100 мг действующего вещества в 1 мл раствора). Хондрогард представляет собой высокомолекулярный мукополисахарид, влияющий на обменные процессы в гиалиновом хряще, препарат уменьшает дегенеративные изменения в хрящевой ткани суставов, ускоряет процессы ее восстановления, стимулирует синтез протеогликанов.
Для оценки эффективности и переносимости препарата Хондрогард на базе ревматологического кабинета ФКУЗ МСЧ МВД РФ по Ульяновской области было проведено открытое клиническое исследование, в которое были включены 60 пациентов (32 женщины и 28 мужчин) с двусторонним первичным гонартрозом (36 пациентов) и двусторонним первичным коксартрозом (24 пациента).
Дизайн исследования соответствовал рекомендациям Европейской антиревматической лиги (EULAR) Outcome Measures in Arthritis Clinical Trials (OMERACT III) и представлял собой рандомизированное двойное слепое контролируемое исследование в параллельных группах с активным контролем. Диагноз «остеоартроз» был установлен в соответствии с критериями ACR 1987 г. [6, 7]. Все пациенты, средний возраст которых составлял 52,36±4,04 года, были разделены на 2 группы (табл. 1). Больные 1-й группы (n=30) получали только Хондрогард в/м в дозе 200 мг ежедневно, на курс 20 инъекций. Больные 2-й группы (n=30) – Хондрогард в/м в дозе 200 мг (на курс 20 инъекций) по интермитирующей схеме (через день); при этом допускалось применение нестероидного противовоспалительного препарата (НПВП) Немулекс по потребности (при интенсивных болях) в суточной дозе не более 200 мг. Соответственно, у пациентов 1-й группы курс терапии составил 20 календарных дней, у пациентов 2-й группы – 40.
У пациентов в обеих группах исследовался суммарный индекс Лекена (индекс тяжести для гонартроза и коксартроза), индекс боли по визуально-аналоговой шкале (ВАШ), терапевтический эффект по мнению пациента и врача, качество жизни (в соответствии с опросником качества жизни SF-36), оценивались побочные эффекты терапии. Клинические показатели определялись до начала терапии и после ее окончания. Критерии включения в исследование: наличие первичного остеоартроза коленных и тазобедренных суставов I–III стадии по Келлгрену-Лоуренсу [8], наличие боли в целевом суставе от 40 мм по ВАШ, индекс Лекена от 4 до 12 баллов, согласие пациента на участие в клиническом исследовании (все пациенты до начала терапии подписали информированное согласие). Критерии исключения из исследования: наличие у пациента помимо первичного остеоартроза воспалительной артропатии или системного заболевания соединительной ткани, предшествующее внутрисуставное введение глюкокортикоидов, физиотерапевтическое лечение в течение предшествующего исследованию месяца.
Статистическая обработка материала проводилась с использованием программ Microsoft Office Excel 2010 и Statistica Base 6.0. Применялись методы описательной статистики, непараметрические методы. Статистическая значимость показателей была определена как р
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Эффективность и безопасность гликозаминогликан-пептидного комплекса в терапии обострений хронической боли при остеоартрите коленных суставов у коморби

В статье представлены результаты наблюдательной комплексной программы, включающей немедикаментозные и медикаментозные методы лечения рецидива хронической боли при остеоартрите у коморбидных пациентов. Наиболее важными компонентами данной программы являетс
The article presents the results of complex observational program which includes drug and non-drug methods of treatment of recurrent chronic pain in osteoarthritis in comorbid patients. The most important components of this program are application of glycosaminoglycan-peptide complex and physical exercises. Special attention is paid to patients with comorbid diseases as the most widespread group of patients disposed to polypharmacy and having contraindications for NSAID administration.
Остеоартрит (ОА) — заболевание суставов, характеризующееся клеточным стрессом и деградацией экстрацеллюлярного матрикса, возникающих при макро- и микроповреждениях. Данная нозология характеризуется такими анатомическими и физиологическими нарушениями, как деградация хряща, ремоделирование кости, образование остеофитов, воспаление и потеря нормальной функции сустава. В современной клинической практике остеоартрит является одним из самых частых компонентов коморбидности. Клинико-эпидемиологические работы последних лет четко обозначили медико-социальное значение проблемы ОА:
Наличие хронической боли является ключевым фактором, увеличивающим число сердечно-сосудистых катастроф. Данные исследования, опубликованные в Европейском журнале сердца [1], свидетельствуют о возрастании числа больших кардиоваскулярных осложнений при наличии ОА:
Именно факт увеличения риска серьезных осложнений сердечно-сосудистых заболеваний и летальности при наличии у пациента клинически манифестированного ОА заставляет взглянуть на данную проблему с точки зрения не столько болезни, изменяющей качество жизни, сколько проблемы, вносящий существенный вклад в увеличение смертности популяции.
Воспаление является ключевым патогенетическим событием как в инициации, так и в прогрессировании коморбидности в целом и ОА в частности. Доказательством тому могут служить данные Роттердамского когортного исследования, демонстрирующие увеличение риска прогрессии ОА (1,3 (1,02–1,6), 0,03) при высоком уровне С-реактивного белка (как маркере интенсивности системного воспаления) и рецидива хронической боли при ОА (1,8 (1,3–2,4), 0,0003) [2].
Медиаторы, запускающие и поддерживающие воспаление в суставе, активно вырабатываются в следующих случаях, требующих обязательной медикаментозной коррекции:
1) избыточная масса тела (клетки жировой ткани продуцируют много провоспалительных и деструктивных медиаторов);
2) нефизиологичная нагрузка на сустав (высокий индекс массы тела, нарушение осей конечностей (деформация ног, халюс вальгус и т. п.), подъем тяжестей, падения, что требует протекции и разгрузки сустава ортезами);
3) гиперхолестеринемия, гипергликемия, артериальная гипертензия, гиперурикемия, гипоксия — состояния, включающие синтез всех возможных медиаторов воспаления и приводящие к деструкции хряща и кости. Вследствие этого лечение боли при ОА возможно лишь в случае целевых значений указанных параметров.
Несомненно, что с повсеместным внедрением возможности эндопротезирования суставов проблема ОА получила революционное решение в случаях неуспешности консервативного лечения. Однако возрастающая потребность в эндопротезировании, явно несоответствующая реальным возможностям системы отечественного здравоохранения, вносит определенный скептицизм в решение проблемы терапии ОА в будущем.
Поэтому в настоящий момент особое внимание клиницистов привлекают рекомендации по консервативному лечению ОА.
С этой точки зрения представляется концептуально правильным предложенный в Клинических рекомендациях РНМОТ [3] порядок врачебных интервенций при ведении больных с ОА и коморбидностью:
В отечественной клинической практике следующая панель аргументов определяет особое место медленнодействующих препаратов в терапии ОА.
Во-первых, это отсутствие достаточной двигательной реабилитации больных, объясняемое крайне низкой приверженностью отечественных пациентов к данной рекомендации. Во-вторых, трудности с назначением центральных анальгетиков. В-третьих, недостаточная доступность эндопротезирования. И, наконец, мнение ведущих лидеров и главных специалистов РФ, оценивающих данную терапию достаточно эффективной интервенцией в терапии боли при ОА.
Существенным событием, ознаменовавшим надежный уровень доказательности хондроитина, было появление в 2015 г. систематического Кохрановского обзора [4]. Эксперты заключили, что хондроитин сульфат (ХС) превосходил плацебо по влиянию на боль в суставах при ОА.
Однако остается открытым вопрос в скорости наступления обезболивающего эффекта. Не секрет, что пероральные формы ХС подвергаются существенной деградации кишечной микробиотой [5]. На основании перорального применения шести различных субстанций ХС показано, что до 76% изначальной дозы ХС обнаруживается в виде деградированных осколков хондроитина в фекалиях пациентов в течение 72 ч. Этот факт отчасти объясняет использование больших доз ХС в таблетированных формах и медленное наступление клинического эффекта.
Следовательно, можно предположить, что парентеральное введение ХС может повлиять на скорость наступления анальгетического эффекта и на размер клинического эффекта.
В отечественной практике особый интерес представляет гликозаминогликан-пептидный комплекс (ГПК) — Румалон, содержащий хондроитин-4-сульфат (64,5%), хондроитин-6-сульфат (16,5%), хондроитин (9,5%), дерматан-сульфат (3,4%), гиалуроновую кислоту (2,1%), кератан-сульфат (4,0%) и пептиды.
Механизм действия ГПК (Румалон) обусловлен наличием высокой концентрации ХС, оказывающего тормозящее действие на синтез провоспалительных медиаторов в тканях сустава, путем снижения активации рецептора к ИЛ-1 и нарушения транслокации ядерного фактора транскрипции kВ [6]. Дерматан- и кератан-сульфат, в совокупности с гиалуроновой кислотой, обеспечивают метаболическую активность клеточных структур сустава и структурирование матрикса хряща. К тому же гиалуроновая кислота, посредством взаимодействия с рецепторами CD-44, увеличивает синтез собственных нитей гиалуроната, служащих структурной единицей протеогликанов хряща.
Румалон хорошо известен врачам на протяжении последних десятилетий, поскольку был первым препаратом, относящимся к группе хондропротекторов, на территории Европы, а впоследствии СССР и стран СНГ. Имеется ряд клинических исследований, выполненных с учетом требований «доказательной медицины» (РКИ), показавших хороший размер клинического эффекта ГПК [7]. Определенный интерес представляет недавно опубликованное исследование ПРИМУЛА [8], данные которого подтверждают хорошее лечебное действие и благоприятную переносимость ГПК (Румалон). В ходе исследования были продемонстрированы быстрый анальгетический и противовоспалительный эффект этого препарата, его позитивное влияние на все клинические проявления ОА. Применение инъекционной формы ГПК имеет свои преимущества: пациенты субъективно рассматривают такое лечение как «более активное», лечащему врачу проще отслеживать соблюдение назначений и оценивать результаты терапии, чем при использовании пероральных средств. Авторы рекомендуют ГПК при тяжелом, прогрессирующем течении ОА, в том числе в тех случаях, когда предыдущая комплексная терапия не дала позитивного результата.
Однако результаты исследования ПРИМУЛА не дают ответа на вопрос, насколько парентеральная форма ГПК способна безопасно купировать болевой синдром в коленных суставах у коморбидных пациентов, и насколько проведенный инъекционный курс терапии позволяет пролонгировать безболевые периоды у данной категории больных, что и послужило целью нашего наблюдения.
Для оценки эффективности и безопасности применения ГПК (Румалон) у коморбидных больных с обострением хронической боли при ОА коленных суставов была спланирована открытая, наблюдательная программа ДАРТС (эффективность и безопасность гликозаминогликан-пептиДного комплекса в терапии остеоАРТрита коленных Суставов у коморбидных больных). Кроме того, программа ДАРТС включала: контролируемую в рамках программы физическую активность (контроль и выполнение с инструкторами ЛФК в сроки инъекционного курса ГПК с последующим контролем ежедневного выполнения специально разработанного комплекса ЛФК и достаточного уровня ходьбы); контроль и компенсация компонентов коморбидности больных.
Целью данной программы было оценить эффективность, сроки наступления эффективного обезболивания и безопасность применения гликозаминогликан-пептидного комплекса (Румалон) у коморбидных пациентов с ОА коленных суставов.
Материалы и методы исследования
Был проведен скрининг 82 пациентов с хронической болью в коленных суставах и коморбидными состояниями. Отобрано 50 пациентов, отвечающих критериям включения и исключения.
Критерии включения:
Критерии исключения:
* ФГБОУ ВО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
** ФГБОУ ВО МГМСУ им. А. И. Евдокимова МЗ РФ, Москва
Эффективность и безопасность гликозаминогликан-пептидного комплекса в терапии обострений хронической боли при остеоартрите коленных суставов у коморбидных больных (результаты наблюдательной программы «ДАРТС»)/ А. В. Наумов, О. Н. Ткачева, Ю. В. Котовская, Н. О. Ховасова
Для цитирования: Лечащий врач № 7/2018; Номера страниц в выпуске: 31-37
Теги: коленные суставы, воспаление, рецидив, сердечно-сосудистые заболевания