Хлорид бария
| Хлорид бария | |
|---|---|
 | |
| Систематическое наименование | Хлорид бария |
| Традиционные названия | Хлористый барий |
| Хим. формула | BaCl2 |
| Рац. формула | BaCl2 |
| Состояние | твёрдое |
| Молярная масса | 208,246 г/моль |
| Плотность | 3,92 (20 °C) |
| Температура | |
| • плавления | 962 °C |
| • кипения | 1560 °C |
| Энтальпия | |
| • образования | -860,1 кДж/моль |
| Растворимость | |
| • в воде | 36,2 (20 °C) |
| ГОСТ | ГОСТ 4108-72 ГОСТ 742-78 |
| Рег. номер CAS | 10361-37-2 |
| PubChem | 25204 |
| Рег. номер EINECS | 233-788-1 |
| SMILES | |
| RTECS | CQ8750000 |
| ChEBI | 63317 |
| Номер ООН | 1564 |
| ChemSpider | 23540 |
| ЛД50 | 50-78 мг/кг (крысы, орально) |
| Пиктограммы ECB |   |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
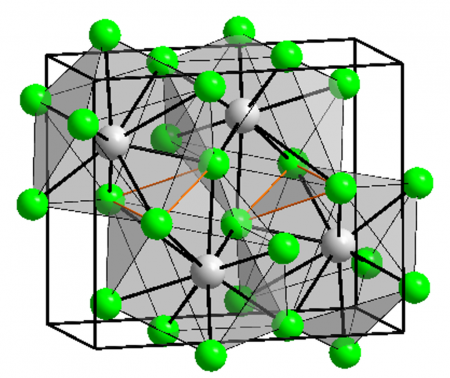
Хлорид бария (хлористый барий) — бинарное неорганическое вещество, относящееся к классу солей. Химическая формула — BaCl2.
Содержание
Описание
Хлорид бария при стандартных условиях представляет собой бесцветные ромбические кристаллы. Малорастворим в спирте, не растворим в диэтиловом эфире. Из водных растворов кристаллизуется дигидрат хлорида бария BaCl2 ⋅ 2H2O — бесцветные кристаллы с моноклинной решёткой. Токсичен, ПДК 0,5 мг/м³
ГОСТ 4108-72 Реактивы. Барий хлорид 2-водный. Технические условия
Получение
1. Взаимодействие металлического бария с хлором:
2. Взаимодействие оксида бария с соляной кислотой:
3. Взаимодействие гидроксида бария с соляной кислотой (реакция нейтрализации):
4. Взаимодействие сульфида бария с хлоридом кальция:
5. Взаимодействие карбоната бария с соляной кислотой:
Химические свойства
1. Взаимодействие с растворами солей (реакция идёт, если образуется нерастворимое вещество):
2. Взаимодействие с некоторыми кислотами (реакция идёт, если образуется нерастворимое вещество):
Применение
Хлорид бария: способы получения и химические свойства
Хлорид бария BaCl2 — соль щелочноземельного металла бария и хлороводородной кислоты. Белый, плавится без разложения. Хорошо растворяется в воде (гидролиза нет).
Относительная молекулярная масса Mr = 208,23; относительная плотность для тв. и ж. состояния d = 3,856; tпл = 961º C;
Способ получения
1. Хлорид бария можно получить путем взаимодействия бария и хлора :
2. В результате взаимодействия карбоната бария и разбавленной соляной кислоты образуется хлорид бария, углекислый газ и вода:
3. Гидроксид бария вступает в реакцию с соляной кислотой с образованием хлорида бария и воды:
Качественная реакция
Качественная реакция на хлорид бария — взаимодействие его с нитратом серебра, в результате реакции происходит образование белого творожного осадка:
Химические свойства
1. Хлорид бария вступает в реакцию со многими сложными веществами :
1.1. Хлорид бария реагирует с кислотами:
1.1.1. Твердый хлорид бария реагирует с концентрированной серной кислотой при кипении , образуя сульфат бария и газ хлороводород :
1.2. Хлорид бария вступает в взаимодействие с солями:
1.2.1. В результате реакции между хлоридом бария и концентрированным раствором карбоната натрия образуется карбонат бария и хлорид натрия:
1.2.2. Хлорид бария может реагировать с сульфатом натрия при 800º С с образованием сульфата бария и хлорида натрия:
2. В результате электролиза раствора хлорида бария образуется водород и хлор:
Хлорид бария
| Хлорид бария | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Хлорид бария |
| Традиционные названия | Хлористый барий |
| Химическая формула | BaCl2 |
| Эмпирическая формула | BaCl2 |
| Физические свойства | |
| Состояние (ст. усл.) | твёрдое |
| Молярная масса | 208,246 г/моль |
| Плотность | 3,92 (20 °C) г/см³ |
| Термические свойства | |
| Температура плавления | 962 °C |
| Температура кипения | 1560 °C |
| Энтальпия образования (ст. усл.) | -860,1 кДж/моль |
| Химические свойства | |
| Растворимость в воде | 36,2 (20 °C) [1] г/100 мл |
| Классификация | |
| Рег. номер CAS | 10361-37-2 |
Содержание
Описание
Получение
1. Взаимодействие металлического бария с хлором:
Химические свойства
1. Взаимодействие с растворами солей (реакция идёт, если образуется нерастворимое вещество):
2. Взаимодействие с некоторыми кислотами (реакция идёт, если образуется нерастворимое вещество):
Применение
См. также
Примечания
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | Н | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
Полезное
Смотреть что такое «Хлорид бария» в других словарях:
хлорид бария — хлористый барий … Cловарь химических синонимов I
Хлорид цезия — Хлорид цезия … Википедия
Хлорид вольфрама(VI) — Общие … Википедия
Хлорид титана(IV) — Хлорид титана(IV) … Википедия
Хлорид вольфрама(II) — Общие Систематическое наименование Хлорид вольфрама(II) Традиционные названия Хлористый вольфрам; гексамер дихлорида вольфрама Химическая формула WCl2 Физические свойства … Википедия
Хлорид вольфрама(IV) — Общие Систематическое наименование Хлорид вольфрама(IV) Традиционные названия хлористый вольфрам Химическая формула WCl4 Физические свойства Сос … Википедия
Хлорид вольфрама(V) — Общие Систематическое наименование Хлорид вольфрама(V) Традиционные названия Хлористый вольфрам Химическая формула WCl5 Физические свойства Состо … Википедия
Хлорид молибдена(II) — Общие Систематическое наименование Хлорид молибдена(II) Традиционные названия Хлористый молибден; гексамер дихлорида молибдена Химическая формула MoCl2 Физические свойства … Википедия
Хлорид молибдена(III) — Общие Систематическое наименование Хлорид молибдена(III) Традиционные названия Хлористый молибден Химическая формула MoCl3 Физические свойства … Википедия
Хлорид молибдена(IV) — Общие Систематическое наименование Хлорид молибдена(IV) Традиционные названия Хлористый молибден Химическая формула MoCl4 Физические свойства Со … Википедия
Хлорид бария — соль, широко использующаяся в промышленности и аналитике
Барий хлористый — неорганическое вещество, которое 
Тонкозернистый порошок белого или сероватого цвета с мелкими бесцветными кристалликами. Водорастворим, слабо растворим в спирте и спиртовых растворах, не растворим в эфирах. Из водных растворов выкристаллизовываются бесцветные кристаллогидраты с одной или двумя молекулами воды. Реактив огне- и взрывобезопасен. Проявляет диамагнитные свойства.
Химически достаточно активная соль. Реагирует с другими солями в водных растворах, если в результате получается нерастворимое соединение, выпадающее в осадок. Это свойство используется в аналитике для обнаружения сульфат-ионов. Хим. реактив способен образовывать двойные соли, эвтектические смеси, а с бромидом бария — твердые растворы.
 |  |  |
| Барий азотнокислый Имп. | Барий хлористый | Барий сернокислый |
Барий хлористый безводный и его кристаллогидраты крайне токсичны. Отравление приводит к необратимым последствиям для головного мозга и серьезному поражению почек, селезенки, желудочного тракта, параличу и потере зрения. Попадание реактива с пылью оказывает негативное воздействие на органы дыхания. Опасно также попадание пыли или раствора в глаза или на кожу.
При проглатывании следует сразу же вызвать врача и промыть желудок 1%-ным раствором сернокислого натрия или магния. Если порошкообразный реактив рассыпан, его нельзя заливать водой. Его следует изолировать, засыпать песком и потом утилизировать.
Работать с хлористым барием следует в спец. одежде, респираторе, резиновых перчатках и защитных очках. Помещение должно быть оборудовано вентиляцией, а места возможного сильного запыления — локальным укрытием и дополнительной местной вентиляцией. В лабораториях для работы с хлоридом бария используют вытяжной шкаф.
Хранят реактив в полиэтиленовых мешках, в сухом помещении, строго следят за тем, чтобы он не контактировал с водой. Перевозят любым крытым транспортом, кроме самолета.
При нагревании BaCl2 разлагается с выделением химически активного хлороводорода, поэтому пожарные должны быть извещены, если в зоне пожара оказались значительные количества реактива.
Хлорид бария
Характеристики и физические свойства хлорида бария
Он хорошо растворяется в воде, при этом не подвергаясь гидролизу, так как образован сильной кислотой и сильным основанием.
Рис. 1. Хлорид бария. Внешний вид.
Основные характеристики хлорида бария приведены в таблице ниже:
Молярная масса, г/моль
Температура плавления, o С
Температура разложения, o С
Растворимость в воде (20 o С), г/100 мл
Получение хлорида бария
В лабораторной практике для получения хлорида бария используют следующие реакции:
Химические свойства хлорида бария
В водном растворе хлорид бария диссоциирует на ионы:
Он хорошо растворяется в концентрированной азотной кислоте и разлагается серной, но нерастворим в концентрированной хлороводородной кислоте.
Хлорид бария вступает в реакции обмена с другими солями только в случае образования в качестве продуктов нерастворимого вещества, газообразного или малодиссоциирующего соединения:
Применение хлорида бария
Хлорид бария используют в кожевенном деле, при производстве керамических изделий, пигментов, а также в химическом анализе, как качественный реактив для обнаружения сульфат-анионов.
Примеры решения задач
| Задание | Вычислите массу хлорида бария, который может прореагировать с концентрированным раствором серной кислоты объемом 100 мл (массовая доля H2SO4 98%, плотность 1,8365 г/мл). Определите объем хлороводорода, выделяющийся в результате этой реакции. |
| Решение | Запишем уравнение реакции: |
Найдем массу раствора серной кислоты, а также массу растворенного вещества H2SO4 в нем:
msolution =100 × 1,8365 = 183,65г.
Рассчитаем количество моль серной кислоты (молярная масса равна 98 г/моль):
Согласно уравнению реакции n (H2SO4) :n (HCl) = 1: 2. Значит,
n(HCl) = 2 × n(H2SO4) = 2 × 1,84 = 3,86 моль.
Тогда, объем выделившегося хлороводорода будет равен:
V (HCl) = 3,86 × 22,4 = 82,432 л.
Согласно уравнению реакции n(H2SO4) :n (BaCl2) = 1: 1. Значит,количество вещества карбоната хлорида бария равно:
Тогда масса хлорида бария, вступившего в реакцию будет равна (молярная масса – 208 г/моль):
m (BaCl2) = 1,84 × 208 = 382,72г.
| Задание | Вычислите массу бария, который необходим для получения хлорида бария массой 7,9 г по реакции взаимодействия с хлором. |
| Решение | Запишем уравнение реакции взаимодействия бария и хлора с образованием хлорида бария: |
Рассчитаем число моль хлорида бария (молярная масса – 208 г/моль):
n (BaCl2) = 7,9 / 208 = 0,04моль.
Согласно уравнению реакции n(BaCl2) :n(Ba) = 1:1, значит,
Масса бария необходимого для получения хлорида бария по реакции взаимодействия с хлоромравна (молярная масса – 137 г/моль):














