Бактериофаги
БАКТЕРИОФАГИ КАК АЛЬТЕРНАТИВА АНТИБИОТИКАМ В ЛЕЧЕНИИ ИНФЕКЦИЙ
Бактериофаги — вирусы бактерий, естественные микроорганизмы, которые, размножаясь внутри бактериальной клетки, ведут к ее быстрой гибели.
Из истории открытия
В 1896 году английский бактериолог Э. Ханкин, исследуя антибактериальное действие воды индийских рек, пришел к выводу о существовании агента, проходящего через бактериальные фильтры и вызывающего лизис холерных вибрионов. Российский микробиолог Н. Ф. Гамалея в 1897 году наблюдал лизис бацилл сибирской язвы. Однако первой научной публикацией о фагах стала статья английского микробиолога Ф. Туорта, в которой он в 1915 году описал инфекционное поражение стафилококков, значительно изменявшее морфологию колоний. В 1917 году канадский бактериолог Ф. Д’Эрелль независимо от Туорта сообщил об открытии вируса, «пожирающего» бактерии — бактериофага.
Интересный факт: при нанесении бактериофага на влажные слизистые он за 20 минут очищает их от определенного вида бактерий, например от стафилококка. Так быстро не работает ни один антибиотик.
Действие бактериофагов отличается от действия антибиотиков:
В лаборатории KDL предлагается 2 варианта посевов на флору с определением чувствительности выделенной культуры микроорганизма к препаратам бактериофагов и разным наборам антибиотиков в зависимости от ситуации пациента (выбирает врач), например:
Какие инфекции можно лечить бактериофагами:
Возбудителями этих инфекций могут быть такие бактерии, как золотистый стафилококк, синегнойная палочка, патогенные формы кишечной палочки, сальмонеллы, стрептококки.
В Новосибирском научном центре технологии персонализированного лечения бактериофагами в большой коллекции бактериофагов есть уникальные штаммы, способные бороться с недавно появившимися и уже получившими широкое распространение возбудителями больничных инфекций, такими как грамотрицательные бактерии Acinetobacter baumanii, Stenotrophomonas maltophilia и др.
Последние годы ознаменовались широкими исследованиями бактериофагов из-за нарастающей проблемы антибиотикорезистентности микроорганизмов, которые находят всё новые применения не только в терапии и профилактике, но и в биотехнологиях. Их очевидным практическим результатом должно стать возникновение нового мощного направления персонализированной медицины, а также создание целого спектра технологий в пищевой промышленности, ветеринарии, сельском хозяйстве и в производстве современных материалов. Мы ждем, что второе столетие исследований бактериофагов принесет не меньше открытий, чем первое.
Журнал для профессионалов аптечного бизнеса
Регистрация
Вирусы против бактерий
Бактериофаги – одни из самых загадочных препаратов аптечного ассортимента. Сейчас они переживают второе рождение – и в нашей стране, и за рубежом снова возник к ним интерес, в журналах появляется не только пересмотр старых результатов, но и масса новых публикаций. Что можно рассказать покупателю, который заинтересовался именно этими средствами?
Вехи истории
Ученые обнаруживали следы жизнедеятельности бактериофагов задолго до того, как возникла вирусология. Британский бактериолог Эрнест Ханкин еще в 1896 году обратил внимание, что некий агент, способный проходить через очень тонкий фарфоровый фильтр, убивает возбудителя холеры. Развитию науки в новом направлении помешала Первая мировая, поскольку финансирование было перенаправлено разработчикам боевых газов, взрывчатых веществ и других более актуальных вещей.
Первооткрывателями бактериофагов считаются два исследователя – британский бактериолог Фредерик Творт, описавший странный фильтрующийся агент в 1915 году, и канадский микробиолог французского происхождения Феликс Д’Эрелль, независимо от Творта сообщивший о точно такой же находке в 1917-м.
За рубежом бактериофагами интересовались в первую очередь микробиологи, так что их находки не имели прикладного значения. Очень долгое время, например, фаг считался не вирусом, а ферментом. В СССР работы изначально велись медиками, в Грузии в 1923 году был создан будущий Всесоюзный центр фаготерапии, собравший на пике своего расцвета коллекцию из более чем 3 тыс. образцов. Однако затем и у нас, и за рубежом дело фаготерапии было практически уничтожено появившимися антибиотиками. Их массовое распространение после Второй мировой создавало впечатление, что изобретена панацея против инфекций и остальные направления исследований – тупиковые.
О бактериофагах ученые вспомнили, когда перед ними в полный рост встала проблема антибиотикорезистентности. Вирусы снова стали объектом экспериментов, в них увидели реальную альтернативу морально и иногда даже физически устаревшим противомикробным препаратам.
Натуральный враг
Бактериофаг, как следует хотя бы из названия, – вирус, пожирающий бактерии. По сути, это такой «грипп бактерий», только летальные исходы случаются куда чаще, чем в человеческом варианте.
Фаги гораздо разнообразнее, чем какие-либо другие известные вирусы, нельзя сказать, что они выглядят однотипно. Чаще всего в качестве иллюстрации используется изображение вирусов группы А по классификации Бредли, она же – группа V по классификации Тихоненко. Такие вирусы устроены сложнее всего, в них имеется головка и отросток с множеством дополнительных элементов (рис. 1). Всего групп выделяют шесть, только в одной из них геном фага представлен одноцепочечной РНК, во всех остальных случаях – это одна- или двухцепочечная ДНК.
Бактериофаги нельзя назвать гигантами, но по своим размерам они, скорее, относятся к крупным и занимают промежуточное положение между самыми большими вирусами табачной мозаики и вирусом иммунодефицита человека 1-го типа (рис. 2).
Вирусы группы А (V) вводят свою ДНК в клетку-мишень очень красиво, процесс чем-то напоминает посадку исследовательского модуля на поверхность Луны или Марса – точно так же он сначала «присаживается» на «опоры», а затем прижимается к мембране бактерии своей базальной пластиной, «пробуравливает» оболочку жертвы и впрыскивает в цитоплазму свой геном. После этого бактериофаг можно считать мертвым, если так вообще можно сказать о вирусах.
Быстро или помучиться?
По механизму действия все бактериофаги можно разделить на две большие группы. Первая – литические, или вирулентные фаги, которые в 100% случаев убивают инфицированную клетку сразу. В случае, показанном на рисунке 3, вирус сразу же уничтожает геном бактерии, используя его исключительно для целей собственной репликации. После наработки максимально возможного числа новых вирусных частиц микроб либо сразу гибнет в момент их выхода, просто разрываясь на части, либо погибает в ближайшее время из-за того, что все критически важные внутренние механизмы физически уничтожены.
Вторая группа – лизогенные, или умеренные фаги. Их геном встраивается в геном носителя и может существовать там в стелс-режиме долгое время, передаваясь из поколения в поколение. Активируется эта «бомба с замедленным действием» под влиянием различных неблагоприятных внешних факторов вроде дефицита питательных веществ. Единичные фаги умеют сочетать оба варианта, отпочковываясь и не разрушая бактериальную клетку сразу, лишь используя часть ее мембраны в качестве оболочки, одновременно оставляя «закладку» в ее геноме. На одного микроба могут напасть сразу несколько фагов с разными механизмами взаимодействия.
Плюсы и минусы
По той же причине у фагов либо меньше побочных эффектов, либо их совсем нет. С резистентностью история схожая, она если и развивается, то только у конкретной бактерии-мишени. С помощью генной инженерии реально перепрограммировать вирус и натравить его на какого-нибудь другого возбудителя, еще не знакомого с вирусом.
Немаловажным фактором в пользу бактериофагов можно считать дешевизну и простоту их производства, особенно по сравнению с новыми перспективными антибиотиками. Действительно получается не менее, а иногда и более эффективная альтернатива с кратно меньшими вложениями.
Недостатки тоже есть, и они тесно связаны с вирусной природой фагов. Прежде всего, их сложно хранить и перевозить, они весьма требовательны к условиям содержания. Кроме того, фаги способны нападать только на свободно плавающие бактерии, внутрь человеческих клеток их никто не пустит. Агрессивная среда желудка уничтожает многие вирусы, не разбирая, кто пришел с миром, а кто нет. И главное, для достижения максимального эффекта терапии бактерию-возбудителя нужно фаготипировать, то есть выделить и в лабораторных условиях доказать, что против нее может быть применен вот этот конкретный вирус.
Факты
В СССР активно изучали медицинское применение бактериофагов, но публикации были либо на русском, либо на грузинском языках, поэтому мировая наука о них не знала и с удивлением изучает и цитирует их уже в наше время.
Работы по бактериофагам удостоены Нобелевской премии. В 1969 году она была присуждена американским исследователям Максу Дельбрюку, Альфреду Херши и Сальвадору Лурия за открытия, касающиеся механизма репликации и генетической структуры вирусов.
В ГРЛС зарегистрированы и обращаются на российском рынке следующие разновидности бактериофагов: брюшнотифозный, дизентерийный, против клебсиелл и отдельно – против клебсиеллы пневмонии, против кишечной палочки, протейный, сальмонеллезный, стафилококковый и против синегнойной палочки. Самый часто используемый в амбулаторной практике препарат – стафилококковый фаг.
Вирусы и бактерии – великое противостояние
Создание современной технологии геномного редактирования, которая уже с успехом применяется на разных животных, растениях, грибах и бактериях, базируется на исследованиях бактериальных систем CRISPR-Cas. Изначально предполагалось, что они участвуют в ликвидации повреждений бактериальной ДНК, но в 2007 г. стало ясно, что истинное предназначение этих систем – борьба с вирусами бактерий, бактериофагами. Всего за девять лет наука проделала гигантский путь от раскрытия механизма бактериального иммунитета до редактирования геномов людей – в настоящее время уже проводятся первые эксперименты по редактированию ДНК человеческих эмбрионов. У бактерий имеются и другие «иммунные» механизмы, изучение которых, возможно, создаст предпосылки для новых прорывов в биомедицине
Бактериофаги – это вирусы, которые поражают только бактерий. В ходе инфекции они влияют на все процессы жизнедеятельности бактериальной клетки, фактически превращая ее в фабрику по производству вирусного потомства. В конце концов клетка разрушается, а вновь образованные вирусные частицы выходят наружу и могут заражать новые бактерии.
Несмотря на огромное число и разнообразие природных фагов, встречаемся мы с ними редко. Однако бывают ситуации, когда деятельность этих вирусов не остается незамеченной. Например, на предприятиях, где производят сыры, йогурты и другие молочно-кислые продукты, часто приходится сталкиваться с вирусной атакой на бактерии, сбраживающие молоко. В большинстве таких случаев фаговая инфекция распространяется молниеносно, и полезные бактерии гибнут, что приводит к значительным экономическим потерям (Neve et al., 1994).
Именно благодаря прикладным исследованиям в интересах молочной промышленности, направленным на получение устойчивых к бактериофагам штаммов молочно-кислых бактерий, был открыт ряд механизмов, с помощью которых бактерии избегают инфекции. Параллельно были изучены способы, с помощью которых вирусы, в свою очередь, преодолевают бактериальные системы защиты (Moineau et al., 1993).
Кто защищен – тот вооружен
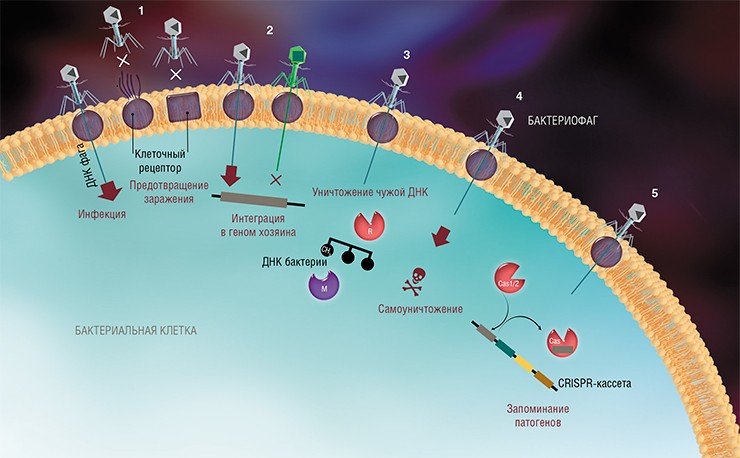
На сегодня известно пять основных, весьма хитроумных механизмов защиты, которые бактерии выработали в непрестанной борьбе с вирусами: изменение рецептора на поверхности клетки; исключение суперинфекции; системы абортивной инфекции; системы рестрикции-модификации и, наконец, системы CRISPR-Cas.
В ходе эволюции происходила и сейчас происходит селекция бактерий, способных избежать гибели при инфицировании вирусами, что, в свою очередь, служит стимулом для бактериофагов совершенствовать свои агрессивные стратегии. Эта «гонка вооружений», длящаяся несколько миллиардов лет, т. е. ровно столько, сколько существуют сами бактерии и их враги, породила целый ряд изощренных механизмов защиты и нападения
Вирусная атака начинается с прикрепления фага к специфическому рецептору на поверхности бактериальной клетки, но при потере рецептора или изменении в его структуре связывания вируса не происходит. Бактерии могут менять рецепторы в зависимости от окружающих условий, таких как плотность и разнообразие микроорганизмов в среде, а также доступность питательных веществ (Bikard et al., 2012). Любопытный пример — бактерии вида Vibrio anguillarum, которые способны формировать биопленку, т. е. плотный слой клеток, прикрепленный к какой-либо поверхности. У этой бактерии имеется своего рода «чувство кворума», за счет чего при увеличении плотности клеток у них понижается выработка рецептора, с которым может связываться вирус. В результате биопленка становится почти полностью устойчивой к заражению (Tan et al., 2015).
Однако потеря рецепторов не всегда выгодна для бактерии, поскольку они выполняют разнообразные важные функции, например, транспорт питательных веществ или формирование межклеточных контактов (Lopez-Pascua et al., 2008). В результате для каждой пары «бактерия-бактериофаг» в ходе эволюции находится оптимальное решение, обеспечивающее приемлемый уровень защиты при сохранении возможности роста бактерий в различных условиях среды.
Следующий защитный механизм – исключение суперинфекции. Для бактериофагов известны два основных пути инфекции: литический, приводящий к быстрой гибели зараженной бактерии с высвобождением вирусного потомства, и затяжной лизогенный путь, когда наследственный материал вируса находится внутри генома бактерии, удваивается только с хозяйской ДНК, не причиняя клетке вреда. Когда клетка находится в состоянии лизогенной инфекции, то, с точки зрения «домашнего» вируса (профага), ее заражение другим вирусом нежелательно.
Действительно, многие вирусы, встроившие свою ДНК в геном клетки, ограничивают вновь проникшего в клетку бактериофага («суперинфекцию») посредством специальных белков-репрессоров, не позволяющих генам «пришельца» работать (Calendar, 2006). А некоторые фаги даже препятствуют другим вирусным частицам проникнуть в инфицированную ими клетку, воздействуя на ее рецепторы. В результате бактерии – носительницы вируса имеют очевидное преимущество по сравнению с незараженными собратьями.
В 1978 г. за открытие ферментов рестриктаз швейцарский генетик В. Арбер и американские микробиологи Д. Натанс и Г. Смит были удостоены Нобелевской премии. Изучение систем рестрикции-модификации привело к созданию технологии молекулярного клонирования, которая широко применяется во всем мире. С помощью рестриктаз можно «вырезать» гены из генома одного организма и вставить в геном другого, получив химерную рекомбинантную ДНК, не существующую в природе. Различные вариации этого подхода используются учеными для изолирования отдельных генов и их дальнейшего изучения. Кроме того, он широко применяется в фармацевтике, например, для наработки инсулина или терапевтических антител: все лекарства такого рода созданы с помощью молекулярного клонирования, т. е. являются продуктом генной модификации
Во время инфекции все ресурсы бактериальной клетки направлены на производство новых вирусных частиц. Если рядом с такой клеткой будут находиться другие уязвимые бактерии, то инфекция быстро распространится и приведет к гибели большинства из них. Однако для таких случаев у бактерии имеются так называемые системы абортивной инфекции, которые приводят ее к запрограммированной гибели. Конечно, этот «альтруистичный» механизм не спасет саму зараженную клетку, но остановит распространение вирусной инфекции, что выгодно для всей популяции. Бактериальные системы абортивной инфекции очень разнообразны, но детали их функционирования пока изучены недостаточно.
К средствам противовирусной защиты бактерий относятся и системы рестрикции-модификации, в которые входят гены, кодирующие два белка-фермента – рестриктазу и метилазу. Рестриктаза узнает определенные последовательности ДНК длиной 4—6 нуклеотидов и вносит в них двуцепочечные разрывы. Метилаза, напротив, ковалентно модифицирует эти последовательности, добавляя к отдельным нуклеотидным основаниям метильные группы, что предотвращает их узнавание рестриктазой.
В ДНК бактерии, содержащей такую систему, все сайты модифицированы. И если бактерия заражается вирусом, ДНК которого не содержит подобной модификации, рестриктаза защитит от инфекции, разрушив вирусную ДНК. Многие вирусы «борются» с системами рестрикции-модификации, не используя в своих геномах последовательности, узнаваемые рестриктазой, – очевидно, что вирусные варианты с другой стратегией просто не оставили потомства.
Последней и в настоящее время самой интересной системой бактериального иммунитета является система CRISPR-Cas, с помощью которой бактерии способны «записывать» в собственный геном и передавать потомству информацию о фагах, с которыми они сталкивались в течение жизни. Наличие таких «воспоминаний» позволяет распознавать ДНК фага и эффективней противостоять ему при повторных инфекциях. В настоящее время к системам CRISPR-Cas приковано пристальное внимание, так как они стали основой революционной технологии редактирования геномов, которая в будущем, возможно, позволит лечить генетические заболевания и создавать новые породы и сорта сельскохозяйственных животных и растений.
Врага нужно знать в лицо
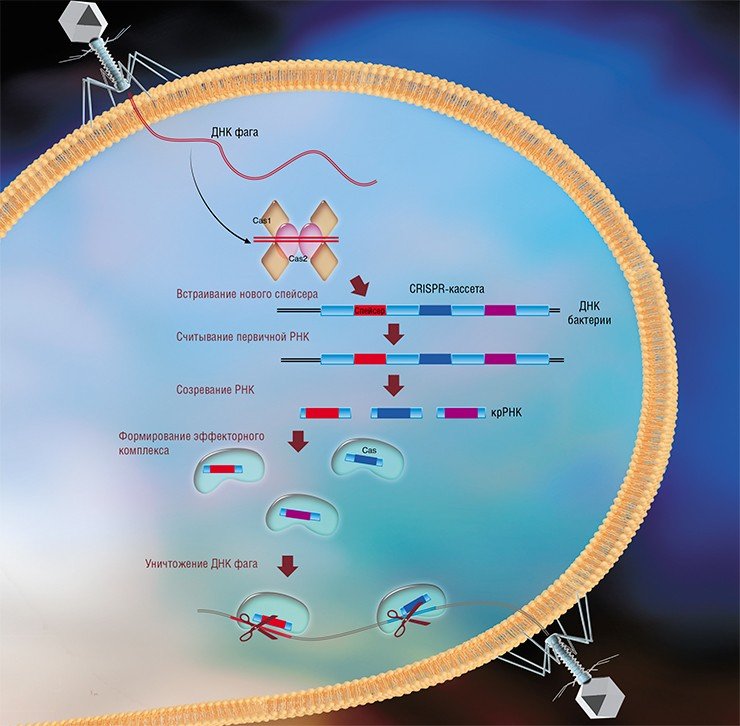
Системы CRISPR-Cas являются уникальным примером адаптивного иммунитета бактерий. При проникновении в клетку ДНК фага специальные белки Cas встраивают фрагменты вирусной ДНК длиной 25—40 нуклеотидов в определенный участок генома бактерии (Barrangou et al., 2007). Такие фрагменты называются спейсерами (от англ. spacer – промежуток), участок, где происходит встраивание, – CRISPR-кассета (от англ. Clustered Regularly Interspaced Short Palindromic Repeats), а сам процесс приобретения спейсеров – адаптацией.
Чтобы использовать спейсеры в борьбе с фаговой инфекцией, в клетке должен происходить еще один процесс, управляемый белками Cas, названный интерференцией. Суть его в том, что в ходе транскрипции CRISPR-кассеты образуется длинная молекула РНК, которая разрезается белками Cas на короткие фрагменты – защитные криспрРНК (крРНК), каждая из которых содержит один спейсер. Белки Cas вместе с молекулой крРНК образуют эффекторный комплекс, который сканирует всю ДНК клетки на наличие последовательностей, идентичных спейсеру (протоспейсеров). Найденные протоспейсеры расщепляются белками Cas (Westra et al., 2012; Jinek et al., 2012).
Системы CRISPR-Cas обнаружены у большинства прокариот – бактерий и архей. Хотя общий принцип действия всех известных систем CRISPR-Cas одинаков, механизмы их работы могут существенно отличаться в деталях. Наибольшие различия проявляются в строении и функционировании эффекторного комплекса, в связи с чем системы CRISPR-Cas делят на несколько типов. На сегодняшний день описаны шесть типов таких неродственных друг другу систем (Makarova et al., 2015; Shmakov et al., 2015).
Наиболее изученной является система CRISPR-Cas I типа, которой обладает излюбленный объект молекулярно-биологических исследований – бактерия кишечная палочка (Esсherichia coli). Эффекторный комплекс в этой системе состоит из нескольких небольших белков Cas, каждый из которых отвечает за разные функции: разрезание длинной некодирующей CRISPR РНК, связывание коротких крРНК, поиск, а затем разрезание ДНК-мишени.
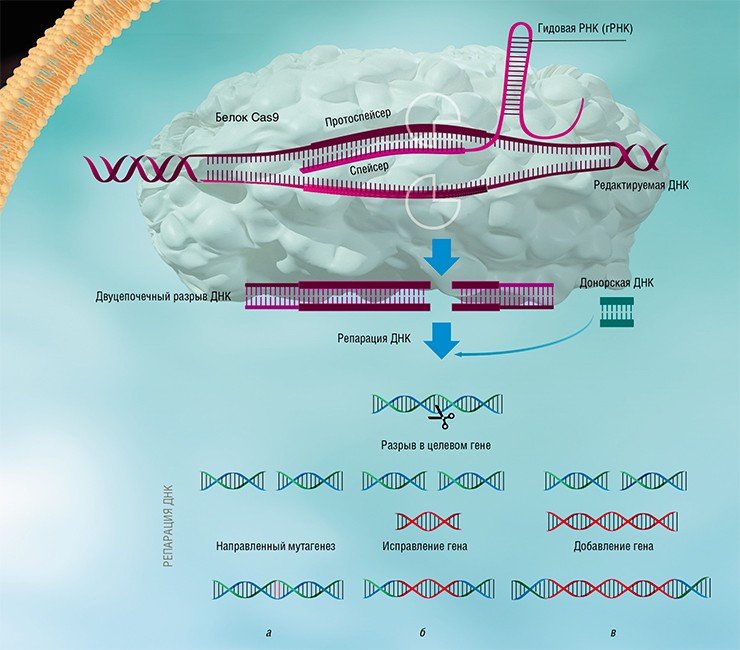
В системах II типа эффекторный комплекс образован единственным большим белком Cas9, который в одиночку справляется со всеми задачами. Именно простота и относительная компактность таких систем послужили основой для разработки технологии редактирования ДНК. Согласно этому методу, в клетки эукариот (например, человека) доставляют бактериальный белок Сas9 и крРНК, которую называют гидовой (гРНК). Вместо спейсера вирусного происхождения такая гРНК содержит целевую последовательность, соответствующую интересному для исследователя участку генома, например, где есть мутация, вызывающая какую-то болезнь. Получить же гРНК «на любой вкус» совсем несложно.
Эффекторный комплекс Cas9-гРНК вносит двуцепочечный разрыв в последовательность ДНК, точно соответствующую «гидовой» РНК. Если вместе с Cas9 и гРНК внести в клетку и последовательность ДНК, не содержащую мутацию, то место разрыва будет восстановлено по матрице «правильной» копии! Таким образом, используя разные гРНК, можно исправлять нежелательные мутации или вводить направленные изменения в гены-мишени. Высокая точность программируемого узнавания мишеней комплексом Cas9-гРНК и простота метода привели к лавинообразному росту работ по редактированию геномов клеток животных и растений (Jiang & Marraffini, 2015).
Гонка вооружений
В ходе эволюции бактерии и бактериофаги выработали ряд приспособлений, которые должны обеспечить каждому из участников «гонки вооружений» преимущество в борьбе с противником или возможность уклониться от его атаки.
Бактериофаги, как факторы среды, вызывают направленные изменения в геноме бактерий, которые наследуются и дают бактериям явное преимущество, спасая от повторных инфекций. Поэтому системы CRISPR-Cas можно считать примером ламарковской эволюции, при которой происходит наследование благоприобретенных признаков (Koonin et al., 2009)
Что касается систем CRISPR-Cas, то если фаг обзаведется мутацией в протоспейсере, эффективность его узнавания эффекторным комплексом снижается, и фаг получает возможность заразить клетку. Но и бактерия не оставит без внимания такую попытку ускользнуть от CRISPR-Cas: в качестве ответной реакции она начинает с резко возросшей эффективностью приобретать новые дополнительные спейсеры из ДНК уже «знакомого» фага, пусть и мутировавшего. Такое явление, названное праймированной адаптацией, многократно повышает эффективность защитного действия систем CRISPR-Cas (Datsenko et al., 2012).
Некоторые бактериофаги реагируют на наличие в бактериальной клетке систем CRISPR-Cas выработкой особых анти CRISPR-белков, способных связываться с белками Cas и блокировать их функции (Bondy-Denomy et al., 2015). Еще одно ухищрение — обмен участков генома вируса, на которые нацелена система CRISPR-Cas, на участки геномов родственных вирусов, отличающихся по составу нуклеотидной последовательности (Paez-Espino et al., 2015).
Результаты работ нашей лаборатории свидетельствуют, что зараженные клетки на самом деле погибают даже при наличии защиты CRISPR-Cas, но при этом они ограничивают численность вирусного потомства. Поэтому CRISPR-Cas правильнее относить к системам абортивной инфекции, а не к «настоящим» иммунным системам.
Благодаря постоянному совершенствованию биоинформатических алгоритмов поиска, а также включению в анализ все большего количества прокариотических геномов, открытие новых типов CRISPR-Cas систем является делом недалекого будущего. Предстоит также выяснить и детальные механизмы работы многих недавно открытых систем. Так, в статье, опубликованной в 2016 г. в журнале Science и посвященной анализу системы CRISPR-Cas VI типа, описан белок С2с2, образующий эффекторный комплекс с крРНК, который нацелен на деградацию не ДНК, а РНК (Abudayyeh et al., 2016). В будущем такое необычное свойство может быть использовано в медицине для регулирования активности генов путем изменения количества кодируемых ими РНК.
Изучение стратегий борьбы бактерий с бактериофагами, несмотря на свою кажущуюся фундаментальность и отвлеченность от задач практической медицины, принесло неоценимую пользу человечеству. Примерами этого могут служить методы молекулярного клонирования и редактирования геномов – направленного внесения или удаления мутаций и изменения уровня транскрипции определенных генов.
Благодаря быстрому развитию методов молекулярной биологии всего лишь через несколько лет после открытия механизма действия систем CRISPR-Cas была создана работающая технология геномного редактирования, способная бороться с болезнями, ранее считавшимися неизлечимыми. Доступность и простота этой технологии позволяют рассматривать ее как основу для медицины, ветеринарии, сельского хозяйства и биотехнологий будущего, которые будут базироваться на направленных и безопасных генных модификациях.
Нет никаких сомнений, что дальнейшее изучение взаимодействия бактерий и их вирусов может открыть перед нами такие возможности, о которых мы сейчас даже не подозреваем.
Abudayyeh O. O., Gootenberg J. S., Konermann S. et al. C 2c2 is a single-component programmable RNA-guided RNA-targeting CRISPR effector // Science. 2016. V. 353: aaf5573.
Barrangou R., Fremaux C., Deveau H. et al. CRISPR provides acquired resistance against viruses in prokaryotes // Science. 2007. V. 315. P. 1709–1712.
Bikard D., Marraffini L. A. Innate and adaptive immunity in bacteria: mechanisms of programmed genetic variation to fight bacteriophages // Curr. Opin. Immunol. 2012. V. 1 P. 15–20.
Bondy-Denomy J., Garcia B., Strum S. et al. Multiple mechanisms for CRISPR-Cas inhibition by anti-CRISPR proteins // Nature. 2015. V. 526. P. 136–139.
Calendar R., Abedon S. T. The Bacteriophages // 2nd Ed., Oxford University Press. 2006.
Datsenko K. A., Pougach K., Tikhonov A. et al. Molecular memory of prior infections activates the CRISPR/Cas adaptive bacterial immunity system // Nat. Commun. 2012. V. 3. P. 945
Jiang W., Marraffini L. A. CRISPR-Cas: New Tools for Genetic Manipulations from Bacterial Immunity Systems // Annu. Rev. Microbiol. 2015. V. 69. P. 209–28.
Jinek M., Chylinski K., Fonfara I., et al. A programmable dual-RNA-guided DNA endonuclease in adaptive bacterial immunity // Science. 2012. V. 337. P. 816–821.
Koonin E. V., Wolf Y. I. Is evolution Darwinian or/and Lamarckian? // Biol. Direct. 2009. V. 4. P. 42.
Lopez-Pascua L., Buckling A. Increasing productivity accelerates host-parasite coevolution // J. Evol. Biol. 2008. V. 3. P. 853–860.
Makarova K. S., Wolf Y. I., et al. An updated evolutionary classification of CRISPR-Cas systems // Nat. Rev. Microbiol. 2015. V. 11. P. 722–736.
Moineau, S., Pandian S., Klaenhammer T. R. Restriction/modification systems and restriction endonucleases are more effective on lactococcal bacteriophages that have emerged recently in the dairy industry // Appl. Envir. Microbiol. 1993. V. 59. P. 197–202.
Neve H., Kemper U., et al. Monitoring and characterization of lactococcal bacteriophage in a dairy plant // Kiel. Milckwirtsch. Forschungsber. 1994. V. 46. P. 167–178.
Nuñez J. K., Harrington L. B., et al. Foreign DNA capture during CRISPR-Cas adaptive immunity // Nature. 2015a. V. 527. P. 535–538.
Nuñez J. K., Kranzusch P. J., et al. Cas1-Cas2 complex formation mediates spacer acquisition during CRISPR-Cas adaptive immunity // Nat. Struct. Mol. Biol. 2014. V. 21. P. 528–534.
Nuñez J. K., Lee A. S., Engelman A., Doudna J. A. Integrase-mediated spacer acquisition during CRISPR-Cas adaptive immunity // Nature. 2015b. V. 519. P. 193–198.
Paez-Espino D., Sharon I., et al. CRISPR Immunity Drives Rapid Phage Genome Evolution in Streptococcus thermophilus // MBio. 2015. V. 6: e00262–15.
Shmakov S., Abudayyeh O. O., Makarova K. S., et al. Discovery and Functional Characterization of Diverse Class 2 CRISPR-Cas Systems. // Mol. Cell. 2015. V. 60. P. 385–397
Tan D., Svenningsen S. L., Middelboe M. Quorum sensing determines the choice of antiphage defense strategy in Vibrio anguillarum. // mBio 2015. V. 6: e00627–15.
Westra E. R., van Erp P. B., Künne T., et al. CRISPR immunity relies on the consecutive binding and degradation of negatively supercoiled invader DNA by Cascade and Cas3 // Mol. Cell. 2012. V. 46. P. 595–605.
Работа поддержана грантом РФФИ (№ 16-34-01176)