Во власти опухоли: почему метастазы так сложно остановить?
Метастазы в цельном мозге мыши, обработанном по специальной методике. Красный — MDA-231-D клетки, экспрессирующие mCherry; зеленый — сосуды, помеченные антителами к α-SMA, альфа-актинам гладких мышц [1].
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Когда в организме случилось несчастье, и из 100 триллионов нормальных клеток хоть одна переродилась в раковую и не была уничтожена, срабатывает спусковой крючок, и запускается рост опухоли. Постепенно она приспосабливает к себе окружающие клетки, а также оказывает значительное влияние на весь организм. С развитием заболевания некоторые раковые клетки покидают опухоль и формируют метастазы — вторичные очаги опухолевого роста. Зачастую своевременное удаление первичной опухоли и послеоперационная терапия не способны вызвать ремиссию. Оказывается, что первичная опухоль способна «обучать» микроокружение в очагах развития будущих метастазов уже на ранних этапах своего роста. Кроме того, метастазные раковые клетки перепрограммируют экспрессию своих генов так, чтобы лучше прижиться в новом месте обитания. Знание того, как предотвратить эти процессы, а не только рост первичной опухоли, поможет спасти до 90% людей, умирающих от основных видов рака.
Конкурс «био/мол/текст»-2017
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2017.

Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий и партнером номинации «Биомедицина сегодня и завтра» выступила фирма «Инвитро».

Революция в понимании природы метастазирования
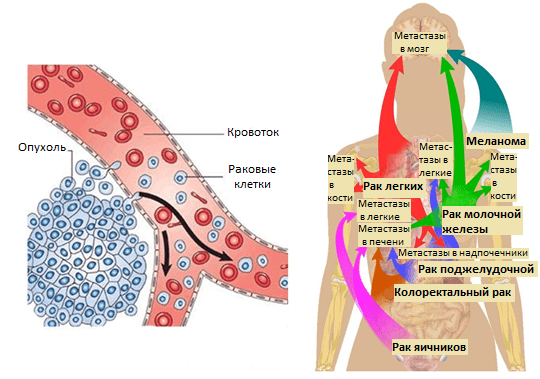
Усилия многих онкологов на протяжении последних десятилетий были направлены на установление деталей возникновения и развития рака — механизмов зарождения опухоли и регуляции ее активного роста, формирования благоприятного микроокружения из клеток стромы [2]. Эти знания несомненно привели к разработке новых подходов в терапии онкозаболеваний. Со временем стало понятно, что основная угроза рака заключена в способности к распространению по организму. Так, некоторые раковые клетки первичной опухоли (то есть развившейся изначально) отделяются от нее за счет эпителиально-мезенхимального перехода или других механизмов [3] и, попадая в кровоток или лимфоток, по маленьким капиллярам путешествуют в главные магистрали сосудистой системы. Они покидают ее за счет задержки в узких капиллярах органов, адгезии к их эндотелиальной стенке и выхода из просвета сосуда в строму органа (рис. 1). Лишь небольшой процент раковых клеток, покинувших первичную опухоль, преуспевает в этом процессе и выживает в новой среде. Эти клетки формируют будущие очаги роста опухоли в новых органах — метастазы.
Рисунок 1. Метастазирование и пути рассеивания раковых клеток.
Процесс рассеивания раковых клеток по организму, названный метастазированием (от древнегреч. «менять, переносить»: meta — «через» + histanai — «устанавливать»), впервые описал еще в 1889 году Стивен Педжет [4], но механизм его развития оставался загадкой для ученого сообщества долгое время (рис. 2).
Рисунок 2. Основоположники учений о метастазировании: английский хирург Стивен Педжет (слева) и американский патолог Джеймс Юинг (справа).
Педжет провел аналогию такого распространения раковых клеток с прорастанием семян. Они тоже выживают и делятся на плодотворной «почве» — в подходящем микроокружении. В те времена невозможно было найти этому экспериментального подтверждения, и долго преобладала совсем иная теория — Джеймса Юинга (рис. 2). Он утверждал, что основную роль в распределении метастазов по организму играет динамика кровотока и устройство сосудистой системы.
Наконец в 1970-е годы в ходе нескольких экспериментов по инъекции радиоактивно меченных раковых клеток мышам Исаак Фидлер смог доказать, что результат метастазирования также зависит от природы раковых клеток. В этом случае клетки меланомы развивали метастазы только в легких, но не в печени, в сосудах которой они также задерживались, но позже не выживали [5].
Позднее было установлено еще больше фактов, подтверждающих, что раковые клетки разной природы метастазируют преимущественно в определенные органы и иногда даже в заданной последовательности. Например, клетки рака молочной железы — сначала в кости, печень, лимфатические узлы, легкие, а потом уже в мозг; клетки рака желудочно-кишечного тракта и яичников — в печень и легкие; рака простаты — в основном, в кости (рис. 1). Явление специфичного распределения метастазов по организму назвали органотропией метастазирования. Чаще всего метастазы встречаются в легких, печени и костях.
Несмотря на активные исследования, в онкологии все еще остается много вопросов без ответа. Отличаются ли метастазные раковые клетки от других клеток первичной опухоли? Что лежит в основе органотропии? Как метастазам удается выжить после удаления первичной опухоли и проведенной химиотерапии?
Генетическая и эпигенетическая гетерогенность при метастазировании
Генетическая информация лежит в основе программирования поведения клетки. Перерождение нормальных клеток организма в раковые (злокачественная трансформация) обусловлено мутациями в генах-драйверах, которые приводят к неконтролируемому клеточному делению. Помимо таких выгодных для опухолевых клеток мутаций, также происходят мутации в генах-пассажирах, то есть тех, что изначально не имеют влияния на рост опухоли. С каждым поколением, новым клоном внутри опухоли, накапливаются эти генетические изменения, и некоторые клоны преуспевают больше остальных, что стало основой для формирования представления об эволюции внутри опухоли. Одна из предложенных гипотез, почему некоторые клетки опухоли приобретают способность к метастазированию, основана на схожем со злокачественной трансформацией принципе. По всей видимости, у них тоже накапливаются мутации в генах-драйверах, которые запускают этот процесс. Однако экспериментального подтверждения она так и не нашла, ученые сходятся во мнении, что большинство клеток первичной опухоли способны метастазировать. А вот что происходит позже с геномами метастазных клеток?
В результате сравнения геномов клеток первичных опухолей молочных желез и их локальных (в ближайших лимфатических узлах) и отдаленных метастазов (в печени, легких, дальних лимфатических узлах) было установлено, что геномы метастазов продолжают эволюционировать в своих очагах роста независимо от первичной опухоли [6]. Интересно, что паттерн мутаций схож между метастазами в одном органе, но различен между метастазами в разных органах. Это означает, что раковые клетки на самом глубоком уровне адаптируются к новому микроокружению в зависимости от занятой ими ниши. Изучение генетических изменений при метастазировании рака поджелудочной железы выявило наличие разных субклонов (новых поколений клона), которые формируют метастазы. Однако различия между ними оказались не больше, чем между двумя случайно взятыми клетками одного организма [7].
Интересно, что обнаружили как минимум один ген, FBXW7, мутации в котором противодействуют метастазированию [8]. Происходит это за счет усиления провоспалительной реакции, пролиферации и активности T-лимфоцитов, которые стимулируют формирование адаптивного иммунитета к опухолевым клеткам. Таким образом, мутации в гене FBXW7 противодействуют опухолевой иммунносупрессии. Ее проявления, такие как уменьшение количества лимфатических сосудов и эффекторных T-лимфоцитов в первичной опухоли, связаны с лицензированием метастазирования [8].
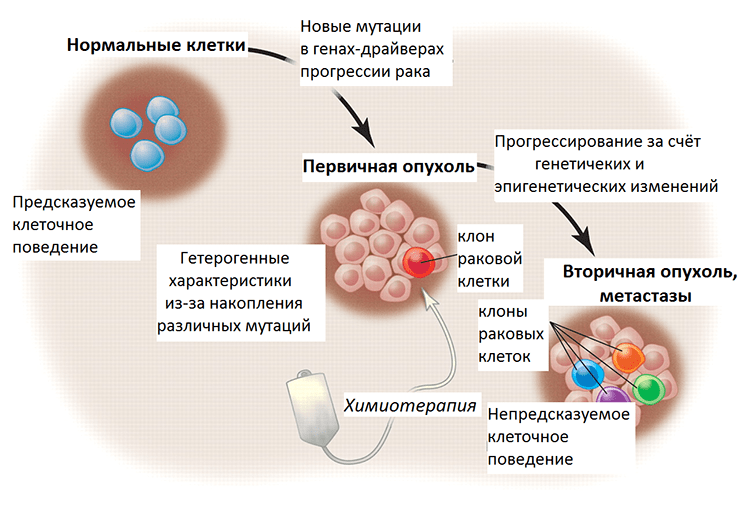
Следующую ступень в регуляции экспрессии генов после непосредственных изменений в ДНК (мутаций, вариаций числа копий и т.д.) занимают эпигенетические изменения (метилирование гистонов, ДНК и др.) (рис. 3). По своей природе они более пластичны, более переменчивы по сравнению с генетическими изменениями и подвластны влиянию клеточной сигнализации, которая подстраивается под воздействие внешних факторов. Оказалось, что эпигенетический код значительно отличается в клетках метастазов по сравнению с первичной опухолью. При раке поджелудочной железы потеря большого количества меток неактивного хроматина (гетерохроматина) — метилирования гистонов (H3K9, H4K20) — и ослабление метилирования ДНК связаны с метастазированием. Эти модификации в раковых клетках переводят участки гетерохроматина в активное состояние, доступное для транскрипционных факторов, и в результате усиливают экспрессию генов онкогенеза, таких как регуляторы мезенхимального фенотипа, KRAS-сигнализации и метаболизма [9].
Рисунок 3. Злокачественная трансформация и прогрессирование рака в перспективе генетических и эпигенетических изменений. Нормальные клетки ткани имеют предсказуемое поведение — темпы пролиферации, срок жизни, характер взаимодействия с другими клетками. При злокачественной трансформации накапливаются мутации, и постепенно опухоль становится генетически гетерогенной (состоит из нескольких клонов, поколений раковых клеток). Химиотерапия уничтожает некоторые клоны, тогда как другие, с выгодными в новых условиях мутациями, выживают и создают новых клонов. Их поведение уже непредсказуемо, так как генетические и эпигенетические изменения этих раковых клеток привели к приобретению ими новых свойств.
Метаболическая пластичность при метастазировании
Эпигенетическая регуляция является одним из важнейших механизмов программирования клеточного метаболизма. С ростом опухоли внутри нее образуются области с недостаточным снабжением кислородом (гипоксией), так как до них не доходят кровеносные сосуды. Это вызывает в раковых клетках активацию гена фактора, индуцируемого гипоксией (HIF-1α). Происходит это за счет эпигенетического освобождения, деметилирования промотора гена, который становится доступным для транскрипционных факторов. Усиленное образование и активность белка HIF-1α, в свою очередь, регулирует экспрессию генов множества метаболических ферментов и транспортеров, что приводит к комплексным изменениям метаболизма раковых клеток и поддерживает их потребности.
Клеточный метаболизм разделен на процессы расщепления с выделением энергии (катаболизм) и образования соединений с использованием энергии (анаболизм). Энергетический обмен клетки протекает за счет этапов клеточного дыхания — гликолиза, цикла трикарбоновых кислот и окислительного фосфорилирования. Раковые клетки по-своему приспосабливаются к сохранению продуктивности энергетического обмена в условиях недостатка кислорода. В первичной опухоли они, в основном, используют анаэробный гликолиз, а не окислительное фосфорилирование, как в нормальных клетках. Это усиленное поглощение глюкозы с преобразованием до лактата, выделяемого раковыми клетками, названо эффектом Варбурга. Он позволяет им выжить при гипоксии и активно пролиферировать за счет использования промежуточных соединений для биосинтеза и выделения энергии [10].
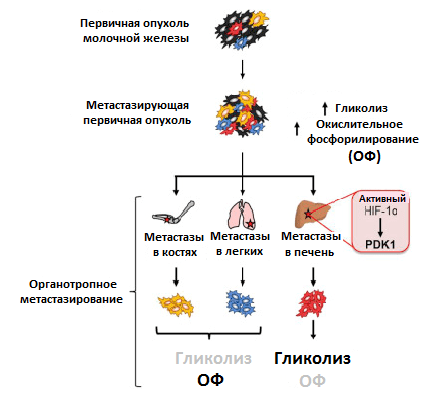
Преимущественный способ генерирования энергии у метастазов, однако, до сих пор мало изучен. Используя клетки рака молочной железы, обладающие широкой или специфической органотропией при метастазировании, ученые обнаружили различия в метаболизме первичной опухоли и метастазов. Раковые клетки, колонизировавшие кости и легкие, активировали использование окислительного фосфорилирования, колонизировавшие печень — гликолиз. Когда раковые клетки колонизировали все вышеперечисленные очаги, они активировали сразу оба метаболических пути (рис. 4) [11]. Похоже, что такая пластичность помогает раковым клеткам освоить новые ниши для колонизации. Например, в печени гликолитический фенотип поддерживается при росте метастазов за счет активности упомянутого ранее фактора HIF-1α, а также повышенной экспрессии белка PDK1. Это фермент, который ингибирует формирование соединения ацетил-КоА. И так как его поток на развилке с гликолитическим путем в цикл трикарбоновых кислот уменьшается, усиливается образование конечного продукта гликолиза — лактата [12].
Рисунок 4. Различия в метаболизме первичной опухоли и метастазов в разных органах. Условные обозначения: ОФ — окислительное фосфорилирование; HIF-1α — индуцируемый гипоксией фактор 1; PDK1 — пируватдегидрогеназный комплекс 1.
Почему же для метастазов в одном органе выгоднее использовать преимущественно один вид метаболизма, чем другой? Ответ на этот вопрос и роль различных факторов в регуляции метаболической пластичности раковых клеток еще только предстоит узнать.
Понятие о преметастазных нишах
И все же метастазные раковые клетки не могут в одиночку справиться со столь непростой задачей — освоением совершенно незнакомого места обитания. Эксперименты группы Дэвида Лидена в 2005 году впервые показали, что первичная опухоль за счет продуцируемых факторов стимулирует формирование так называемых преметастазных ниш в различных органах. Ученые показали, что раковые клетки первичной опухоли за счет стимулирования рецептора фактора роста сосудов (VEGFR-1) на миелоидных клетках-предшественниках активируют их распространение из костного мозга в известные очаги развития метастазов [13]. Кроме того, в этих очагах запускается избыточная экспрессия фибробластами одного из компонентов внеклеточного матрикса (ВКМ) — фибронектина. Миелоидные клетки-предшественники, имея рецепторы клеточной адгезии (интегрины) к этому белку, активно «ловятся на удочку» и заселяют преметастазные ниши. Они секретируют воспалительные цитокины, факторы роста и проангиогенные факторы, стимулирующие формирование сосудов. Это способствует ремоделированию стромы и колонизации ее метастазами (рис. 5) [13].
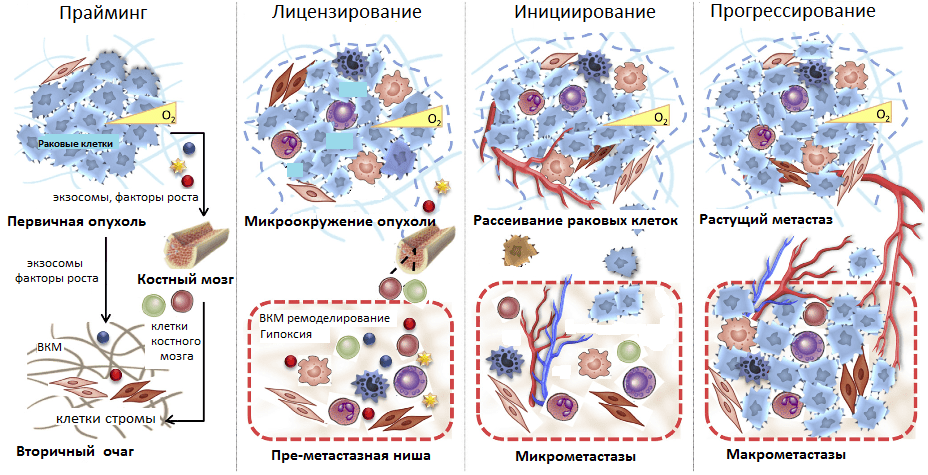
Рисунок 5. Стадии развития метастазов. Прайминг, или обучение, будущего вторичного очага роста первичной опухолью; лицензирование — иммуносупрессия первичной опухоли, создание благоприятного микроокружения в преметастазных нишах; инициирование — начало метастазирования и освоения преметастазной ниши; прогрессирование — рост метастазов во вторичном очаге.
Таким образом, в текущем представлении формирование метастазов происходит в несколько стадий. Начиная с раннего роста первичной опухоли происходит прайминг — обучение будущих ниш развития метастазов с помощью выделения различных факторов раковыми клетками, привлечения клеток из костного мозга. Затем клетки стромы первичной опухоли и преметастазных ниш (фибробласты, клетки миелоидного ряда, T-лимфоциты) формируют благоприятное микроокружение, лицензируя дальнейшее расселение метастазов. Фаза инициирования метастазирования заключается в росте сосудов, ангиогенезе, по которым метастазные клетки покидают первичную опухоль и приходят в преметастазные ниши. Прогрессирование — это финальный этап перехода микрометастазов в макрометастазы — вторичные сформированные опухоли. Он может занять от нескольких месяцев до нескольких лет (рис. 5).
Гетерогенность в механизмах формирования преметастазных ниш
Хотя для большинства органов характерна эта общая схема, существуют некоторые особенности в зависимости от места (органа) формирования ниши. Например, преметастазная ниша в печени и легких также формируется за счет привлечения нейтрофилов. Известно, что они могут помогать метастазирующим клеткам при интеграции в новую нишу за счет секретирования протеаз, цитокинов и непосредственного контакта с раковыми клетками при выходе из капилляров. Другой пример — клетки рака поджелудочной железы. Они выделяют экзосомы — липидные везикулы, которые переносят макрофаг-ингибирующий фактор (MIF). Их поглощают клетки Купфера в печени, и это запускает цепочку обучения ниши. Клетки Купфера синтезируют трансформирующий фактор роста β (TGF-β), клетки Ито активируются им и запускают перестраивание ВКМ, затем привлекая к нему макрофагов [15]. Их роль в микроокружении опухоли подробнее рассмотрена в статье «Одураченные макрофаги, или несколько слов о том, как злокачественные опухоли обманывают иммунитет» [16].
Метастазы в костях — одни из самых коварных, и их преметастазная ниша по-своему особенна. Например, оказалось, что при раке молочной железы только раковые клетки без рецепторов к эстрогену метастазируют в кости. Такие клетки первичной опухоли активно выделяют фермент лизилоксидазу. В костях он вызывает образование взрослых остеокластов и за счет этого стимулирует резорбцию кости. [17]. Именно эти «емкости» внутри кости метастазы занимают позднее. Другая и, пожалуй, основная функция лизилоксидазы — формирование поперечных связей между коллагеновыми волокнами ВКМ — также связана с образованием преметастазных ниш, но в легких. Преобразование коллагеновых волокон привлекает миелоидные клетки, а те позднее разрушают коллагеновые сети и дают путь раковым клеткам при заселении ткани легкого [18].
При некоторых типах рака, таких как меланома, для успешного метастазирования в лимфатические узлы и органы необходимо формирование новых лимфатических сосудов в их преметастазной нише. Недавно ученые установили, что такой лимфангиогенез начинается на ранних стадиях роста первичной опухоли, и медиатором его запуска является фактор роста мидкин, секретируемый клетками меланомы в составе экзосом или в свободном виде [19].
Безусловно, механизмы формирования преметастазных ниш в комплексе позволяют лучше понять развитие рака и не перестают удивлять своей сложностью.
Причины органотропии
Описанные различия в специфичных механизмах формирования ниш могут служить одним из объяснений органотропному метастазированию, но как раковые клетки, которые могут метастазировать сразу в несколько органов, выбирают только один из них?
Ключевой механизм, известный на данный момент, основан на обучении будущих очагов рассеивания метастазов с помощью специфичных к ним экзосом. Эти везикулы, ранее описанные в статье «Экзосома — механизм координации и взаимопомощи клеток организма» [20], представляют собой структуры с рецепторами на своей поверхности и генетическим и секретируемым материалом внутри. Ученые провели интересный эксперимент — выделили экзосомы от раковых клеток разного происхождения (рака груди, поджелудочной железы и пр.) и, внедрив их в кровоток мышей с отличным типом опухоли, показали, что с их помощью возможно перепрограммировать распределение метастазов по органам. Это обусловлено тем, что экзосомы разных типов рака преимущественно содержат на своей поверхности основные рецепторы адгезии, интегрины, специфичные к определенному белку ВКМ (к ламинину — α6β4 и α6β1; к фибронектину — αvβ5 и т.д.).
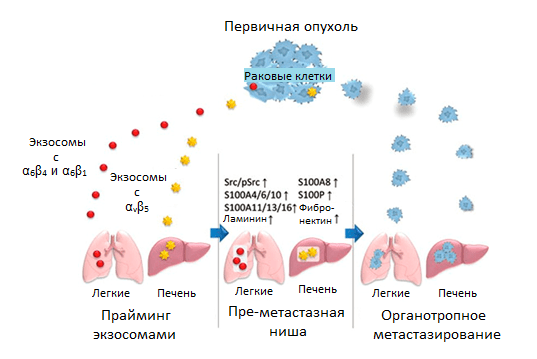
Именно они адресуют доставку экзосом в определенный орган, который преимущественно имеет этот специфический ВКМ-белок в составе стромы. Сливаясь с мембранами клеток стромы того или иного органа, экзосомы доставляют содержимое и запускают свою программу: в фибробластах легких — через экспрессию одних генов S100, в клетках Купфера в печени — через экспрессию других. Активность этих генов стимулирует клеточную сигнализацию и воспалительные реакции, которые занимаются обучением преметастазной ниши (рис. 6) [21].
Рисунок 6. Регуляция органотропного метастазирования с помощью прайминга преметастазной ниши экзосомами со специфическими рецепторами интегринами. Условные обозначения: α6β4 и α6β1 — гетеродимеры интегринового рецептора; Src/pSrc — пропорция неактивной/активной форм киназы.
Перспективы в терапии метастазирования
Подведем итог: описанные здесь механизмы, очевидно, усложняют картину течения онкозаболеваний и развития тактик их лечения. Важно подчеркнуть, что гетерогенность первичной опухоли и метастазов по ряду рассмотренных здесь признаков (генетическая, метаболическая, нишевая) дает понимание того, что следует использовать комбинированное и таргетное лечение на разных стадиях течения болезни. Как подтверждение тому — результаты одного из последних исследований, проведенных на материалах пациента с рецидивами между курсами длительной иммунотерапии. Сравнение популяций T-лимфоцитов из микроокружения разных метастазов показало, что они гетерогенны [22] и, следовательно, первичная, вторичные и т.д. опухоли по-разному отвечали на лечение.
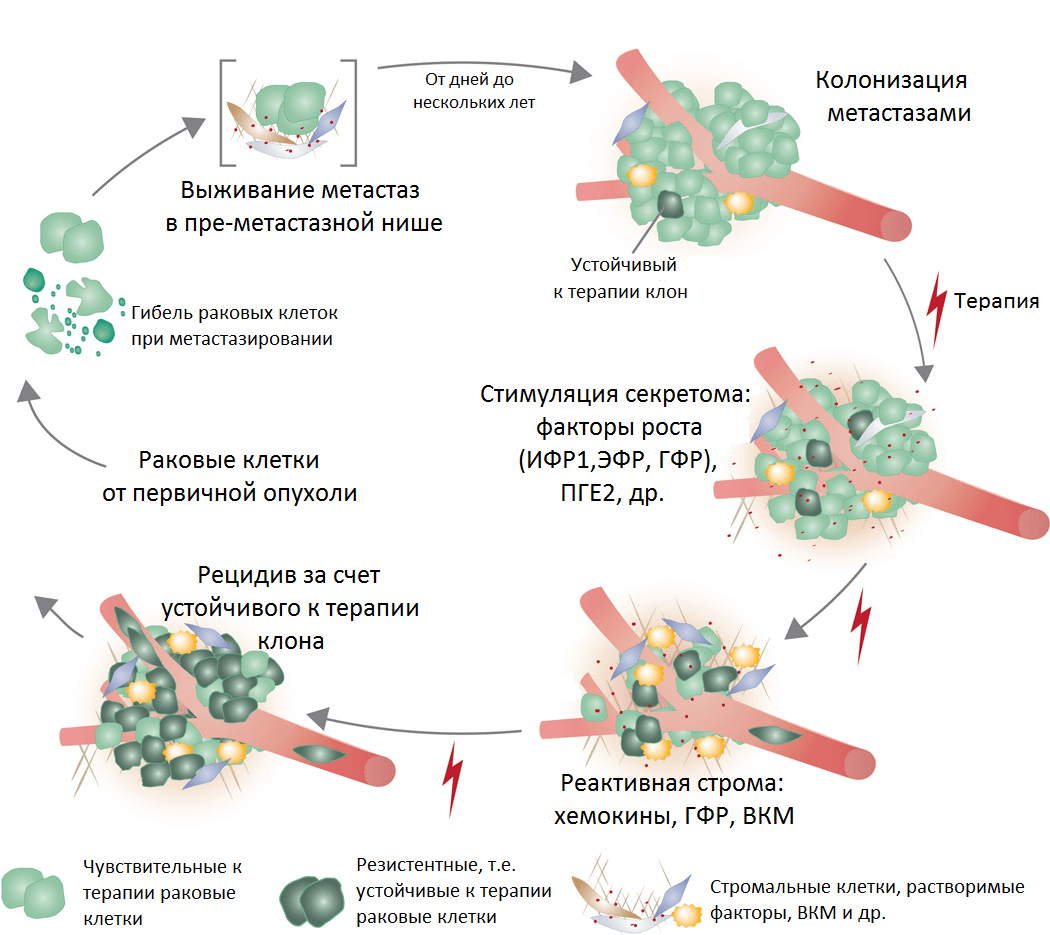
Мы также знаем, что после химиотерапии зачастую выживают субклоны раковых клеток с полезными в новой среде мутациями. Под стрессом воздействия цитостатиков субклоны раковых клеток активируют секрецию факторов роста и запускают клеточную сигнализацию, препятствующую гибели (рис. 7). Кроме того, их выживанию помогает поддержка клеток стромы, заодно изменяющих свое поведение на «оборонительное» под эффектом терапии.
Рисунок 7. Реакция метастазов на терапию, образование резистентности и развитие рецидива. Условные обозначения: ИФР1 — инсулиноподобный фактор роста; ЭФР — эпидермальный фактор роста; ГФР — фактор роста гепатоцитов; ПГЕ2 — простагландин 2; ВКМ — внеклеточный матрикс.
Обнаружение преметастазных ниш и понимание их устройства предложили по-новому взглянуть на развитие подходов в терапии. Если бы стало возможным предотвратить формирование преметастазных ниш, то с большой вероятностью было бы остановлено метастазирование, а значит, и возможность ремиссии. Будем и дальше следить за прорывами в этой области.
Как теоретически можно затормозить рост раковой опухоли
Онкологические заболевания занимают вторую строчку в списке причин смертности в развитых странах. Рак страшен и непредсказуем, но если не бездействовать, можно снизить вероятность заболеть им. Но что конкретно нужно делать? «РР» узнал у специалистов, возможно ли уберечь себя от рака, почему так важен баланс пользы и вреда и что делать, если риск онкологических заболеваний повышен.
Спасения нет?
Пугающее слово «рак» обозначает не одну болезнь, а огромное количество заболеваний — очень разных, но с похожим механизмом появления.
— В клетках нашего организма постоянно возникают мутации — изменения в геноме, происходящие под действием самых разных факторов. Из-за мутаций в процессе жизни в любом возрасте в организме образуются опухолевые клетки, — объясняет врач-онколог Национального медицинского исследовательского центра онкологии им. Н.Н. Петрова, эксперт Фонда профилактики рака Максим Котов.
Программа работы опухолевых клеток сломана, и они уже не способны образовать нормально функционирующие ткани организма. Конечно, организм защищается — отлавливает «плохие» клетки, в случае обнаружения мутации пытается починить испорченный генетический код или уничтожает клетку.
— Иногда эта система дает сбой, не справляется с потоком накопившихся мутаций — возникает опухоль. Чем дольше человек живет, тем больше мутаций накапливается. То есть основной фактор риска появления любого злокачественного образования — возраст, — добавляет Максим.
Есть ли возможность гарантированно защитить себя от развития опухоли? К сожалению, нет. Вероятность заболеть раком существует у каждого человека, и этот базовый риск увеличивается с возрастом.
— Обезопасить себя на 100% от развития рака не получится, это случайный процесс. Мы же не можем гарантировать, что при выходе на дорогу человека не собьет машина, даже если по этой дороге проезжает один автомобиль в день. Зато мы многое знаем о том, как снизить вероятность заболеть раком и умереть от него. На это и должны быть направлены наши практические действия, — объясняет Антон Барчук. — Однако даже раннее выявление опухоли не всегда автоматически означает положительный прогноз. Если мы видим маленькую опухоль, повышается вероятность, что не будет метастазов и лечение будет эффективным. Но гарантии нет.
Стоит ли рисковать?
К счастью, многое находится во власти человека, а не вероятностей. Самые главные риски онкологии давно и хорошо изучены: помимо возраста, среди них курение, употребление алкоголя, ожирение и избыточный вес, солнечное излучение.
Факторы риска и их влияние на организм подробно описаны в Европейском кодексе борьбы против рака, составленном Всемирной организацией здравоохранения. Там же даны рекомендации, как снизить риски, на которые мы можем повлиять, — их называют модифицируемыми.
— Курение повышает риск развития большой доли онкологических заболеваний — порядка 20% злокачественных опухолей так или иначе связано с курением. Причем у людей, которые не курят, но регулярно вдыхают табачный дым, риск рака тоже высок, — предупреждает Антон Барчук. — Другой фактор риска — употребление алкоголя. Долгое время считалось, что есть безопасная доза, употребляя которую человек ничем не рискует. Это, скорее всего, не так.
Ожирение и малоподвижный образ жизни вне зависимости от массы тела повышают риск развития колоректального рака, рака пищевода. В России сейчас заболеваемость этими видами рака повышается. Рак пищевода традиционно связывался с курением и алкоголем, но сейчас риск ассоциирован именно с ожирением.
Употребление красного мяса и переработанных мясных продуктов, таких как сосиски и колбасы, большого количества соли и сахара, тоже существенно повышает риск развития рака.
У женщин, которые не кормили грудью, может быть повышен риск развития рака молочной железы. Не всегда это можно модифицировать, но об этом надо помнить.
Еще одна причина многих онкологических заболеваний — вирус папилломы человека (ВПЧ). Он передается половым путем, но вызывает рак не только половых органов, но и опухоли головы и шеи. Сейчас распространенность онкозаболеваний, связанных с ВПЧ, в нашей стране растет, — перечисляет Антон Барчук.
Как работают факторы риска? Антон Барчук приводит упрощенную, но рабочую модель: фактор риска при постоянном воздействии на организм приводит к появлению предопухолевых изменений, затем опухолевых клеток; их количество растет, появляются симптомы заболевания, диагноз и его последствия.
Профилактика рака в идеале начинается с действий самого человека — нужно оценить свои риски и постараться их устранить. Нет фактора риска — вся цепочка не работает.
— Бросить курить или вообще не курить — значит устранить этот фактор риска, свести вероятность заболеть связанным с ним раком к минимуму (хотя и не к нулю, к сожалению). Рак шейки матки вызывается вирусом папилломы человека, а обезопасить себя от заражения ВПЧ можно с помощью вакцинации, раз и навсегда устранив этот фактор риска.
Зачем нужен скрининг
Следующий этап профилактики — скрининг рака. Его главная задача — предотвратить смерти от онкологических заболеваний, и он рассчитан на людей, у которых нет никаких симптомов.
— Мы можем находить предопухолевые изменения и устранять их — истинная опухоль тогда не появится. Например, так работает скрининг рака шейки матки и колоректального рака. В первом случае выявляют дисплазии, во втором — полипы, предшественники опухолей.
Иногда скринингом называют и выявление ранних опухолевых изменений. Например, скрининг рака молочной железы выявляет опухоль на раннем этапе, когда можно от нее избавиться без тех проблем, что несут продвинутые стадии рака. Снижение рисков называют первичной профилактикой, а скрининг — вторичной профилактикой, — объясняет Барчук.— Есть еще ранняя диагностика. Она направлена на выявление онкологических заболеваний у людей с минимальными симптомами или у людей из группы повышенного риска развития рака. А все последующие меры уже относятся к лечению.
— Важно понимать общее правило: чем раньше мы зайдем в тот сценарий, в котором развивается опухоль, тем выше будет эффективность наших действий, — заключает онкоэпидемиолог.
Баланс пользы и вреда
Итак, вы избавляетесь от вредных привычек и с завтрашнего дня начинаете заниматься спортом, но все равно хотите обследоваться, чтобы удостовериться, что онкологии у вас нет.
Есть несколько вещей, которые нужно знать о скрининге. Во-первых, он далеко не всегда сможет помочь. Так, по словам Антона Барчука, с помощью скрининга рака молочной железы можно предотвратить лишь 20% смертей. Во-вторых, важно знать о балансе вреда и пользы. Вред от скрининга тоже возможен — например, ложноположительные результаты теста, за которыми могут последовать ненужные операции, которые тоже несут свои риски, например риск смерти от анестезии. Поэтому все вмешательства и их риски нужно обсуждать с врачом.
Что делать
Если вы решили все же обследоваться, обратите внимание, что возможностей в нашем распоряжении не так уж много — на все виды рака провериться, увы, не получится.
— Есть пять доказанных способов снижения смертности от рака, причем из них только три показали себя в рамках больших скрининговых программ: это скрининг рака шейки матки, молочной железы и колоректального рака. Два остальных вызывают вопросы — скрининг рака легкого среди курильщиков и рака простаты методом ПСА. В некоторых случаях рак простаты не требует лечения, только наблюдения в динамике. Но если человек сдаст ПСА-тест и найдет у себя такую неагрессивную опухоль, скорее всего, он захочет ее удалить. А операция — это тоже риски.
ПСА-скрининг действительно снижает смертность от рака предстательной железы, но ценой гипердиагностики и ненужных операций, поэтому его не рекомендуют делать повально, а только после объяснения человеку, что его ждет. Чтобы он сам принял решение: «Я готов рискнуть и испортить себе жизнь ненужной операцией, которая приведет к недержанию мочи и к импотенции, но не умереть от рака простаты, хотя эта вероятность мала». К скринингу рака легкого тоже есть вопросы. Низкодозная компьютерная томография, в отличие от других методов скрининга, направлена только на заядлых курильщиков. Нужно знать не только возраст, но и статус курения — это затрудняет организацию программ, где принято высылать приглашения на скрининг. К тому же есть крайне эффективный способ профилактики рака — отказ от курения, поэтому для государства куда более эффективно поддерживать программы отказа от курения. Кроме того, в отличие от других программ, при скрининге рака легкого все заканчивается довольно инвазивной процедурой — биопсией легкого, поэтому скрининг будет работать, только если минимизировать такие вмешательства и осложнения, это требует крайне сложных процессов контроля качества, — говорит Антон Барчук.
— Почему для скрининга выбраны именно эти заболевания?
— Они наиболее распространены — это шанс снизить смертность в больших масштабах, а их стадии имеют значительную разницу в выживаемости Еще, например, есть опухоли, у которых прогноз неблагоприятный вне зависимости от стадии — это опухоли головного мозга (глиобластомы) или поджелудочной железы. А значит, скрининг здесь работать не будет, — объясняет Максим Котов.
— Какие процедуры включают в себя разные виды скрининга?
— Скрининг колоректального рака, как правило, двухэтапный. По достижении 50 лет раз в два года человеку предлагается сдать иммунохимический анализ кала на скрытую кровь. Если результат анализа положительный, нужно пройти колоноскопию — эндоскопическое исследование толстого кишечника. Колоректальный рак развивается из полипов в кишечнике. Во время колоноскопии эти полипы убирают, что сокращает риск развития рака толстой кишки,— продолжает Котов.
— Для скрининга рака шейки матки женщинам с 25 лет нужно проходить цитологическое исследование — с окраской по Папаниколау раз в три-пять лет в зависимости от качества исследования. С 30 лет — сдавать ВПЧ-тест раз в пять-десять лет. До 30 лет этот тест не надо делать: он дает слишком много положительных ответов, между тем как риск предраковых изменений крайне мал. Скрининг должен включать верификацию: после цитологии идет кольпоскопия, а после ВПЧ-теста — цитологическое исследование. Если осмотр шейки матки и биопсия подтверждают диагноз, выполняется конизация — удаление дисплазии или раннего рака.
Скрининг рака молочной железы начинается в 50 лет с маммографии раз в два года. Данная рекомендация исходит из баланса пользы и вреда: в 40 лет вероятность получить этот диагноз много меньше, чем в 50 лет. Возраст начала скрининга и интервалы установлены на основании данных исследований, проведенных за рубежом. В них постарались максимально соблюсти баланс. Начинать раньше или делать чаще одного раза в два года — значит, соглашаться на то, что нежелательных явлений будет больше ради крайне небольшой прибавки в снижении риска умереть от рака, — говорит Антон Барчук.
— Какие симптомы должны насторожить человека?
— Когда у человека есть жалобы, то мы уже занимаемся не скринингом, а ранней диагностикой. Если что-то беспокоит, нужно обратиться к врачу и пройти обследование. Например, человек заметил кровь в моче. Это может быть заболевание почек, острый цистит, а может — рак мочевого пузыря, — поясняет Максим Котов. — Любые симптомы, которые настораживают, беспокоят и не проходят со временем, требуют медицинского расследования. У курильщиков, например, меняются характеристики кашля, появляется кровь в мокроте. Когда где-либо кровь появляется — в стуле, в моче, в мокроте, — лучше обратиться к врачу. Если на теле появляются образования, родинки или пигментные пятна меняют форму или начинают кровоточить, — опять повод обратиться к врачу. Желательно раньше, чем позже.
— Чаще всего онкологические заболевания связаны с возрастом. И если такие симптомы проявляются в пожилом возрасте, обязательно нужно разбираться. Только не нужно сразу думать на любой симптом, что у вас рак: риск онкологии все-таки небольшой. Но обратиться к врачу и выяснить, что это, не помешает, — добавляет Антон Барчук.
К сожалению, даже если вы решили провериться на доступные скринингу виды рака, это сделать будет довольно сложно – из-за отсутствия в России грамотно организованных скрининговых программ.
По словам Максима Котова, в Москве уже запущен пилотный проект скрининга рака легкого методами низкодозной компьютерной томографии.
Чего делать не надо
— Какие методы скрининга онкологических заболеваний неэффективны?
— Скрининг рака щитовидной железы выявляет гигантское количество случаев рака, но все они неагрессивные — в большинстве своем их даже трогать не нужно. Огромный рост заболеваемости, никак не отражающийся на смертности. Опасней риски и последствия лечения, например лучевой терапии, ненужных операций.
— Были попытки внедрения скрининга рака полости рта — в том числе с помощью осмотра стоматолога, но смертности это не снижает, поэтому метод признан неэффективным. Самообследование при раке молочной железы по нынешним рекомендациям тоже неэффективно из-за низкой точности, — добавляет Максим Котов.
Рак по наследству
Кроме людей со средним риском развития злокачественных опухолей есть те, у которых этот риск повышен из-за генетических мутаций. Примерно 5–10% всех случаев рака возникает на фоне наследственной предрасположенности. Остальные случаи называются спорадическими (случайными).
— В основе любого рака лежат генетические изменения, но они в основном ненаследственные, так как находятся не в половых клетках организма. Но если такое генетическое нарушение возникает в половой клетке, то во всех клетках унаследовавшего ее организма ребенка будет присутствовать эта мутация. Риск развития определенного вида рака у такого человека существенно повышен — где-то в десятки раз. И рак будет начинаться раньше: ведь теперь клетке, чтобы стать раковой, нужно накопить, скажем, не 10 мутаций, а 9.
История, когда у человека есть мутация, увеличивающая риск развития рака, называется наследственным опухолевым синдромом. В США у женщины средний риск заболеть раком молочной железы — около 12%. А если у нее соответствующий опухолевый синдром, риск возрастает до 70–90%. Описано и изучено примерно два десятка опухолевых синдромов. Их носителями являются несколько процентов всей популяции — сколько точно, никто не знает, — поясняет Антон Тихонов, кандидат биологических наук, научный директор генетической лаборатории yRisk.
— Как заподозрить, что у человека может быть опухолевый синдром?
— Рак появляется скорее в раннем возрасте, чем в позднем — до 50 лет. Редко, но бывает, что у человека возникает сразу несколько опухолей — в разных или в парных органах, таких как молочные железы. Или если в истории семьи много случаев рака, особенно одного и того же вида. Например, есть такой опухолевый синдром — диффузный рак желудка. В семьях с определенной мутацией часто и рано по одной линии встречается рак желудка, а вдобавок часто повышается риск одного редкого подтипа рака молочной железы — лобулярного.
Еще один опухолевый синдром — наследственный рак молочной железы и яичников. Из названия понятно, что при наличии этой мутации возможно несколько видов рака; кроме того, при этой мутации также повышается риск рака предстательной и поджелудочной желез.
Ложиться ли на операцию для профилактики?
— Что делать, если нашел у себя один или несколько таких признаков наследственного опухолевого синдрома?
— Нужна консультация онкогенетика; целесообразно генетическое тестирование на опухолевые синдромы. Проблема еще в том, что это нужно делать здоровому человеку, а он не всегда в больницу ходит — ничего же не болит… Мы работаем в этой сфере, но нам очень сложно убеждать людей проходить тестирование. Да и некоторые врачи не очень верят в эффективность профилактики и скрининга, в тесты, которые выявляют людей из группы риска и дают им другую программу обследований. Пока у нас медицина в основном занимается лечением, а не превенцией.
— То есть людям с высоким риском нужен другой скрининг?
— Да, им не подходит среднепопуляционный скрининг. Например, при наличии мутации, ассоциированной с повышенным риском рака молочной железы, женщине нужна не только маммография, но и МРТ молочной железы. Начинать скрининг нужно раньше, и интервалы будут другие.
Для людей с некоторыми опухолевыми синдромами есть еще одна мера, правда, весьма радикальная — профилактическая операция. При том же диффузном раке желудка профилактическая мера одна — удаление желудка. Звучит страшно, но люди без желудка живут; конечно, есть модификации в диете и еще какие-то неприятности, но это лучше, чем умереть от рака в 40 лет. У людей с этим синдромом риск развития рака очень высок, этот вид рака очень плохо лечится.
То же при наследственном раке молочной железы и яичников: людям с наследственным синдромом настойчиво рекомендуется удалять яичники после рождения всех запланированных детей, ближе к менопаузе. Это резко снижает риск. В яичниках, в отличие от молочной железы, поймать рак очень сложно.
— Кроме операции, других опций нет?
— Лишь для небольшой части опухолевых синдромов превентивная операция является опцией — не все органы можно удалять без последствий для организма. Это мутации, повышающие риск рака желудка, молочной железы и яичников, наследственный семейный полипоз — полипы в кишечнике, из которых с большой вероятностью разовьется рак, причем, как правило, в раннем возрасте. В последнем случае удаляют кишечник. Для всего остального есть только еще более тщательный скрининг, внимательное отношение к факторам риска и к собственному здоровью.
Еще сейчас проходят клинические испытания препаратов, так называемая хемопревенция, — вы принимаете лекарства, которые снижают риск рака, не нужно делать операцию. В частности, для хемопревенции рака молочной железы и яичников сейчас испытываются препараты, которые обычно применяют в терапии рака. Исследования показывают, что они отлично работают в профилактике, но пока официального разрешения на их повсеместное применение нет.
Есть также данные, что людям с опухолевым синдромом, повышающим риск рака кишечника, нужно пить аспирин — это сильно снизит риск. Раньше аспирин назначали людям в возрасте, для профилактики сердечно-сосудистых заболеваний. Но последние исследования показали, что риск превышает пользу. И пока не понятно, стоит ли его пить людям с повышенным риском рака.
Еще важный момент: опухоль у человека с мутацией зачастую по своим характеристикам отличается от спорадической и лечится немного по-другому. Это важно знать, даже если человек уже заболел, потому что это может изменить подход к терапии и привести к более успешному результату лечения.
— А что насчет законодательного регулирования превентивных операций в России?
— Государство относится к превентивным операциями ужасно. По факту это серая зона. Чтобы удалить желудок, нужно придумать несуществующее заболевание.
Хорошо работает такая схема: допустим, у женщины нашли рак одной молочной железы, и она носитель генетической мутации, а значит, высок риск, что вторую железу (на данный момент здоровую) тоже поразит опухоль. Разумнее всего в этой ситуации удалить сразу обе железы. Это законодательство допускает, потому что, строго говоря, это не совсем превентивная мера — заболевание уже есть.
Никакого массового понятного пути, как это делать, к сожалению, нет. Однако частные клиники за это берутся.
— Что делать человеку, если он в группе риска?
— В первую очередь, нужно внимательно проходить скрининг — у хороших специалистов, на хороших приборах, по разумной схеме. Исключить из жизни все факторы риска развития рака — бросить курить, снизить потребление алкоголя до минимума, приблизить образ жизни к максимально здоровому — это очень сильно снижает риск. Если есть необходимость в профилактической операции, нужно искать врача «в теме» либо ехать за границу.
Какие процедуры скрининга нужны вам?
Алгоритм составил онкоэпидемиолог Антон Барчук
За полтора года мы проанализировали генетический материал 120 человек. Примерно у десятка выявили повышенный риск, нескольким рекомендовали довольно радикальные меры: например, выявили мутации, связанные с наследственным раком молочной железы и яичников, у пяти человек. Насколько мы знаем, никто никаких операций пока не делал — возраст неподходящий. Одна девушка даже сказала: «Не хочу яичники удалять, я планирую 12 детей родить в ближайшие 10 лет!».