Выбор препарата для диуретической терапии: взгляд клинического фармаколога
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Диуретики — это лекарственные средства, применяемые для усиления образования мочи, выведения из организма избыточного количества воды и устранения отеков. В обзорной статье представлены клинико-фармакологические подходы к диуретической терапии, данные о применении основных классов диуретиков. Основное внимание в статье сосредоточено на эффективности и профиле безопасности петлевых диуретиков и наиболее современного препарата из данной группы — торасемида, обладающего дополнительными свойствами. Обусловленная способностью блокировать альдостероновые рецепторы возможность торможения миокардиального фиброза под действием торасемида может обеспечивать этому препарату дополнительные преимущества с точки зрения замедления прогрессирования хронической сердечной недостаточности и увеличения выживаемости больных. Эффективность и профиль безопасности торасемида практически не меняются даже при существенном снижении скорости клубочковой фильтрации. Торасемид — вероятная альтернатива фуросемиду в лечении отечно-асцитического синдрома, в т. ч. резистентного к диуретикам, у больных циррозом печени. Торасемид отличается лучшей по сравнению с другими петлевыми диуретиками переносимостью. Торасемид, очевидно, следует рассматривать как наиболее предпочтительный препарат для лечения большинства вариантов отечного синдрома, в т. ч. резистентного к стандартным вариантам диуретической терапии.
Для цитирования: Максимов М.Л., Ермолаева А.С., Кучаева А.В. Выбор препарата для диуретической терапии: взгляд клинического фармаколога. РМЖ. 2018;1(II):115-119.
1 Kazan State Medical Academy, branch of the Russian Medical Academy of Continuous Professional Education
2 Sechenov University, Moscow
Diuretics are the drugs used to enhance diuresis, remove excess amounts of water from the body and eliminate edema.
The review presents clinical and pharmacological approaches to diuretic therapy, data on the use of the main classes of diuretics. The article focuses on the efficasy and safety of loop diuretics, and the latest drug from this group — torasemide, which has additional advantages. Due to the ability of torasemide to block aldosterone receptors thus inhibiting myocardial fibrosis, this drug may provide additional benefits in terms of slowing the progression of chronic heart failure and increasing patient survival. The efficasy and safety of torasemide are practically not affected even by a significant decrease in the glomerular filtration rate. Torasemide is a probable alternative to furosemide in the treatment of edematous-ascitic syndrome, including the one resistant to diuretics, in patients with liver cirrhosis. Torasemide is better tolerated than other loop diuretics. Torasemide, obviously, should be considered as the drug of choice for the treatment of most variants of edematous syndrome, including those resistant to standard diuretic therapy.
В статье с позиции клинического фармаколога обоснован выбор препарата для диуретической терапии. Основное внимание сосредоточено на эффективности и профиле безопасности петлевых диуретиков и наиболее современного препарата из данной группы — торасемида, обладающего дополнительными свойствами.
Введение
Классификация диуретиков
Принципы рациональной терапии и выбор диуретического препарата
Правила назначения диуретиков при ХСН
Терапия начинается только при наличии симптомов недостаточности кровообращения и признаках задержки жидкости.
Назначение диуретиков должно происходить на фоне уже применяемой терапии ингибиторами ангиотензинпревращающего фермента (АПФ) и бета-адреноблокаторами.
Мочегонная терапия осуществляется только в ежедневном режиме. Прерывистые курсы мочегонной терапии приводят к гиперактивации нейрогормональных систем и росту уровня нейрогормонов.
Назначение диуретиков идет «от слабейшего к сильнейшему».
При достижении клинического эффекта (уменьшение клинических проявлений НК, увеличение толерантности к физическим нагрузкам) начинается титрация «на понижение».
Тиазидные диуретики обладают высоким профилем безопасности только в комбинации с ингибиторами АПФ, блокаторами рецепторов ангиотензина (БРА) и бета-адреноблокаторами. В современных схемах роль тиазидных диуретиков в лечении ХСН умеренна. Следует особо помнить, что при низкой скорости клубочковой фильтрации (СКФ) и клинической картине хронической почечной недостаточности (ХПН) тиазидные диуретики неэффективны.
В лечении ХСН преимущество отдается петлевым диуретикам с большим периодом полувыведения (Т ½) и плейотропными эффектами. Комбинация диуретиков у пациентов с ХСН возможна только в ситуации, когда нет ХПН, а уровень калия — нормальный или пониженный. Строго обязателен лабораторный контроль уровня калия и креатинина. При уровне калия более 5,0–5,5 ммоль/л доза уменьшается на 50%. При более значимом отклонении от нормы — более 5,5 ммоль/л — проводится коррекция дозы вплоть до отмены препарата. После снижения дозы на 50% повторное увеличение дозы возможно спустя 1 мес. при условии стойкой нормокалиемии. При стабильном состоянии и отсутствии колебаний уровня креатинина контроль уровня калия должен осуществляться 1 раз в 3–6 мес. Необходимо помнить, что сочетание ингибиторов АПФ и калийсберегающих диуретиков всегда должно рассматриваться как приводящее к гиперкалиемии [11–13].
В таблице 3 представлены рекомендуемые начальные и поддерживающие дозы диуретиков, применяемых для лечения ХСН с сохранной и сниженной фракцией выброса (ФВ) [1, 3, 4]. 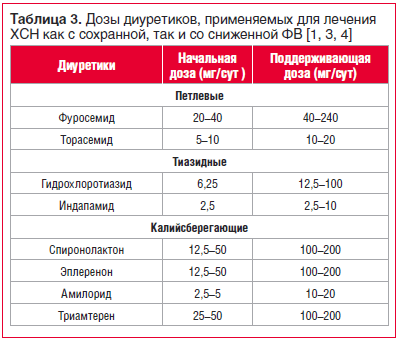
Петлевые диуретики
Возможности применения торасемида в клинической практике
Только для зарегистрированных пользователей
Применение диуретиков при хронической болезни почек
В зависимости от этиологии почечного повреждения ХБП подразделяют на диабетическую ХБП и недиабетическую ХБП.
Диабетическая ХБП характеризуется более ранним возникновением альбуминурии (микроальбуминурии), АГ и более высоким риском развития ССЗ и сердечно-сосудистых осложнений (ССО). Характер почечного поражения при СД 1 и 2 типа аналогичен, однако при ХБП на фоне СД 2 типа отмечается более раннее развитие гипертонии и сосудистого повреждения, чем при ХБП на фоне СД 1 типа (3). Развитие АГ у пациентов с СД 1 типа означает возникновение почечного повреждения, в то время как при СД 2 типа АГ может быть при отсутствии значимого поражения почек.
Недиабетическая ХБП включает целый ряд заболеваний: гломерулярные, за исключением СД; сосудистые, исключая реноваскулярные; тубулоинтерстициальные и поликистоз. Наибольшую роль в диагностике, а также в определении прогноза этих заболеваний играет уровень протеинурии (1).
Гломерулярные заболевания характеризуются более ранним развитием и более высоким уровнем протеинурии. Более низкие уровни протеинурии отмечаются при сосудистых и тубулоинтерстициальных заболеваниях, поликистозе.
При недиабетической ХБП также отмечается высокая распространенность АГ. В исследовании AIPRI (ACE Inhibition in Progressive Renal Insufficiency Study) она составила 92%, в исследовании REIN (Ramipril Efficacy in Nephropathy Study) – 84%, в исследовании MDRD (The Modification of Diet in Renal Disease) – 62% при тубулоинтерстициальных заболеваниях, 85% при гломерулярных, 87% при поликистозе, 100% при сосудистых заболеваниях (4, 5).
В проспективных исследованиях продемонстрирована сильная взаимосвязь между повышенным уровнем АД и высоким риском почечной недостаточности или ухудшения функционального состояния почек как при диабетической, так и при недиабетической ХБП (5, 6).
Нарушения функции почек являются важным фактором риска (ФР) развития ССО. Назначение медикаментозной терапии способно снизить риск развития ССО и почечных осложнений, замедлить прогрессирование нарушения функции почек (2).
Среди всех лекарственных препаратов, применяемых при ХБП, диуретики являются наиболее полезными в терапии большинства пациентов с ХБП. Влияние диуретиков на прогрессирование нефропатии в крупных рандомизированных исследованиях не изучалось (2). При ХБП возможно применение всех групп диуретиков (петлевые, тиазидные и тиазидоподобные, калийсберегающие). Все группы диуретиков действуют преимущественно за счет уменьшения реабсорбции натрия в почечных канальцах, однако они отличаются по механизму действия и точке приложения, а следовательно имеют специфические фармакологические свойства и особые показания к применению (7).
Принципы использования диуретиков у пациентов с ХБП сводятся к достижению целевого артериального давления (АД) и снижению сердечно-сосудистого риска (8). Выбор диуретического агента напрямую зависит от уровня СКФ и наличия необходимости в снижении объема внеклеточной жидкости. Неблагоприятные побочные реакции (НПР), ассоциированные с диуретической терапией при ХБП, аналогичны побочным эффектам, наблюдаемым в общей популяции. Единственное отличие заключается в более высокой частоте и большей их выраженности, что, наиболее вероятно, связано с применением более высоких доз диуретиков у пациентов с ХБП.
Рациональная диуретическая терапия должна быть основана на знании физиологии и фармакологии, принципов дозирования (стартовые дозы и принципы титрации дозы), принципов мониторирования функционального состояния почек и НПР (8).
Задержка натрия возникает при развитии дисбаланса между поступлением натрия и его выведением, что обуславливает увеличение объема внеклеточной жидкости (таблица 1).
Уменьшение экскреции натрия вызвано либо снижением клубочковой фильтрации натрия, либо повышенной его реабсорбцией в канальцах, либо сочетанным действием вышеуказанных механизмов.
Увеличение объема внеклеточной жидкости может вызывать компенсаторное уменьшение канальцевой реабсорбции натрия с дальнейшим восстановлением баланса натрия и развитием АГ. АГ как единственное проявление увеличения объема внеклеточной жидкости свидетельствует о недостаточном подавлении канальцевой реабсорбции. Резкое увеличение объема внеклеточной жидкости может отмечаться при очень высоком потреблении натрия или при выраженном снижении СКФ (например, при ХБП 4-5 стадии).
Истощение компенсаторных механизмов приводит к дальнейшему возрастанию объема внеклеточной жидкости и появлению клинических симптомов (см. таблицу 1). Повышенная канальцевая реабсорбция натрия отмечается при нефротическом синдроме, СН и циррозе печени. Кроме того, увеличение реабсорбции натрия могут вызвать такие лекарственные препараты, как флудрокортизон (альдостерон), эстрогенсодержащие препараты и НПВС.
Антигипертензивный эффект диуретиков основан на преимущественном уменьшении канальцевой реабсорбции натрия и соответственно увеличении его экскреции. Вышеуказанные механизмы обуславливают уменьшение объема внеклеточной жидкости и снижение АД. Эффективность диуретической терапии зависит от соблюдения немедикаментозных мер (ограничение употребления натрия), поэтому резистентность артериальной гипертонии к терапии диуретиками может быть обусловлена как неадекватной терапией, так и чрезмерным потреблением натрия.
Терапия диуретиками потенцирует действие большинства антигипертензивных препаратов. Это обусловлено тем, что большинство антигипертензивных препаратов стимулирует реабсорбцию натрия в почечных канальцах, увеличивая таким образом объем внеклеточной жидкости и ослабляя тем самым антигипертензивный эффект ЛП. Диуретики, уменьшая реабсорбцию натрия и объем внеклеточной жидкости, усиливают антигипертензивный эффект других препаратов. В то же время уменьшение объема внеклеточной жидкости активирует ренин-ангиотензиновую систему (РААС), что приводит к вазоконстрикции, нарастанию системного сосудистого сопротивления, а соответственно и к ослаблению антигипертензивного эффекта самих диуретиков. Именно поэтому наиболее эффективна для снижения АД комбинация диуретика с ингибиторами ангиотензин-превращающего фермента (ИАПФ) или антагонистами рецепторов ангитензина II (АРА II). Степень снижения АД на фоне комбинированной терапии диуретиком и ИАПФ или АРА II напрямую зависит от величины диуреза. Наибольшая эффективность отмечается при назначении петлевого диуретика.
Выделяют три группы диуретиков: тиазидные и тиазидоподобные, петлевые, калийсберегающие. По своему действию антагонисты альдостерона могут быть отнесены к последним. Кроме того, антагонисты альдостерона действуют на минералокортикоидные рецепторы сердца и кровеносных сосудов, а также на стероидные рецепторы в других тканях. Характеристика основных групп диуретиков представлена в таблице 2.
Тиазидные и тиазидоподобные диуретики можно условно разделить на два поколения. Первое поколение включает производные бензотиадиазина и фталимидина (хлорталидон), второе поколение – производные хлорбензамида (индапамид, ксипамид и др.) и квиназолинона (метолазон). Второе поколение характеризуется значительным натрий- и диуретическим действием при почечной недостаточности (9).
Тиазидные диуретики имеют многолетнюю историю эффективного снижения АД и риска ССО (10). Согласно результатам исследования ALLHAT, диуретики играют центральную роль в терапии эссенциальной артериальной гипертонии и являются предпочтительными препаратами для снижения АД и риска ССО (11). Также в исследовании ALLHAT в подгруппе пациентов с ХБП не было выявлено превосходство амлодипина и лизиноприла над хлорталидоном в предотвращении терминальной стадии ХБП у пациентов с АГ и ХБП (12).
Тиазидные и тиазидоподобные диуретики следует использовать при ХБП 1-3 стадии. Метолазон – единственный представитель тиазидоподобных диуретиков, эффективный при СКФ 2 (при применении в рекомендуемых терапевтических дозах). Он характеризуется низкой биодоступностью и длительным периодом полувыведения, в связи с чем его назначают 2-3 раза в неделю.
Если на фоне терапии тиазидными диуретиками не удается достичь целевого АД или отмечается прогрессирование ХБП до 4-5 стадии, их заменяют петлевыми диуретиками. В случае адекватного контроля АД и регресса отечного синдрома, смены тиазидного диуретика петлевым не требуется.
Петлевые диуретики представлены разнообразными химическими соединениями. Все они, за исключением этакриновой кислоты, имеют в своей структуре сульфонамидную группу. Препараты действуют в восходящем (толстом) сегменте петли Генле и оказывают мощное, но относительно короткое диуретическое действие. При ХБП петлевые диуретики сохраняют свои диуретические и натрийуретические свойства (9).
Транспорт петлевых диуретиков к месту действия осуществляется в ассоциации с белками плазмы, сродство к которым у данной группы препаратов крайне велико. Именно поэтому при снижении концентрации белка и альбумина в сыворотке крови (нефротический синдром, печеночно-клеточная недостаточность), эффективность петлевых диуретиков снижается. Из-за выраженного связывания с белками плазмы клубочковая фильтрация ЛП ограничена. Однако благодаря наличию механизма активного транспорта они в достаточном количестве секретируются в проксимальном отделе канальцев и в неизмененном виде поступают к месту своего действия (7, 9, 13).
В крупных исследованиях артериальной гипертонии в общей популяции петлевые диуретики не изучались, поэтому их эффективность в снижении риска ССЗ не известна. Тем не менее, они эффективно уменьшают объем внеклеточной жидкости и во многих исследованиях у пациентов с ХБП применялись в комбинации с другими антигипертензивными препаратами. Петлевые диуретики можно применять на всех стадиях ХБП. У пациентов со специфическими состояниями, обуславливающими повышенную реабсорбцию натрия, ответ на терапию снижается в зависимости от тяжести исходного заболевания, и требуются значительно большие дозы фуросемида для достижения положительного диуреза.
Так как эффективность тиазидных диуретиков в уменьшении объема внеклеточной жидкости снижается при низких значениях СКФ, то у этой категории больных с СКФ 2 предпочтительно использование петлевых диуретиков (8). В случае резистентности к петлевым диуретикам целесообразна комбинация петлевого диуретика с метолазоном (действует в нескольких отделах почечных канальцев) (8).
Тиазидные и петлевые диуретики повышают доставку натрия к дистальным канальцам, что в свою очередь повышает экскрецию калия с мочой. Этот побочный эффект может иметь положительное значение у пациентов с ХБП, особенно получающих терапию ИАПФ или АРА II. Несмотря на это, возможно развитие гипокалиемии, что при отсутствии адекватного лечения характеризуется аналогичным потенциальным риском, что и у пациентов без ХБП.
Триамтерен, амилорид, спиронолактон и эплеренон традиционно объединяют в группу калийсберегающих диуретиков, так как они способны снижать экскрецию калия почками. Другой общей для них характеристикой является способность действовать в конечной части дистальных канальцев и системе собирательных трубочек и вызывать слабый диуретический эффект. Все они по своей структуре относятся к разным химическим соединениям.
По механизму действия калийсберегающие диуретики можно разделить на две подгруппы: средства, блокирующие натриевые каналы эпителиальных клеток почек, и антагонисты альдостерона (7, 9).
Калийсберегающие диуретики, триамтерен и амилорид, в качестве монотерапии менее эффективны в снижении объема внеклеточной жидкости, чем тиазидные и петлевые диуретики. Как правило, они используются в дополнение к тиазидным и петлевым диуретикам для профилактики или лечения диуретик-индуцированной гипокалиемии или у пациентов с отечным синдромом. Калийсберегающие диуретики назначают больным с ХБП с большой осторожностью в связи с высоким риском развития гиперкалиемии (особенно у пациентов, принимающих ИАПФ или АРА II, и при СКФ 2 ). При ХБП калийсберегающие диуретики назначают, начиная с минимальных доз и постепенно титруя при частом мониторировании уровня калия. Антагонисты альдостерона действуют как калийсберегающие диуретики и могут быть использованы в тех же ситуациях, что и триамтерен с амилоридом (14).
Выбор диуретического препарата зависит от стадии ХБП и объема избыточной внеклеточной жидкости. В таблице 3 суммирована информация об отдельных представителях основных групп диуретиков.
В таблице 4 отражены принципы назначения основных групп диуретиков у пациентов с ХБП.
Резистентность к терапии диуретиками у пациентов с ХБП может быть связана с наличием состояний, обуславливающих повышенную реабсорбцию натрия в почечных канальцах, таких например, как нефротический синдром, СН, цирроз печени, терапия НПВС. Появление резистентности к диуретикам может быть следствием повышенного употребления натрия с пищей. Диагноз устанавливается путем определения суточной экскреции натрия с мочой. Уровень экскреции натрия > 100 ммоль/сут. свидетельствует о чрезмерном употреблении натрия с пищей.
Нежелательные побочные реакции
К побочным эффектам терапии диуретиками относятся артериальная гипотония, снижение СКФ, нарушения электролитного баланса (гипокалиемия, гиперкалиемия, гипонатриемия, гипомагниемия, гиперкальциурия, гипокальциурия), нарушения кислотно-основного состояния (метаболический алкалоз или ацидоз), аллергические реакции, влияние на развитие плода. Характеристика НПР диуретиков представлена в таблице 5.
Развитие большинства НПР диуретиков зависит от уровня потребления натрия с пищей. Высокий уровень поступления натрия с пищей препятствует истощению запасов внеклеточной жидкости, увеличивая тем самым экскрецию калия, магния и кальция с мочой. Наоборот, ограничение употребления натрия с пищей может сокращать вышеуказанные потери, но при этом повышается риск истощения запасов внеклеточной жидкости (15).
Артериальная гипотония и снижение СКФ являются следствием сокращения объема внеклеточной жидкости. Гипотония и/или транзиторное снижение СКФ наблюдаются как правило при первом применении диуретиков в сочетании с ИАПФ или АРА II (16). Гипотония наиболее часто наблюдается у пациентов с нефротическим синдромом, СН или циррозом печени на фоне терапии высокими дозами диуретиков. Другие причины уменьшения объема внеклеточной жидкости у пациентов с ХБП представлены в таблице 6.
Профилактика вышеуказанных НПР заключается в поэтапном увеличении дозы диуретиков и тщательном мониторировании при назначении комбинированной терапии диуретика и ИАПФ/АРА II. Терапия уже развившихся НПР состоит в снижении дозы диуретика (и/или ИАПФ/АРА II) или временной его отмене. Краткосрочное увеличение потребления натрия способствует восстановлению объема внеклеточной жидкости.
На фоне терапии диуретиками у пациентов с ХБП среди всех нарушений электролитного баланса и кисло-основного состояния наиболее часто встречаются гипокалиемия или гиперкалиемия, метаболический алкалоз, гипомагниемия, гипокальциурия или гиперкальциурия (обычно без изменения концентрации кальция в сыворотке крови). Вышеописанные состояния могут наблюдаться как по отдельности, так и сочетанно. Большинство диуретик-индуцированных нарушений электролитного баланса зависит от дозы диуретика и уровня потребления натрия. Поэтому, чем выше доза диуретика (и соответственно больше продолжительность действия), тем больше экскреция натрия и других электролитов (17).
Среди всех НПР, связанных с нарушением электролитного баланса, наибольшее значение имеет гипокалиемия. Гипокалиемия определяется при уровне калия сыворотки 2 (ХБП 3-5 стадии) ввиду повышенного риска развития гиперкалиемии.
Для мониторирования НПР важно определить уровень артериального давления, СКФ, сывороточного калия до начала диуретической терапии. Эти показатели в дальнейшем будут считаться исходным уровнем. Частота мониторирования НПР зависит именно от этих исходных показателей. Рекомендуемые интервалы мониторирования НПР на фоне диуретической терапии представлены в таблицах 8, 9.
Лечение возникших НПР в основном сводится к отмене препарата и коррекции водно-электролитных нарушений.
Диуретики – одни из самых важных препаратов нашего лекарственного обеспечения и несмотря на свой более чем 50-летний опыт применения до сих пор широко используются в мировой клинической практике и остаются незаменимыми в лечении ряда заболеваний. Диуретики – одни из наиболее часто применяемых лекарственных препаратов у пациентов с ХБП. Они уменьшают объем внеклеточной жидкости, снижают уровень АД, потенцируют эффекты ИАПФ и АРА II, а также других антигипертензивных препаратов. Рациональное применение диуретиков у этой категории больных снижает риск развития ССЗ и замедляет прогрессирование ХБП.
Почечная недостаточность: симптомы, стадии, лечение
Почечная недостаточность – острое или хроническое заболевание, при котором нарушаются фильтрационная, выделительная и другие функции почек с развитием многочисленных сбоев в работе всего организма. При этом происходит отравление собственными токсичными продуктами обмена веществ, попавшими в кровь – уремия. Патология, особенно при стремительном развитии, может угрожать жизни больного и требует скорейшего лечения.
Распространенность хронической болезни почек во всем мире в среднем составляет 13,4%. В России почечная недостаточность встречается у 36% лиц старше 60 лет и у 16% граждан трудоспособного возраста.
Причины
Хроническая форма заболевания чаще всего развивается как осложнение других патологий. Ранее основной причиной почечной недостаточности считался гломерулонефрит. В настоящее же время ведущее место занимают гипертоническая болезнь и сахарный диабет, приводящие к поражению мелких сосудов, питающих почки, и стойкому нарушению кровообращения в них.
Острая почечная недостаточность (ОПН) более чем в половине случаев связана с травмой или перенесенными операциями на органах малого таза. Развивается она также при неправильном приеме лекарственных препаратов, нарушении работы сердца, кровотечениях и шоке, генерализованной аллергической реакции, обезвоживании, циррозе, отравлении, аутоиммунных и инфекционных болезнях, онкологии, переливании несовместимой крови.
Симптомы почечной недостаточности
Почки не только очищают кровь от токсинов и выводят их из организма, но также регулируют водно-солевой баланс, контролируют уровень артериального давления, тонус сосудов, концентрацию гемоглобина, помогают в сохранении здоровья опорно-двигательного аппарата и сердца. Учитывая такое многообразие функций органа, почечная недостаточность проявляется многочисленными симптомами, выраженность которых зависит от стадии и формы заболевания.
При остром повреждении почек на начальной стадии имеются лишь проявления основного заболевания. Далее следует самая тяжелая, олигурическая стадия, продолжительностью до 3-х недель, со снижением суточного объема мочи менее 500 мл. Первым признаком болезни становится резкое уменьшение или прекращение мочеиспускания.
Состояние часто обратимо (если обратимо основное заболевание или состояние, приведшее к ОПН) и при правильном лечении переходит в полиурическую стадию почечной недостаточности с восстановлением объема мочи. При этом самочувствие пациента нормализуется, но может развиваться обезвоживание организма и присоединиться инфекция. Стадия полного восстановления продолжается от шести месяцев до года. При выраженных нарушениях состояние переходит в хроническую форму.
Хроническая почечная недостаточность (ХПН) развивается медленно, в течение нескольких месяцев и даже лет, и приводит к стойким изменениям в органе. На начальном этапе специфических симптомов обычно не бывает, но иногда человек может заметить снижение объема выделяемой мочи. Либо единственным проявлением патологии может быть никтурия – частое ночное мочеиспускание.
Осложнения
Болезнь осложняется появлением артериальной гипертензии, анемии, перикардита, аритмии и сердечной недостаточности, остеопороза, подагры, энцефалопатии, язвенной болезни желудка и двенадцатиперстной кишки, атеросклероза сосудов с развитием инфаркта и инсульта, синдрома беспокойных ног.
У детей почечная недостаточность приводит к задержке роста костной ткани.
Развитие почечной недостаточности у женщин во время беременности сопряжено с невынашиванием плода или формированием у него врожденных пороков.
Без лечения ХПН может закончиться смертью пациента от сердечно-сосудистых осложнений или уремической комы.
Диагностика
При первичном обследовании врач собирает анамнез заболевания, уточняя жалобы и давность симптомов. Далее проводятся осмотр кожных покровов, пальпация и поколачивание пальцами поясничной области.
Лечение почечной недостаточности
Обязательно проводятся диагностика и лечение патологии, послужившей причиной почечной недостаточности, а также устранение факторов риска.
При выраженном или длительном нарушении фильтрационной функции почек пациенту показано аппаратное очищение крови – гемодиализ. Процедура проводится регулярно и позволяет убрать из организма токсичные вещества. Альтернативой выступает перитонеальный диализ, при котором в брюшную полость вводится с последующим удалением специальный раствор, забирающий на себя вредные вещества.
В случае тяжелого течения хронической почечной недостаточности выполняется операция по трансплантации почки. После пересадки проводится курс терапии препаратами, подавляющими иммунитет, чтобы не произошло отторжения донорской ткани.





