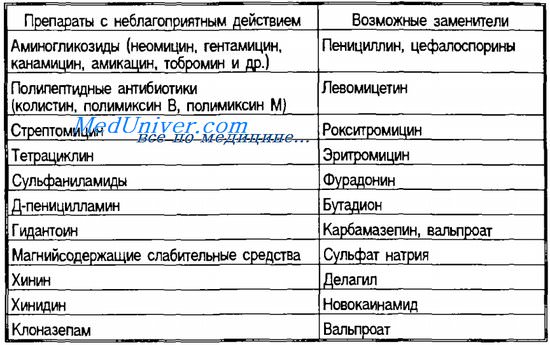
Какие обезболивающие можно при миастении
Основные направления лечения миастении — улучшение нервно-мышечной передачи применением ингибиторов холинэстеразы (антихолинэстеразные препараты, АХЭП), воздействия на вилочковую железу и на иммунную систему.
Ингибиторы холинэстеразы или антихолинэстеразные препараты — это прозерин, пиридостигмина бромид и оксазил. Прозерин применяется подкожно в инъекциях (ампулы по 1-2 мл 0,05 % раствора) и внутрь в таблетках по 0,015 г; пиридостигмина бромид (калимин, мес-тинон) также подкожно (ампулы по 1 мл 0,5 % раствора) и внутрь (таблетки по 0,06 г); оксазил (амбеноний, мети-лаза) — внутрь (таблетки по 0,005 г).
Дозы лекарств при миастении подбираются индивидуально. Следует учитывать, что продолжительность действия прозерина при пероральном приеме — 2-4 ч, пиридостигмина бромида — 4-6 ч, оксазила — 6-8 ч. Прием одной таблетки прозерина эквивалентен приему одной таблетки калимина и двух таблеток оксазила (соответственно, 15, 60 и 10 мг). Прозерин используется также в качестве обязательного диагностического теста. В то же время ингибиторы холинэстеразы, особенно прозерин, вызывают побочные явления (саливацию, дискомфорт со стороны желудочно-кишечного тракта, понос, бронхорею, мускариновый эффект).
Для длительного лечения миастении применяется, как правило, пиридостигмина бромид в индивидуальной дозировке — чаще 60—120 мг 3—4 раза в сутки. Препарат лучше применять после приема небольшого количества пищи (для уменьшения побочного влияния на желудочно-кишечный тракт).
Действие ингибиторов холинэстеразы при миастении усиливается при добавлении хлорида калия или калийсберегающих средств. Хлорид калия применяется внутрь по 0,5-1,0 г/сут (в молоке, соке или воде во время еды). Блокада проводящей системы сердца и нарушение функции почек служат противопоказанием. Калийсберегающим средством выбора является спиронолактон (верошпирон, альдактон). Препарат задерживает калий в клетках организма. Назначается по 0,025—0,05 г 3-4 раза в день; его не следует применять в первом триместре беременности, при мастопатии и гинекомастии.
Другим направлением в лечении миастении является коррекция иммунологических расстройств. Наиболее эффективным оказалось применение глюкокортикоидов. В настоящее время общепринято назначение их в повышенной дозе через день. Это не подавляет собственную глюкокортикоидную функцию надпочечников в дни перерыва приема этих препаратов. Дозы— 1—1,5 мг/кг в сутки. Эффект наступает на 4-6-й день лечения. После достижения и закрепления стойкого терапевтического эффекта дозы постепенно снижаются до 50 % от максимальной. В случае сохранения эффекта в дальнейшем можно постепенно (на 5 мг в месяц) осторожно уменьшать дозу. Как правило, удается достичь дозы 10—20 мг через день, которая сохраняется на много лет. Если при снижении дозы наступает ухудшение, дозу несколько повышают до компенсации состояния больного либо применяют другие методы лечения.
В последние годы принята пульс-терапия миастении преднизолоном в дозе 30 мг/кг на одно введение внутривенно. Этот метод показан при тяжелом состоянии больных, находящихся, как правило, в отделениях интенсивной терапии или реанимации, что в большинстве случаев ведет к выраженному улучшению.
Побочные явления при глюкокортикоидной терапии миастении общеизвестны: воспалительные и язвенные изменения со стороны желудка и двенадцатиперстной кишки, вегетативные расстройства, гипергликемия (возможен стероидный диабет), остеопороз позвоночника (возможна гормональная спондилопатия), кушингоид.
ЛЕКАРСТВЕННЫЕ ПРЕПАРАТЫ И МИАСТЕНИЯ
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Миастения – заболевание нейромышечного соединения, при котором нормальная передача нейромышечного импульса нарушается или не допускается антителами к ацетилхолиновым рецепторам (АХР).
Индуцированная лекарственными препаратами миастения
Нарушение проведения нервного импульса к мышце вследствие действия фармакологических препаратов возможно на 4 уровнях:
• пресинаптическом (средства для местной анестезии);
• нарушение выхода АХ из пресинаптических везикул;
• блокада постсинаптических АХР (курареподобное действие);
• ингибирование распространения импульса в концевой пластинке двигательного нерва из-за прерывания постсинаптического потока ионов.
Применение ряда препаратов связано с риском индуцирования или обострения миастении. Рассматривая эти связи, авторы выделяют 3 степени (по убыванию) влияния препаратов: определенные, вероятные и возможные ассоциации.
Пеницилламин индуцирует ряд аутоиммунных заболеваний, включая миастению. У 70% больных с развившейся пеницилламининдуцированной миастенией (ПИМ) определяют антитела к АХР. Эти антитела антигенно сходны с таковыми при идиопатической миастении. Большинство больных, описанных в литературе, получали пеницилламин по поводу ревматоидного артрита. Предполагают, что препарат связывается с АХР и действует как гаптен, индуцируя образование антител к рецептору. Согласно другой теории, пеницилламин, усиливая продукцию простагландина Е1, способствует накоплению его в синапсе, что в свою очередь препятствует связыванию АХ с АХР. Поскольку ПИМ развивается преимущественно на фоне аутоиммунного заболевания, ряд авторов предполагают, что пеницилламин может демаскировать идиопатическую миастению.
Кортикостероиды являются важным дополнительным средством в лечении миастении. Однако использование данных препаратов ассоциируется с миопатией, возникающей обычно при их длительном применении в результате усиленного катаболизма в мышцах; она затрагивает преимущественно проксимальные скелетные мышцы. Кортикостероидиндуцированная миопатия может «наложиться» на миастению. Транзиторное обострение миастении при использовании высоких доз кортикостероидов часто встречается, и об этом следует помнить. Но это не значит, что нужно отказаться от назначения кортикостероидов при тяжелой миастении. Многие клиницисты используют кортикостероиды как препараты первой линии при обострениях миастении.
Антихолинергические препараты теоретически могут нарушать нейромышечную передачу в концевой пластинке двигательного нерва вследствие конкурентного подавления связывания АХ с постсинаптическими рецепторами. Описано возникновение миастенических симптомов у больного паркинсонизмом под влиянием тригексифенидила гидрохлорида.
Антибактериальные препараты (ампициллин натрий, имипенем и циластатин натрий, эритромицин, пирантел памоат) могут вызвать значительное ухудшение состояния и/или обострение симптомов миастении.
Сердечно-сосудистые средства. Описан случай усиления птоза и диплопии, присоединения дисфагии и слабости скелетных мышц у больной миастенией после приема пропафенона гидрохлорида, что связывают со слабым b-блокирующим эффектом данного препарата. Описан случай клинического ухудшения миастении на фоне лечения верапамилом гидрохлоридом. Этот эффект может быть связан с редукцией содержания внутриклеточного ионизированного кальция, что, в свою очередь, может нарушить обратный поток ионов калия.
Хлорохин фосфат – антималярийный и противоревматический препарат, способный индуцировать миаcтению, хотя и значительно реже, чем пеницилламин.
Блокаторы нейромышечной проводимости применяют при миастении с осторожностью в связи с риском развития длительных параличей. Предшествующее лечение пиридостигмином снижает ответ на недеполяризующие нейромышечные блокаторы.
Глазные препараты пропаракаин гидрохлорид (антимускариновый мидриатик) и тропикамид (местный анастетик) при последовательном применении вызвали внезапную слабость и птоз у больной миастенией.
Прочие лекарственные препараты. Ацетазоламид натрий снизил реакцию на эдрофониум у 7 больных миастенией, что, возможно, связано с подавлением карбоангидразы. При изучении гиполипидемического препарата декстрокарнитина-левокарнитина у 3 больных с терминальной стадией патологии почек развилась слабость жевательных мышц и мышц конечностей. На фоне лечения a-интерфероном описано 3 случая развития миастении. Обострение миастении зарегистрировано при назначении метокарбамола по поводу болей в спине. Рентгеноконтрастные препараты (иоталамическая кислота, диатризоат меглюния) в отдельных случаях вызывали обострение миастении, однако, по мнению авторов, миастения не является противопоказанием для применения рентгеноконтрастных препаратов.
Авторы пришли к заключению, что ряд препаратов при миастении следует назначать с осторожностью. Назначая новый препарат, следует проводить тщательное наблюдение на предмет выявления генерализованной мышечной слабости и особенно таких симптомов, как птоз, дисфагия, затруднение жевания, дыхательная недостаточность. Индукция ятрогенной миастении связана с применением пеницилламина.
Wittbrodt ЕТ, Pharm D. Drugs and Myasthenia Gravis. Arch Intern Med 1997;157:399–408.
Лечение тяжелой миастении. Часть 3
» data-image-caption=»» data-medium-file=»https://unclinic.ru/wp-content/uploads/2020/12/lechenie-tjazheloj-miastenii-900×600.jpg» data-large-file=»https://unclinic.ru/wp-content/uploads/2020/12/lechenie-tjazheloj-miastenii.jpg» title=»Лечение тяжелой миастении. Часть 3″>
Галина Кучма, врач УЗИ. Редактор А. Герасимова
В первую очередь для лечения тяжелой миастении применяются медикаментозные препараты.
Лекарства для симптоматического лечения
Все подгруппы тяжелой миастении реагируют на ингибирование ацетилхолинэстеразы.
Тяжелая миастения с применением антител к мышечно-специфической киназе хуже реагирует на симптоматические лечебные препараты, чем другие подгруппы миастении. Ювенильная миастения характеризуется отличным ответом на лечение пиридостигмином.
Доза пиридостигмина подбирается с учетом влияния на мышечную силу, дозозависимых побочных реакций, и чаще всего мешает работе желудочно-кишечного тракта. Типичные побочные эффекты включают диарею, боль в животе, судороги, метеоризм, тошноту, повышенное слюноотделение, задержку мочи и повышенное потоотделение. Поэтому для каждого пациента следует подбирать индивидуальную дозу, которая может меняться в разные дни. Эффекты пиридостигмина остаются неизменными в течение многих лет. Пациентам с легкой формой заболевания, достигшим полной ремиссии с помощью симптоматических лекарств, никакие другие лекарства не рекомендуются
Иммуносупрессивная терапия
Большинству пациентов с миастенией требуется иммуносупрессивная терапия для полного или частичного восстановления физических функций и полного качества жизни. Иммунодепрессанты назначают всем пациентам, которые не реагируют адекватно на лечение только симптоматическими препаратами.
» data-medium-file=»https://unclinic.ru/wp-content/uploads/2020/12/immunosupressivnaja-terapija.jpg» data-large-file=»https://unclinic.ru/wp-content/uploads/2020/12/immunosupressivnaja-terapija.jpg» loading=»lazy» src=»https://unclinic.ru/wp-content/uploads/2020/12/immunosupressivnaja-terapija.jpg» alt=»Иммуносупрессивная терапия» width=»900″ height=»563″ srcset=»https://unclinic.ru/wp-content/uploads/2020/12/immunosupressivnaja-terapija.jpg 900w, https://unclinic.ru/wp-content/uploads/2020/12/immunosupressivnaja-terapija-768×480.jpg 768w» sizes=»(max-width: 900px) 100vw, 900px» title=»Лечение тяжелой миастении. Часть 3″> Иммуносупрессивная терапия
Иммуносупрессивная терапия первой линии – преднизолон с азатиоприном. Изменение дозировки преднизолона в разные дни часто снижает побочные эффекты глюкокортикоидов, но клинических исследований на эту тему мало. Чтобы болезнь не усугубилась, дозу обычно увеличивают постепенно – с 60 мг до 80 мг в разные дни.
По достижении контроля над симптомами дозу глюкокортикоидов следует постепенно снижать до минимальной эффективной поддерживающей дозы с добавлением симптоматического лечения. которая обычно составляет от 10 мг до 40 мг в разные дни.
Основная цель лечения глазной миастении гравис – предотвратить генерализацию заболевания. Ретроспективные и наблюдательные клинические исследования показали, что монотерапия преднизолоном снижает этот риск. Многие специалисты рекомендуют лечение низкими дозами глюкокортикоидов пациентам с глазной миастенией гравис, у которых есть стойкие симптомы и факторы риска, такие как установленные антитела к рецепторам ацетилхолина, увеличенный тимус, нейрофизиологические доказательства повреждения других мышц (не только глаза).\
Большинству пациентов, получающих преднизолон, дополнительно назначают азатиоприн, поскольку эта комбинация препаратов приводит к лучшим функциональным результатам и меньшему количеству побочных эффектов, чем монотерапия преднизолоном.
Если глюкокортикоиды противопоказаны или пациент отказывается их принимать, может быть назначена монотерапия азатиоприном. Рекомендуемая доза составляет 2-3 мг на килограмм массы тела. Азатиоприн подавляет синтез пурина, тем самым подавляя пролиферацию клеток, особенно В- и Т-клеток. Если возможно, перед лечением азатиоприном следует проверить активность тиопуринметилтрансферазы, поскольку слабая активность этого фермента увеличивает риск побочных эффектов азатиоприна. Этот фермент неактивен всего для 0,3% всего населения, а низкая активность обнаруживается у 10% населения.
Азатиоприн не рекомендуется пациентам, у которых нет активной тиопуринметилтрансферазы, а пациентам с низким уровнем этого фермента следует назначать более низкую дозу азатиоприна. Воздействие азатиоприна на мышечную слабость часто проявляется всего через несколько месяцев после начала лечения, и в этот период пациентам следует назначать другие иммунодепрессанты. Длительное лечение азатиоприном безопасно для пациентов любого возраста.
Многие руководящие принципы рекомендуют для лечения миастении легкой и средней степени тяжести микофенолата мофетил, хотя польза этого препарата не была продемонстрирована в двух краткосрочных проспективных исследованиях=. Этот препарат блокирует синтез пурина и останавливает пролиферацию В- и Т-клеток.
Метотрексат, циклоспорин и такролимус – это иммунодепрессанты второго ряда. Эффекты этих препаратов аналогичны эффектам азатиоприна.
Ритуксимаб – потенциально многообещающий препарат для лечения миастении. Это моноклональное антитело специфически связывается с поверхностным антигеном CD20 в В-лимфоцитах и поэтому эффективно при лечении опосредованных антителами заболеваний, таких как тяжелая миастения. Ритуксимаб также влияет на Т-клетки.
» data-medium-file=»https://unclinic.ru/wp-content/uploads/2020/12/rituksimab.jpg» data-large-file=»https://unclinic.ru/wp-content/uploads/2020/12/rituksimab.jpg» loading=»lazy» src=»https://unclinic.ru/wp-content/uploads/2020/12/rituksimab.jpg» alt=»Ритуксимаб» width=»900″ height=»578″ srcset=»https://unclinic.ru/wp-content/uploads/2020/12/rituksimab.jpg 900w, https://unclinic.ru/wp-content/uploads/2020/12/rituksimab-768×493.jpg 768w» sizes=»(max-width: 900px) 100vw, 900px» title=»Лечение тяжелой миастении. Часть 3″> Ритуксимаб
Группа экспертов, которая одобрила последние рекомендации по миастении, не смогла прийти к единому мнению о месте ритуксимаба в лечении этого заболевания. Хотя в небольших клинических испытаниях две трети пациентов с тяжелой миастенией, которые не ответили должным образом на преднизолон и азатиоприн, показали значительное улучшение при применении ритуксимаба. Рекомендуемая индукционная доза не установлена. Лечение следует повторить через несколько месяцев, если симптомы повторяются.
При лечении других аутоиммунных заболеваний обнаружен положительный эффект моноклональных антител. Они влияют на функции В- и Т-клеток, комплемента и других иммуноактивных элементов.
У пациентов с миастенией, появившейся в пожилом возрасте или у которых есть антитела к тимоме или мышечно-специфической киназе, с большей вероятностью разовьются наиболее тяжелая форма заболевания. Обычно они требуют длительной иммуносупрессивной терапии, хотя у некоторых пациентов с поздней миастенией гравис течение заболевания более легкое, больше похоже на раннюю миастению.
Показание для иммуносупрессивной терапии – обнаружение антител к мышечно-специфической киназе, тайтину, рецепторам рианодина или Kv1.4. Миастения, характеризующаяся появлением мышечно-специфических антител к киназе, лучше поддается лечению ритуксимабом.
Тимэктомия – еще один метод лечения миастении
Пациентам с миастенией и тимомой следует сделать тимэктомию – операцию по удалению тимуса. Преимущества тотальной тимэктомии продемонстрированы даже у пациентов с ранней миастенией, у которых не была диагностирована тимома.
Основным механизмом патогенеза тимуса при миастении является выработка антител к рецепторам ацетилхолина. В большинстве клинических испытаний сравнивали результаты у пациентов, которым удалили вилочковую железу, и которые не перенесли эту операцию. Результаты почти всех исследований показали, что результат был лучше у пациентов, перенесших тимэктомию. Международное рандомизированное исследование 126 пациентов с ранней или поздней миастенией. подтвердили преимущество ранней тимэктомии у пациентов с генерализованной миастенией, с длительностью заболевания до 3–5 лет, до 60–65 лет и симптомами, плохо контролируемыми препаратами, блокирующими холинэстеразу.
В европейских руководствах рекомендуется ранняя тимэктомия пациентам с ранней миастенией. У таких пациентов обычно наблюдается гиперплазия щитовидной железы. Также следует рассмотреть возможность тимэктомии у детей с миастенией.
Большинство пациентов с поздней миастенией имеют атрофический тимус. Однако гиперплазия щитовидной железы может развиться у более молодых пациентов в группе поздней миастении. Тимэктомию следует рассматривать у пациентов с генерализованной миастенией, у которых есть антитела к рецепторам ацетилхолина и у которых развиваются симптомы в возрасте от 50 до 65 лет, особенно если биомаркеры заболевания аналогичны биомаркерам ранней миастении.
Тимэктомия не проводится в следующих случаях:
Тяжелая миастения: особенности лечения
Пациентов с развивающейся прогрессирующей мышечной слабостью и требующих интубации или неинвазивной вентиляции легких, следует лечить быстродействующими иммунодепрессантами. Тяжелый миастенический криз, проявляющийся быстрым ухудшением состояния пациента и прогрессирующей мышечной слабостью, требует аналогичного лечения.
Нарастающая общая слабость, респираторная, сердечная недостаточность, тяжелая инфекция и сопутствующие патологии приводят к решению о показаниях для лечения миастенического криза в отделении интенсивной терапии. В этом случае мониторинг жизненно важных функций, параметров газов крови имеет ограниченное значение, так как ухудшение состояния пациента может быть очень внезапным и неожиданным, проявляясь в результате миастенического истощения.
Эффективны при лечении тяжелой миастении внутривенные иммуноглобулины и плазмаферез. Выбор между этими методами лечения зависит от индивидуальных факторов пациента, клинического опыта и доступности. Внутривенные иммуноглобулины более удобны для пациентов из-за более легких побочных эффектов.
Иногда для пациента может быть эффективным только один метод лечения, а другой – нет. Лечение этими методами следует сочетать с длительной иммуносупрессивной терапией. У некоторых пациентов эффект от лечения может быть отсроченным. Иммуносупрессивная терапия должна сочетаться с интенсивной терапией до тех пор, пока это необходимо для достижения ремиссии.
Миастенический криз с дыхательной недостаточностью в настоящее время является редким заболеванием, а смертность от миастенического криза невысока.
Поддерживающая терапия миастении и последующее наблюдение за пациентами
Пациентам с миастенией, в зависимости от состояния, рекомендуются физические нагрузки низкой и средней интенсивности и программы систематических тренировок. Следует избегать лишнего веса. При появлении глазных симптомов можно использовать глазные средства.
» data-medium-file=»https://unclinic.ru/wp-content/uploads/2020/12/glaznye-sredstva-900×600.jpg» data-large-file=»https://unclinic.ru/wp-content/uploads/2020/12/glaznye-sredstva.jpg» loading=»lazy» src=»https://unclinic.ru/wp-content/uploads/2020/12/glaznye-sredstva.jpg» alt=»Глазные средства» width=»900″ height=»600″ srcset=»https://unclinic.ru/wp-content/uploads/2020/12/glaznye-sredstva.jpg 900w, https://unclinic.ru/wp-content/uploads/2020/12/glaznye-sredstva-768×512.jpg 768w» sizes=»(max-width: 900px) 100vw, 900px» title=»Лечение тяжелой миастении. Часть 3″> Глазные средства
По возможности не следует назначать пациентам с миастенией миорелаксанты, пеницилламин, некоторые антибиотики – фторхинолоны, макролиды, аминогликозиды. Статины могут усугубить миастению, но миастения не является противопоказанием к назначению статинов по мере необходимости. Показания к применению статинов у пациентов с миастенией такие же, как у пациентов без этого заболевания. Если показаны статины, их можно назначить, но требуется бдительность из-за прогрессирования мышечной слабости.
Дыхательная недостаточность из-за слабости диафрагмальных и межреберных мышц представляет собой наибольший риск. Но пациентам с миастенией следует уделять особое внимание дыхательной функции во время любых хирургических вмешательств, в том числе тимэктомии.
Важная часть лечения миастении – оптимальное лечение всех сопутствующих патологий. Это серьезная проблема при лечении пожилых пациентов с сопутствующими заболеваниями.
Пероральный прием пиридостигмина и преднизолона во время беременности безопасен. Новые исследования предоставляют информацию о том, что лечение азатиоприном и циклоспорином также безопасно для беременных. Между тем, микофенолят мофетил и метотрексат противопоказаны беременным из-за риска тератогенных эффектов.
Женщинам после прекращения лечения ритуксимабом рекомендуется избегать беременности в течение 1 года.
Пациенткам с обострением во время беременности можно назначать внутривенные иммуноглобулины и плазмаферез. Следует поощрять грудное вскармливание. Транзиторная миастения встречается у новорожденных в 15% случаев из-за антител IgG к ацетилхолину, мышечно-специфической киназе, кроссовер рецептора LRP4 через плаценту.
Резюме
Тяжелая миастения – это аутоиммунное заболевание, характеризующееся связыванием аутоантител с рецепторами ацетилхолина в нервно-мышечном соединении постсинаптической мембраны и, как следствие, слабостью скелетных мышц.
Всех пациентов с миастенией следует разделить на подгруппы в соответствии с различными симптомами заболевания, и эта классификация определяет выбор тактики лечения.
Лечение первой линии для симптоматического лечения – пиридостигмин, а для иммуносупрессивного лечения – преднизолон с азатиоприном. Тимэктомия должна выполняться пациентам с миастенией, леченным тимомой.
Симптоматическое, иммуносупрессивное, хирургическое и поддерживающее лечение имеют очень хорошие эффекты, поэтому прогноз заболевания с точки зрения мышечной силы, функциональных возможностей, качества жизни и выживаемости хороший.
Миастения
Миастения – это патология, которая проявляется чрезмерной утомляемостью мускулатуры. В основе развития заболевания лежат аутоиммунные процессы, то есть выработка организмом антител против собственной ткани. Болезнь чаще всего возникает у молодых пациентов и без своевременной помощи врачей нередко приводит к глубокой инвалидизации и даже летальному исходу.

Общая информация
Любая мышца сокращается под влиянием нервного импульса. Он передается от нерва к мышечному волокну через специальное соединение, которое называется синапс. Во время прохождения импульса в нем выделяется большое количество ацетилхолина, который служит медиатором процесса. Повышение его концентрации приводит к возбуждению рецепторов мышцы и провоцируют сокращение волокна.
При миастении организм начинает активно вырабатывать антитела к рецепторам, реагирующим на повышение концентрации ацетилхолина. В результате они постепенно разрушаются, и качество реакции мышцы на возбуждение постоянно ухудшается. Чем интенсивнее работает мускулатура, тем заметнее снижается качество работы синапса. По мере прогрессирования патологического процесса разрушение захватывает все большее количество рецепторов, что может привести к полной потере способности к сокращению, т.е. параличу.
Причины возникновения
В настоящее время врачи и ученые не смогли найти точную причину развития миастении. Среди наиболее распространенных теорий, объясняющих биомеханизм развития заболевания, популярностью пользуется тимогенная. Считается, что антитела вырабатываются в тимусе (вилочковой железе). Она играет важную роль в формировании детского иммунитета, но по мере взросления подвергается обратному развитию вплоть до полной атрофии. У многих больных с миастенией обнаруживается увеличение вилочковой железы или опухоль в ее ткани, что говорит о высокой вероятности связи между этими патологиями.
Существует ряд факторов риска, которые повышают вероятность развития миастении:
Формы и симптомы
Врачи выделяют несколько форм миастении, которые отличаются друг от друга происхождением или особенностями течения. Причина и время появления специфического синдрома, характерного для нарушения нервно-мышечной проводимости, позволяют выделить две разновидности:
Среди практикующих врачей более востребована клиническая классификация миастении, которая позволяет выделить три основных формы.
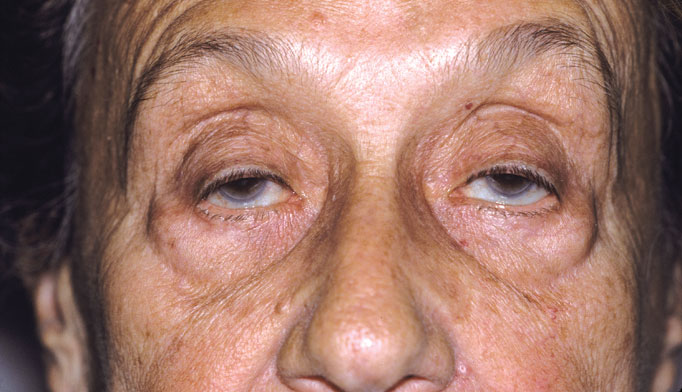
Глазная миастения
Поражение захватывает мышцы, расположенные в непосредственной близости от глазного яблока. Они отвечают за процесс открытия и закрытия глаз, их повороты в ту или иную сторону, а также настройку на близкое и дальнее расстояние. В результате пациент жалуется на:
Все симптомы становятся особенно яркими к вечеру на фоне утомления мускулатуры, а утром проходят полностью или частично.
Бульбарная миастения
В первую очередь страдают мышцы, ротовой полости, глотки, гортани, а также мимическая мускулатура. В результате у пациента существенно нарушается дикция, речь становится неразборчивой, а голос – гнусавым и хриплым. Во время жевания и глотания быстро нарастает усталость, что делает прием пищи нелегкой задачей.
Если в патологический процесс вовлекается мимическая мускулатура, мимика становится бедной и неестественной. У пациента возникают затруднения при попытке улыбнуться или оскалить зубы.
Генерализованная миастения
Эта форма заболевания встречается наиболее часто и характеризуется последовательным поражением мускулатуры всего тела. Сначала пациент начинает быстро уставать при ходьбе, а затем затрудняются движения, связанные с подъемом рук. Способность к передвижению и самообслуживанию постепенно ухудшается, что в конечном итоге приводит к инвалидизации пациента.
Все виды миастении характеризуются нарастанием симптоматики к вечеру. Это связано с физической активностью пациента в дневные часы и постепенным утомлением мышц. Чем тяжелее заболевание, тем быстрее возникают затруднения движений.
Диагностика
Миастения относится к неврологическим заболеваниям, вот почему при появлении любых подозрительных симптомов необходимо обратиться к неврологу. Нередко специалисту достаточно взглянуть на мимику и походку пациента, чтобы заподозрить патологию. Затем проводится подробный опрос, в ходе которого уточняются:
Затем врач проводит подробный осмотр с оценкой мышечного тонуса и силы, чувствительности отдельных частей тела, выраженности рефлексов. Как правило, этого хватает для постановки предварительного диагноза, который затем подтверждается объективными исследованиями:
Диагностика дополняется стандартными тестами: общий анализ крови, общий анализ мочи, электрокардиография и т.п. При необходимости список исследований расширяется.
Лечение миастении
В настоящее время врачи не имеют возможности полностью остановить процесс разрушения ацетилхолиновых рецепторов и избавить человека от симптомов миастении. Основное лечение направлено на остановку патологического процесса и достижение ремиссии, а также снижение утомляемости мускулатуры.
Основу терапии составляют средства, тормозящие работу иммунной системы: гормоны (преднизолон), цитостатики (циклоспорин), а также иммуноглобулины. Специфические препараты прозерин и калимин тормозят разрушение ацетилхолина, что позволяет увеличить его концентрацию в нервно-мышечном синапсе и, соответственно, улучшить передачу нервного импульса. Для ускорения процесса возбуждения используют препараты калия.
Специфическое лечение миастении дополняется общими средствами, в частности, антиоксидантами, стабилизирующими работу нервной системы. В зависимости от ситуации также назначаются лекарства, устраняющие побочные эффекты основных медикаментов.
При выявлении в ходе диагностики опухоли вилочковой железы проводится ее хирургическое удаление, иногда в сочетании с лучевой терапией. Показаниями к операции выступает неуклонное прогрессирование заболевания и его генерализованная форма у пациентов младше 70 лет. При идеальном результате после удаления тимуса человек практически полностью отказывается от медикаментов, а симптомы контролируются диетой и образом жизни.
При запредельно высокой концентрации антител в крови может назначаться ее искусственная очистка: плазмаферез, криофероз, иммуносорбция. Во время ремиссии проводятся курсы физиопроцедур (электрофорез, электромиостимуляция), массаж, санаторно-курортное лечение.
Осложнения
Главная опасность миастении – это миастенический криз. Как правило, это осложнение провоцируется самим пациентом, например, при самовольной отмене или замене препаратов, изменении их дозировки. Вызвать криз также могут острые инфекции, запредельные физические или психические перегрузки. В результате утомляемость мышц повышается до такой степени, что пациент не может встать с постели, принимать пищу и даже говорить.
При крайне тяжелом течении миастенического криза страдает также дыхательная мускулатура, обеспечивающая движения грудной клетки. Это состояние может стать причиной летального исхода, вот почему пациент экстренно госпитализируется в реанимационное отделение. Врачи проводят мероприятия, направленные на снижение количества антител, при необходимости человека подключают к аппарату искусственного дыхания.
Первые признаки надвигающегося миастенического криза включают:
В случае появления подобных симптомов необходимо как можно быстрее обратиться за медицинской помощью.
Профилактика
Специфической профилактики возникновения заболевания не существуют. Основные профилактические меры рассчитаны, в первую очередь, на людей, у которых уже имеется миастения, и направлены на предотвращение ухудшения. Необходимо следовать следующим правилам:
Диета
Важным аспектом профилактики миастении является соблюдение диеты. Ежедневный рацион должен быть сбалансированным по основным нутриентам (белкам, жирам, углеводам) и обладать достаточным, но не чрезмерным калоражем. Если у человека имеется избыток массы тела, рекомендуется придерживаться дефицита калорий (не более 10-15% от ежедневной нормы). В меню должны присутствовать продукты с высоким содержанием калия (картофель, бананы и т.п.). По назначению врача допускается прием поливитаминных препаратов.
Лечение в клинике «Энергия здоровья»
Миастения – это тяжелое заболевание, но врачи клиники «Энергия здоровья» имеют огромный опыт работы с такими пациентами. Это позволяет нам добиваться значительного улучшения состояния и стойкой ремиссии. Вот основные преимущества лечения в нашем медицинском центре:
Преимущества клиники
«Энергия здоровья» – это современный многопрофильный медицинский центр, оборудованный в соответствии с самыми строгими стандартами. Мы делаем все, чтобы каждый пациент получил максимально полную и эффективную медицинскую помощь вне зависимости от диагноза. К Вашим услугам:
Совсем недавно диагноз миастения звучал как приговор. Человек был по умолчанию обречен на летальный исход от постепенной парализации дыхательной мускулатуры. Современные методы лечения, хотя и не дают возможности полностью избавиться от патологии, но позволяют добиться стойкой ремиссии на долгие годы. Если Вы сами или Ваш близкий человек стали замечать беспричинную слабость мышц, особенно заметную в вечерние часы, не тяните с обращением к неврологу. Врачи клиники «Энергия здоровья» ждут вас!