Какими методами исследования можно предположить наличие гемофилии
Лабораторное исследование при гемофилии показывает:
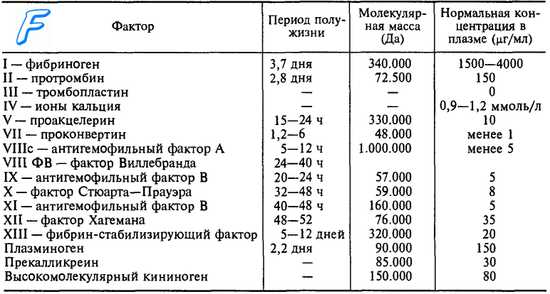
а) Тесты с нормальными результатами: число тромбоцитов, В.К., Т. тромбина, капиллярная резистентность, ретракция сгустка, Ф. VIII-Ag, Ф. VIII-vW и TQ. Из них, две пары тестов представляют чрезвычайную важность; число тромбоцитов и TQ, нормальность которых исключает из дифференциальной диагностики тромбопении и парагемофилии; уровни Ф. VIII-Ag, и Ф. VIII-vW, которые исключают болезнь фон Виллебранда.
б) Тесты с аномалийными результатами:
1) Т.Н., Р.Т.Т. и Р.Т.Т.К. значительно удлиненные. Чувствительность этих тестов повышается в порядке их перечисления, так что в легких случаях выделяется лишь Р.Т.Т. и Р.Т.Т.К., а в стертых формах лишь Р.Т.Т.К.
2) Т.E.G. показывает трассу со значительно удлиненными «r» и «к» и с нормальным «ma».
3) TGT — характерный тест, подтверждающий диагноз болезни и устанавливающий одновременно ее типологию: глобально, он удлинен при обоих типах гемофилии; плазматическое TGT удлиненное и сывороточное TGT нормальное указывает на гемофилию типа А; плазматическое TGT нормальное и сывороточное TGT удлиненное указывает на гемофилию типа В.
4) Определение уровня Ф. VIII или IX устанавливает степень суровости данной гемофилии (А или В).
5) Т.С.Р. всегда очень сокращенный.
6) Дозирование плазматического фибриногена дает либо нормальные, либо слегка повышенные цифры. Речь идет об умеренном гиперинозе, характерном для большинства гемофиликов.
7) T.L.C.E. нормальный или сокращенный; последняя возможность является часто реакцией на гипериноз и встречается главным образом у гемофиликов с повышенным фибриногеном.
Положительный диагноз гемофилии основывается с клинической точки зрения на обследовании существующего в данный момент состояния, обследование, которое объективирует острый геморрагический синдром, выраженный в одном из проявлений, приведенных нами в разделе симптоматологии.
Анамнез выявляет аномалийные, ранние и повторные кровотечения по поводу незначительных травм, с преобладающе суставными или мышечными явлениями. Гередоколлатеральное прошлое больного показывает заболеваемость только по мужской линии и передаваемость по женской линии.
Лабораторные исследования превращают предположение гемофилии в уверенность на основании вышеуказанных тестов. Дифференциальная диагностика производится по отношению к следующим заболеваниям: тромбопении, гемофилоидные синдромы, гипопротромбинемия, парагемофилии, болезнь фон Виллебранда и афибриногенемия; выделение при помощи специфических лабораторных тестов дефицитного фактора окончательно решает диагноз.
Следует упомянуть по этому поводу и о диагнозе носительниц гемофилического порока. Семейный опрос позволяет сгруппировать их в две категории: непременные и вероятные. Первые являются матерями, имеющими: либо 2 сыновей гемофиликов, либо одного сына гемофилика и одного члена семьи по боковой линии гемофилика (племянника, двоюродного брата от тетки по матери), либо, наконец, являются дочерями отца гемофилика.
Вторыми, вероятными, являются матери одного сына гемофилика или с одним родственником по боковой линии гемофиликом. (Вероятно они родительницы случаев «de novo»).
Их максимально достоверное выявление (в особенности вероятных носительниц) имеет важнейшее значение для профилактики гемофилии. Статистики крупнейших гематологических клиник мира показывают, что непременные носительницы не нуждаются в лабораторном исследовании, так как уже найдено стопроцентное подтверждение. Что касается вероятных носительниц, биологическое исследование дает положительные результаты в вариабильных процентнах в зависимости от использованных для выявления тестов. Так (для гемофилии А):
— На основании определения ф. VIII—С 60—65%
— На основании определения Ф. VIII—С/Ф. VIII—Аe 78—85%
— На основании определения фактора VIII-C/Ф.VIII-Ag с линейной дискриминацией 90%
Что касается носительниц гемофилического порока В, цифры несколько ниже, но с клинической точки зрения они представляют клинические проявления (различные кровотечения) намного чаще, чем носительницы гемофилического порока А.
В этой же связи следует рассматривать и диагноз появления ингибиторов (антител). Их появление наблюдается чаще при гемофилии А, чем при гемофилии В и является опасным осложнением подымающим серьезные терапевтические проблемы. Речь идет о появлении антитела-гомолога, нейтрализирующего действия на Ф. VIII—С (соответственно Ф. IX—С), со структурой типа IgG с легкими цепями. Частота его появления вариабильная от одной статистики к другой. Напр:, в США = 16%, в Канаде = 12%, в Западной Европе = 5%.
Риск появления антител чрезвычайно вариабильный; полученные до сих пор конкретные данные показывают следующее:
— Не существует никакого абсолютного семейного основания, хотя нельзя отрицать некоторую конституционную тенденцию в этом отношении.
— Не сучествует никакой связи с системой HLA; скорее, в рамках классических групп крови, весы склоняются в сторону группы АВ (IV).
— Возраст больных имеет некоторое значение: группы 1—5 лет и группы старше 40 лет наиболее уязвимы.
— Критической является не доза применяемого антигемофилического препарата, а большая продолжительность лечения.
— Клинические типы суровой и среднесуровой гемофилии имеют большую частоту (18%) по сравнению со средними и легкими (2%).
— Степень очищенности антигемофилического фактора, используемого в лечении прямо пропорциональна частоте появления ингибиторов; менее чистые препараты индуцируют меньший антителовый ответ.
Методология выделения появившихся ингибиторов развертывается в двух фазах:
— Качественная проба. Основывается на тесте РТТК. Определяется его значение у нормального контроля, у больного и смеси 1/1 плазмы обоих вышеуказанных лиц. Если значение РТТК этой смеси приближается к нормальному (макс, отклонение + 25%), тогда проба является отрицательной и значит больной не имеет ингибиторов. Если значение РТТК этой смеси ближе к значению РТТК больного (макс, отклонение—25%), это означает наличие ингибиторов, и следовательно проба является положительной; затем мы переходим к следующей фазе.
— Количественная проба. Это титрирование, в котором используется также техника РТТК, в виде группы серийных определений, в десятичных дилюциях Ф. VIII, соответственно Ф. IX. Дилюат — плазма больного, дилюент — плазма нормального контроля. Результат выражается в единицах Bethesda/мл. плазмы. На результатах этой пробы строится схема лечения больного.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Диагностика гемофилии
Диагностика заболевания начинается со сбора личного и семейного анамнеза, а также выявления признаков геморрагического синдрома.
Скрининговые лабораторные исследования
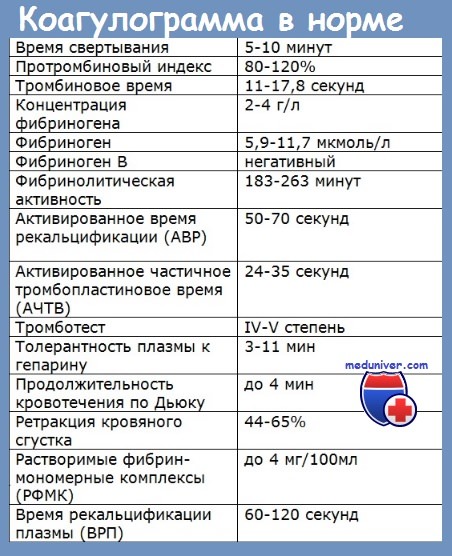
При выполнении скрининга используются такие тесты, как подсчет тромбоцитов, время кровотечения (напр. по Ivy), ПВ, АЧТВ, концентрация фибриногена. Необходимо учесть, что при легких формах гемофилии в результатах скрининговых тестов может не обнаружиться значимых изменений, даже при наличии клинической симптоматики. Для данной группы пациентов показано количественное определение активности факторов свертывания.
При удлинении времени свертывания назначаются корректировочные тесты (микс тесты, тесты смешивания) для дифференцировки истинной гемофилии от влияния ингибитора.
1 АЧТВ удлинено в отдельных случаях, степень удлинения зависит от выраженности дефицита и от чувствительности реагента к фактору VIII/ IX.
2 При смешивании равных объемов плазмы пациента и пула нормальной плазмы удлинение АЧТВ может быть скорректировано.
Специализированные тесты
Дифференциальная диагностика
Для постановки корректного диагноза важно учитывать возможность наличия других заболеваний, связанных с дефицитом факторов свертывания. Дифференциальная диагностика состоит в исключении других причин геморрагического синдрома и удлинения АЧТВ.
Редко встречающиеся дефициты факторов свертывания
Комбинированный дефицит ф.VIII и ф.V является редкой патологией (один случай на 1 000 000), однако его фактическая распространенность гораздо выше, чем теоретическая. Данное нарушение вызвано мутацией в генах [чаще ERGIC (также известный как LMAN1), реже MCFD2], кодирующих транспортные белки, которые участвуют во внутриклеточном транспорте факторов VIII и V, и обычно приводит к умеренному снижению факторов VIII и V (от 5 до 20%).
Лабораторная диагностика основывается на одновременном выявлении удлинения времени свертывания в тестах АЧТВ и ПВ с дальнейшим определением активности ф.V. Рекомендуется определять уровень активности ф.VIII минимум один раз у всех пациентов с выявленным дефицитом ф.V, чтобы не пропустить данную патологию.
Антитела к факторам свертывания
Появление ингибиторов нередко наблюдается у пациентов, получающих заместительную терапию факторами свертывания. Наличие ингибиторов следует предполагать у пациентов с низкой эффективностью использования заместительной терапии.
Приобретенная гемофилия связана с присутствием антител к фактору у пациентов, не имеющих мутантного гена гемофилии. Это редкое заболевание может возникнуть, в частности, у женщин во время беременности, у пациентов с аутоиммунными заболеваниями, а также у пожилых пациентов. Наиболее частым клиническим проявлением являются выраженные гематомы.
Наличие ингибиторов к факторам свертывания крови должно быть подтверждено лабораторными исследованиями.
Определить наличие ингибиторов в плазме крови можно на основании теста смешивания.
Тест смешивания:
Диагностика специфических ингибиторов факторов свертывания включает определение АЧТВ методом Bethesda или Nijmegen.
Тип 2N болезни Виллебранда
Дефицит витамина К
В связи с тем, что ф.IX является витамин К-зависимым фактором свертывания, наблюдается снижение его уровня при дефиците витамина К или назначении АВК препаратов. При данной патологии наблюдается комбинированное снижение витамин-К зависимых компонентов свертывания (ф. X, IX, VII, II, а также протеинов С и S).
— «Что такое ингибиторы?» World Federation of Hemophilia, 2010
Как диагностировать гемофилию?
Гемофилия представляет группу наследственных заболеваний, которые характеризуются патологическим кровотечением. В основе заболевания лежит дефект гена, отвечающего за синтез фактора свертывания крови. Всего существует 13 факторов свертывания крови. Вместе с тромбоцитами эти факторы обеспечивают свертывание крови, что является физиологической реакцией в ответ на повреждение и нарушение целостности кожного покрова. Нехватка одно из факторов свертывания, нарушает процесс гемокоагуляции, что приводит к длительным неостанавливающимся кровотечениям. Именно они свойственны гемофилиям. В зависимости от дефицита фактора VIII, IX, XI развиваются гемофилия А, В и С соответственно.
Типы гемофилии
Наиболее часто встречаются гемофилия типа А и В. Гемофилия C имеет самую низкую частоту. Заболевание проявляется на протяжении всей жизни и манифестирует в раннем возрасте. Мальчики болеют чаще, чем девочки, частота встречаемости 1 случай на 5000, что связано с особенностями типа наследования заболевания.
Причина заболевания
Гемофилия А и В является генетическим заболеванием и наследуется по Х-связанной рецессивной генетической схеме. Патологичный ген на Х-хромосоме проявляется только тогда, когда нет нормального гена. У женщин две Х-хромосомы, в то время как у мужчин одна. Мужчин болеют всегда, когда присутствует один дефектный ген на X-хромосоме; женщины страдают от недуга, когда дефектный ген присутствует на обеих Х-хромосомах. Те женщины, у которых есть только один измененный ген гемофилии являются здоровыми носителями и не болеют.
Гемофилия названа королевской болезнью или царской, поскольку часто встречалась среди царских и королевских дворов в предыдущие века. В основном, этот феномен связан с частыми близкородственными браками того времени.
Полностью вылечить данное заболевание достаточно сложно. Поэтому очень важно чтобы люди, страдающие гемофилией, соблюдали меры предосторожности, которые бы помогали не усугубить им свое положение. В первую очередь необходимо навсегда отказаться от внутримышечных инъекций, так как они могут привести к резким кровоизлияниям в мягкие ткани. Именно поэтому все возможные препараты нужно принимать только внутривенно или перорально. Больным гемофилией нужно очень внимательно подходить к выбору лекарственных средств, и исключить аспирин и ибупрофен.
Врачи рекомендуют придерживаться диеты: употреблять продукты питания, которые содержат много кальция и витаминов.
Гемофилия
Гемофилия – наследственная патология гомеостаза, проявляющаяся в нарушении свертывания крови на фоне сниженного синтеза необходимых веществ организмом пациента (факторов VII, IX, XI). Страдающие от заболевания лица регулярно находят на своем теле гематомы или сталкиваются с гемартрозами, внутренними кровотечениями на фоне травм или хирургических вмешательств. Лечение гемофилии у детей строится на заместительной терапии, которую необходимо получать на протяжении всей жизни.
Причины развития патологии
Механизм и тип наследования гемофилии изучены достаточно подробно. Гены, провоцирующие недостаточную выработку факторов свертывания крови, сцеплены с Х-хромосомой. Патология наследуется по рецессивному признаку по женской линии. Наследственно обусловленная патология встречается исключительно у мальчиков.
Сыновья здорового мужчины и женщины-носительницы патологического гена с одинаковой вероятностью могут родиться без признаков гемофилии или с ними. Мужчина, страдающий от нарушений свертывания крови, сможет зачать здоровых детей с женщиной, не являющейся носительницей измененного гена.
Медицине известны единичные случаи обнаружения гемофилии у женщин. Их матери были носительницами мутировавшего гена, а отцы страдали от недостаточной выработки факторов свертывания крови. Причинами гемофилии в подобных случаях становится соединение рецессивного и доминантного генов.
Классификация заболевания
Виды гемофилии выделяются на основании дефицита определенного фактора свертываемости крови в организме пациента. Основные сведения о типах заболевания представлены в таблице.
Диагностируется у 84-86% людей, страдающих от рассматриваемой патологии. Вызван дефицитом VIII фактора свертываемости (антигемофильного глобулина).
Занимает долю в 12-13% от клинически диагностируемых случаев гемофилии. Развивается на фоне дефицита IX фактора свертываемости (тромбопластина)
Встречается не чаще 1-2%. Становится следствием недостаточной выработки XI фактора свертывания крови.
Около 0,5% выявляемых случаев гемофилии различной этиологии относятся к иным типам – V, VII, X и другим.
Симптомы гемофилии
Первые признаки патологии можно обнаружить у новорожденных детей. Так, на вероятность подтверждения диагноза «гемофилия» у ребенка укажут длительное кровотечение из пуповины и многочисленные подкожные гематомы. Обильное истечение крови у младенцев в момент прорезывания зубов становится не менее тревожным фактором. Но в период лактации ребенок получает достаточное количество тромбокиназы с молоком матери.
Посттравматические кровотечения характерны для детей, научившихся ползать и ходить. К носовым кровотечения добавляются межмышечные гематомы и кровоизлияния в суставы (гемартрозы). На фоне этого развивается анемия.
С возрастом дети могут столкнуться с истечением крови из органов ЖКТ. Причиной этого становятся травмы или медицинские манипуляции. Наибольшую опасность представляют кровотечения из носоглотки и зева. На их фоне может развиться обструкция дыхательных путей.
Диагностика патологии
Диагностические процедуры выполняются врачами нескольких специализаций: неонатологом, педиатром, генетиком и гематологом. При сопутствующих патологиях могут потребоваться консультации с гастроэнтерологом, ортопедом, отоларингологом и неврологом.
Семейным парам из группы риска следует посетить врача до зачатия ребенка. Молекулярно-генетическое исследование биоматериалов будущих родителей позволит учесть риск рождения ребенка с гемофилией. После зачатия возможно выполнение пренатальных скринингов. Их результаты подтвердят или опровергнут факт наследования гемофилии ребенком.
Неонатальные тесты, выполняемые в первые дни жизни малыша, оказываются не менее эффективности. Коагулограмма дает неонатологу исчерпывающие сведения о продуцировании факторов свертываемости организмом новорожденного.
При гемартрозах ребенку назначается рентгенографическое исследование суставов. Ультразвуковая диагностика выполняется при обнаружении признаков внутренних кровотечений и забрюшинных гематом.
Лечение заболевания
Терапевтические мероприятия на фоне лечения гемофилии относятся к одной из двух групп – профилактическим или симптоматическим. В первом случае пациент с тяжелой формой патологии получает регулярные дозы концентратов факторов свертывания крови. Их присутствие снижает риск развития артропатии и внутренних кровотечений. При планировании оперативных вмешательств (включая удаление зубов) пациент получает повторные трансфузии препаратов.
Симптоматические процедуры выполняются при порезах и наружных кровотечениях. Врачи рекомендуют использовать гемостатическую губку и накладывать давящую повязку. Мелкие раны следует обрабатывать тромбином.
Прогноз
Заместительная терапия позволяет организму пациента выработать достаточное количество антител, которые блокируют прокоагулянтную активность. Дополнительными мерами поддержания мальчиков или мужчин становится плазмаферез и прием иммунодепрессантов. На фоне регулярных переливаний крови и плазмы пациенты могут столкнуться в ВИЧ, гепатитом, герпесом или цитомегаловирусом.
Легкая степень гемофилии не оказывает существенного влияния на качество и продолжительности жизни пациентов. При тяжелых формах патологии прогноз выживаемости существенно ухудшается. Клинические рекомендации при гемофилии предусматривают регулярные консультации пациентов с гематологом и контроль показателей свертываемости крови посредством лабораторных тестов.
Статистика
Гемофилия относится к наследственным коагулопатиям – причина развития заболевания обусловлена особенностями генетического материала матери и отца ребенка. В Москве патология типов A и B выявляется с частотой 1 случай на 10000 и 50000 новорожденных мальчиков соответственно. Симптомы заболевания диагностируются в раннем возрасте в ходе осмотра младенца неонатологом или педиатром.
Вопросы и ответы
Можно ли полностью излечиться от гемофилии?
Медикаментозная терапия и манипуляции по переливанию крови или плазмы купируют острые синдромы патологии. Иногда пациентам назначается длительный прием препаратов, подобранных с учетом данных анамнеза. Но полное устранение симптомов гемофилии по-прежнему остается невозможным.
Несет ли гемофилия угрозу жизни ребенка?
При своевременном обращении родителей за медицинской консультацией малыш окажется вне опасности. Быстрая постановка правильного диагноза и начало лечения позволят ребенку не ограничивать себя в двигательной активности и играх.
Может ли мальчик, болеющий гемофилией, передать ее своим сыновьям?
Риск рождения детей с гемофилией от отца, испытывающего проблемы со свертыванием крови, минимален. Заболевание будет унаследовано сыновьями только в том случае, если их мать входит в число носителей измененного гена.
Существует ли эффективный механизм профилактики гемофилии?
Нет, такого механизма не существует. Но будущие родители могут пройти скрининги, которые определяет вероятность рождения страдающего от недостаточной свертываемости крови ребенка.
Диагностика и лечение гемофилии
Общая информация
Краткое описание
КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ по ДИАГНОСТИКЕ И ЛЕЧЕНИЮ ГЕМОФИЛИИ
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Таблица 1. Классификация гемофилии по степени тяжести
Около 60-70% всех диагностированных случаев гемофилии составляют тяжелые формы заболевания, для которых характерны спонтанные геморрагические эпизоды (преимущественно гемартрозы и гематомы мягких тканей различных локализаций). Степень тяжести нарушений свертывания крови и клинических проявлений при гемофилии зависит, как правило, от уровня активности фактора в крови, однако в клинической практике не всегда существует прямая корреляция между лабораторным и клиническим фенотипами заболевания [2, 3].
Клиническая картина
Cимптомы, течение
Таблица 2. Клинические проявления гемофилии
Диагностика
При сборе анамнеза заболевания и семейного анамнеза пациента рекомендуется выяснять наличие проявлений геморрагического синдрома: жалоб на легко появляющиеся экхимозы и гематомы в раннем детстве; возникновение спонтанных кровотечений (особенно в суставы, мышцы и мягкие ткани); длительных кровотечений после травм или хирургического вмешательства [3].
Данные семейного анамнеза примерно у 2/3 больных содержат указания на геморрагические проявления у близких родственников по материнской линии (у мужчин, реже у женщин). Данные персонального анамнеза могут содержать информацию о геморрагических проявлениях у пациента. При сборе анамнеза заболевания необходимо обращать внимание на наличие геморрагических проявлений в неонатальном периоде в виде кефалогематом, внутричерепных кровоизлияний, кровоточивости и длительном заживлении пупочной ранки; у грудных детей – экхимозов, не связанных со значимой травмой, гематом мягких тканей после незначительных ушибов или спонтанных. У некоторых детей кровотечения могут отсутствовать на первом году жизни до тех пор, пока ребенок не начнет ходить [2]. Важно обращать внимание на несоответствие выраженности геморрагических проявлений тяжести предшествовавшей травмы, на рецидивы кровотечений после первичной остановки, не связанные с повторной травмой, массивные и (или) множественные гематомы, системность геморрагических проявлений (проявления различной локализации), «спонтанные геморрагические проявления». При легкой форме гемофилии кровотечения могут отсутствовать до первой травмы или хирургического вмешательства. Сбор жалоб и анамнеза позволит определить объем обследования пациента.
При проведении физикального осмотра рекомендуется обращать внимание на наличие кожного геморрагического синдрома различной выраженности в виде множественных экхимозов и гематом, возможных при тяжѐлой и среднетяжелой форме гемофилии [4]. Высоковероятно выявление признаков поражения суставов в виде деформации, отека и локального повышения температуры кожи (острый гемартроз) и/или признаков нарушения подвижности, объема движений суставов, гипотрофии мышц конечности на стороне поражѐнного сустава, нарушение походки (деформирующая артропатия).
Диагноз устанавливается при наличии как минимум двух из трех критериев.
Инструментальная диагностика позволяется визуализировать кровотечения/кровоизлияния различных локализаций, а также выявить осложнения, развившиеся вследствие геморрагических проявлений. По показаниям проводятся следующие обследования:
эзофагогастродуоденоскопия;
Лечение
Рекомендуется отдавать предпочтение тому препарату, который при равной эффективности лучше всего переносится пациентом, имеет лучшие фармакокинетические индивидуальные показатели и наиболее удобен в использовании, исходя из конкретных условий [4, 7, 9]. Смена МНН у конкретного пациента при отсутствии зарегистрированных нежелательных явлений на введение используемого препарата и удовлетворительном клиническом ответе на терапию возможна после 100 экспозиционных дней введения концентратов факторов свертывания крови.
Существует два вида специфической терапии – лечение по факту возникновения кровотечений (по требованию) и профилактическая терапия [4].
Таблица 3. Рекомендуемые уровни фактора и продолжительность терапии при различных видах кровотечений 
Расчет дозы концентрата FVIII у пациентов старше 1 года проводится следующим образом: доза (МЕ) = масса тела (кг) х (требуемая активность – базальная активность) х 0,5.
Учитывая вариабельность фармакокинетических показателей у каждого конкретного пациента заместительная терапия требует клинического и, при необходимости, лабораторного контроля. Клинический контроль должен проводиться гематологом при обращении пациента, родителями и самим пациентом постоянно. В основе клинического контроля лежит оценка динамики геморрагических проявлений и ее сопоставление с проводимой заместительной терапией. Лабораторный контроль включает определение активности дефицитного фактора в крови, тест восстановления, оценку фармакокинетической кривой (с расчетом периода полувыведения). Для оценки результативности гемостатической терапии возможно проведение интегральных тестов: тромбоэластография, тест генерации тромбина, тромбодинамика в динамическом наблюдении [8].
Таблица 4. Виды профилактики при гемофилии

** Переход к следующему шагу при развитии спонтанного гемартроза.
При клиническом контроле решение о недостаточной эффективности профилактической терапии принимается в следующих случаях: более двух эпизодов спонтанных гемартрозов в год, появление признаков хронического синовиита или артропатии, возникновение спонтанных геморрагических проявлений другой локализации. Лабораторный контроль заключается в определении остаточной активности фактора перед следующим введением (должна быть не ниже 1%), контроле наличия ингибитора, и, по возможности, в проведении фармакокинетического исследования [12].
При наличии клинических или лабораторных данных о неэффективности профилактической терапии принимается решение о повышении дозы или кратности введения препарата. Учитывая, что основная задача профилактической заместительной терапии – сохранение качества жизни пациента, у пациентов с высоким уровнем физической активности допустимо повышение стандартных доз или увеличение кратности введения препарата.
Особенности проведения гемостатической терапии в зависимости от локализации кровотечения
Реабилитационные мероприятия и ЛФК целесообразно начинать после прекращения болевого синдрома с учетом состояния места повреждения. Если пациент не получает постоянное профилактическое лечение, после купирования кровотечения показана кратковременная профилактика, особенно на время реабилитации [4, 6, 9].
После кровоизлияния в ЦНС рекомендована обязательная профилактическая терапия в течение 3—6 месяцев.
Помимо заместительной терапии, рекомендовано соблюдение постельного режима и проведение гидратации (3 л/м2) в первые 48 часов. Не рекомендуется применение ингибиторов фибринолиза. Дополнительное возможно назначение преднизолона. Пациентам, у которых развилось почечное кровотечение, необходимы консультация уролога и урологическое обследование. [3, 4, 8, 14]
При тяжелой форме гемофилии появление ингибитора не влияет на количество и локализацию кровотечений. Но поскольку при появлении ингибиторов заместительная терапия факторами становится неэффективной, риск тяжелых осложнений и даже смерти от кровотечения у этих больных выше.
При ингибиторной ГВ до 50% пациентов могут иметь тяжелые аллергические реакции, в том числе анафилаксию, при применении FIX. Такие реакции часто бывают первым симптомом развития ингибитора [15].
Подтверждение наличия ингибитора и определение его титра выполняется в коагулологической лаборатории. У детей оценка наличия ингибитора должна проводиться каждые 5 дней первые 20 ДВ, каждые 10 дней с 21 до 50-й ДВ, а затем не менее 2 раз в год до 100 ДВ. У пациентов с более чем 100 ДВ препарата оценка наличия ингибитора должна проводиться 1 раз в год и дополнительно в следующих ситуациях: снижение эффективности заместительной терапии факторами при введении адекватных доз, появление или увеличение количества кровотечений на профилактической терапии, отсутствие достаточного повышения уровня фактора в крови после введения препарата. Кроме того, диагностика ингибитора также должна проводиться в следующих ситуациях:
— при смене препарата (через 10-20 ДВ и через 6 месяцев терапии);
— перед хирургическими вмешательствами и после операции при отсутствии адекватного повышения уровня фактора в крови после введения препарата;
— через 4 недели после окончания проведения интенсивной терапии.
Существуют различные протоколы проведения ИИТ (табл.6). Оптимального режима проведения ИИТ нет. Для пациентов с высокореагирующим ингибитором, независимо от титра ингибитора на момент начала ИИТ, рекомендована начальная схема 100 – 150 МЕ/кг FVIII каждые 12 часов. Для пациентов с низкореагирующим ингибитором рекомендовано начинать ИИТ по схеме 50 – 100 МЕ/кг FVIII ежедневно или каждый второй день.
Таблица 6. Протоколы проведения ИИТ
Таблица 7. Критерии эффективности ИИТ
Опыт проведения ИИТ у пациентов с ингибиторной ГB ограничен. Это обусловлено очень низкой эффективностью и наличием аллергических реакций.
У большинства пациентов с гемофилией вследствие рецидивирующих гемартрозов формируются различные повреждения опорно-двигательного аппарата.
Диагностика включает выявление клинических признаков, УЗИ и/или МРТ суставов. Терапия проводится совместно с ортопедами, имеющими опыт лечения больных гемофилией. При сохранении признаков воспаления показана терапия нестероидными противовоспалительными препаратами (ингибиторами COX-2).
При недостаточной эффективности заместительной терапии возможно проведение курса пункций сустава с введением стероидных противовоспалительных препаратов (на первом этапе); далее вариантами выбора являются химическая или эндоскопическая синовэктомия, а при их недостаточной эффективности – хирургическая коррекция.
Основой профилактики развития хронической артропатии является адекватная постоянная профилактическая заместительная терапия. Своевременное лечение синовиита также необходимо для предотвращения развития артропатии. Диагностика артропатии основана на выявлении клинических признаков и на результатах инструментальных исследований: УЗИ, КТ, МРТ [8].
Целью лечения уже развившейся хронической артропатии является улучшение функционирования сустава и уменьшение болевого синдрома. Для борьбы с болевым синдромом оптимально использовать ингибиторы COX-2. Для восстановления функции сустава, состояния мышц проводят курсы ЛФК и физиотерапии. В ряде случаев эффективно использование тренажеров. На начальных этапах восстановительного лечения показано проведение курсов препаратов гиалуроновой кислоты. При недостаточной эффективности консервативной терапии показано хирургическое лечение, которое должно проводиться врачами, имеющими опыт лечения пациентов с гемофилией.