Успешное применение метотрексата при прогрессирующей эктопической беременности: пересмотр взглядов
Цель
Цель этого исследования состояла в том, чтобы определить успешность применения метотрексата при прогрессирующей эктопической беременности и соотнести его с уровнями -ХГЧ.
Ход исследования
Это ретроспективное когортное исследование, выполненное в медицинском центре третичного филиала университета, включало женщин, у которых была диагностирована эктопическая беременность между январем 2001 и июлем 2013. Таким женщинам производилось ежедневное измерение уровня -ХГЧ, чтобы определить прогрессию эктопической беременности. Женщинам с гемодинамически стабильным прогрессированием эктопической беременности был назначен метотрексат (50 мг/м2 поверхности тела). Мы исследовали случаи успешного и неудачного применения метотрексата в корреляции с уровнем -ХГЧ.
Результаты
Кандидатами были 1083 женщины для «внимательного наблюдения» (диспансерное ежедневное измерение -ХГЧ). Спонтанное обнуление или снижение уровня -ХГЧ случились у 674 пациенток (39,5%); 409 женщин (24%) имели стабильный или возрастающий уровень -ХГЧ и были пролечены метотрексатом. У 356 женщин (87%) лечение было успешным; 53 женщинам (13%) потребовалась лапароскопическая тубэктомия. Сравнивая с немедленным назначением метотрексата, действия соответственно нашим протоколам привели к меньшему снижению уровня -ХГЧ у женщин с прогрессирующей эктопической беременностью: 75% женщин с уровнями -ХГЧ в 2500/3500 мМЕ/мл и 65% женщин с уровнем -ХГЧ более 4500мМЕ/мл. Была найдена математическая модель, описывающая снижение успешного применения метотрексата в корреляции с -ХГЧ.
Заключение
Успешность применения метотрексата при прогрессирующей внематочной беременности после диспансерного наблюдения за уровнем -ХГЧ, оказалась гораздо ниже, чем сообщалось раньше. Это может быть причиной избыточного назначения метотрексата в случаях, когда эктопическая беременность в конце концов будет разрешена спонтанно.
Ключевые слова
ХГЧ, эктопическая беременность, метотрексат
Methotrexate success rates in progressing ectopic pregnancies: a reappraisal
Aviad Cohen, MD, Liat Zakar, MD, Yaron Gil, MD, Jonia Amer-Alshiek, MD, Guy Bibi, MD, Benny Almog, MD, Ishai Levin, MDemail
Необходимость контрацепции у женщин с ревматоидным артритом, получающих метотрексат

«Показатели индуцированного аборта были ниже у женщин с ревматоидным артритом (РА), получавших метотрексат, по сравнению с не получавшими это лечение женщинами, но все еще достаточно высокими, чтобы вызывать обеспокоенность», считает д-р Evelyne Vinet и ее соавт. из отделения клинической эпидемиологии и ревматологии в McGill University Health Centre (Монреаль, Канада), выполнивших исследование, результаты которого опубликованы на сайте журнала Arthritis Care & Research.
Авторы ожидали получить более высокий уровень искусственных абортов среди женщин, получавших метотрексат, таким образом, результаты были в некотором смысле неожиданными. «Это может быть связано с тем, что женщины были предупреждены о потребности в надежной контрацепции и/или заболевание было настолько серьезным/активным, что снижалась их сексуальная активность», полагает д-р Sasha Bernatsky, соавтор этого исследования в своем интервью Medscape Medical News.
Авторы выполнили исследование методом случай-контроль на основании базы данных госпитализации женщин для искусственного прерывания беременности с 1996 до 2008 в г. Квебеке у женщин в возрасте между 15 и 45 годами. Воздействие метотрексата учитывалось при назначении препарата за ≤ 16 недель до даты аборта.

Хотя уровень искусственного прерывания беременности у женщин с РА, получавших метотрексат, был в два раза ниже, чем у схожих женщин, не получавших этого лечения, «для них был характерен слишком высокий показатель незапланированных беременностей», что отражает недостаточную информированность в отношении необходимости контрацепции.
Mетотрексат является антагонистом фолиевой кислоты (ингибитором фермента дигидрофолат редуктазы) и обладает тератогенными свойствами, связанными с так называемым «фетальным аминоптериновым синдромом», включающим скелетные аномалии, микроцефалию и гидроцефалию (прим. перевод. нельзя забывать, что адекватный фолатный статус в критический период времени (в течение первых 28 дней после зачатия) служит профилактикой дефектов нервной трубки и способствует улучшению здоровья будущего потомства (например, снижает риск аутизма).
«Мать-природа «помогает» многим женщинам с РА, как только у них наступает беременность», отметил независимый эксперт Nathan Wei, являющийся президентом и генеральным директором Центра по лечению Артрита (Arthritis Treatment Center, Frederick, штат Мэриленд, США) в своем интервью Medscape Medical News. «Примерно у 80 % женщин с РА при наступлении беременности сразу наступает спонтанная ремиссия по не ясным до конца причинам. К сожалению, после родов опять возникает обострение заболевания. Мы рекомендуем пациенткам прекращать лечение метотрексатом в течение, по крайней мере, 3 месяцев прежде, чем они попытаются забеременеть вследствие тератогенных свойств этого препарата».
Источник:
Évelyne Vinet et al. Induced abortions in women with rheumatoid arthritis on methotrexate. Arthritis Care Res. Published online April 16, 2013.
Репродуктивная функция у женщин с ревматоидным артритом: влияние заболевания и терапии метотрексатом на уровень антимюллерова гормона
1 ФГБУ «Национальный медицинский исследовательский центр акушерства, гинекологии и перинатологии им. академика В.И. Кулакова» Министерства здравоохранения России, Москва, Россия;
2 ФГБНУ «Научно-исследовательский институт ревматологии им. В.А. Насоновой» Министерства науки и высшего образования Российской Федерации, Москва, Россия
Цель. Оценить овариальный резерв на основании показателя антимюллерова гормона – основного маркера овариального резерва у пациенток с ревматоидным артритом (РА) и бесплодием, получавших и не получавших терапию метотрексатом (МТХ).
Материалы и методы. В наблюдательное исследование были включены 72 пациентки с бесплодием, из которых 32 – больные РА, составившие основную группу, и 40 пациенток с бесплодием группы сравнения. Больные РА были стратифицированы на подгруппы в зависимости от наличия терапии МТХ. Оценивали влияние длительности и степени активности РА, а также длительности, дозы и возраста начала приема МТХ на уровень АМГ.
Результаты. Было показано статистически значимое снижение уровня АМГ у больных РА при сравнении с пациентками с бесплодием, а терапия МТХ была ассоциирована со снижением овариального резерва. Не было получено статистически значимой разницы в уровне АМГ в зависимости от длительности и степени активности основного заболевания, а также суммарной дозы и длительности терапии МТХ.
Выводы. Пациентки с РА имеют более низкие показатели АМГ. Прием МТХ ассоциируется с более выраженным снижением уровня АМГ. Возраст начала приема препарата отрицательно коррелирует со значением АМГ.
Большинство аутоиммунных заболеваний манифестирует у пациенток репродуктивного возраста, и многие женщины данной группы сталкиваются с проблемами в реализации репродуктивной функции. Ревматоидный артрит (РА) является одним из наиболее распространенных аутоиммунных заболеваний во всем мире. В России, по данным эпидемиологических исследований, РА страдают около 800 тысяч человек [1]. Известно, что около трети пациенток с РА, диагностированным до наступления первой беременности, имеют сниженную фертильность [2]. В исследовании Clowse M. et al. (2012) по оценке репродуктивной функции у женщин с РА и системной красной волчанкой (СКВ) было установлено, что 55% женщин с РА и 64% – с СКВ имели меньше детей, чем планировали изначально [3]. О снижении фертильности у женщин с ревматическими заболеваниями, в частности с РА, сообщалось в ряде публикаций 2011–2016 гг. [4, 5].
Следует отметить, что у пациенток с РА зафиксирован более длительный период до наступления первой беременности по сравнению со здоровыми женщинами [5]. Отрицательное влияние на функционирование репродуктивной системы может оказывать как само аутоиммунное заболевание, так и лекарственная терапия [6].
Отрицательное влияние течения РА, а также проводимой терапии на репродуктивную функцию может быть обусловлено следующими механизмами.
Наряду с НПВП и глюкокортикоидами, многие пациенты в качестве базисной терапии получают метотрексат (MTX) – цитотоксический препарат, относящийся к группе антиметаболических средств. MTX оказывает негативное влияние на быстро делящиеся клетки, к которым можно отнести клетки ткани яичника и эндометрия. Повреждение этих клеток, будь то временное или постоянное, способно повлиять на фертильность, особенно у женщин с уже скомпрометированной репродуктивной функцией на фоне течения основного заболевания и/или в связи с приемом других препаратов и сопутствующей гинекологической патологией [12]. В ряде исследований оценивали влияние МТХ на состояние репродуктивной системы и овариальный резерв. По данным Brouwer J. et al. (2013), уровни антимюллерова гормона (AMГ) сыворотки у 72 женщин с недавно диагностированным РА, которые не получали терапию, значительно не отличались от показателей здоровых женщин [13]. Уровень AMГ у пациенток с РА, получавших МТХ парентерально в дозе 20 мг/неделю в течение 6 месяцев, был аналогичен уровню гормона у женщин, не получавших лечение [14]. Однако, согласно результатам исследования Henes M. et al. (2015), уровни AMГ сыворотки были значительно снижены у пациенток с ревматическими заболеваниями (РА, болезнь Бехчета и спондилоартрит) по сравнению с сопоставимыми по возрасту здоровыми женщинами [15]. В ходе другого исследования, в котором оценивали овариальный ответ на стимуляцию яичников, было показано, что среди женщин, принимавших МТХ в течение 18 месяцев, наблюдался значительно более слабый ответ яичников на стимуляцию по сравнению с контрольной группой [12].
Таким образом, отсутствие однозначных данных о влиянии основного заболевания на репродуктивную функцию, а также терапии МТХ на состояние овариального резерва у женщин с проблемами реализации репродуктивной функции и РА послужило основанием для проведения настоящего исследования.
Цель исследования – оценить показатель АМГ – основного маркера овариального резерва, у пациенток с РА и бесплодием, получавших и не получавших терапию МТХ.
Когда можно беременеть после метотрексата
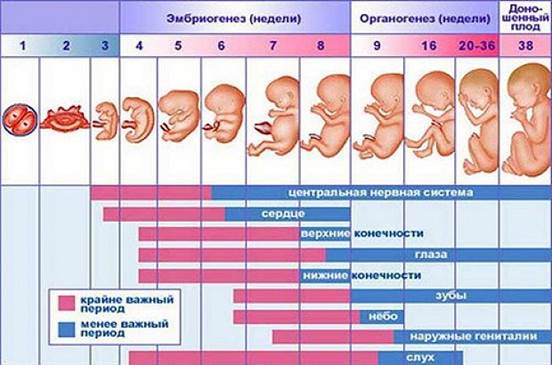
Рис.1 Внутриутробное развитие
Различают 3 вида патологических вариантов воздействия лекарственных средств на развитие плода: эмбриотоксический, тератогенный,фетотоксический. Эмбриотоксическое действие лекарственных препаратов, возникающее в первые 2-3 недели беременности, отмечается в негативном влиянии на зиготу и бластоцисту. Как следствие, может возникнуть гибель плода или морфофункциональные нарушения клеточных систем. Среди препаратов, которые вызывающие эмбриотоксическое действие выделяют противоопухолевые средства, противосудорожные препараты, никотин, эстрогены, гестогены, минералокортикоиды, антибиотики, сульфаниламиды, мочегонные препараты. (Табл. 1) Тератогенные эффекты, возникающие с 3 недели эмбриогенеза, вызывают нарушения биохимического, морфологического и функционального характера. Действие зависит от химической структуры, способности проникать через плаценту, дозировки препарата и скорость выведение лекарства из организма матери. По опасности препараты с тератогенными эффектами делятся на 3 группы: препараты, высоко опасные для плода, их употребление категорически запрещается даже за 6 месяцев до беременности, лекарства с определенной тератогенной опасностью, препараты, вызывающие отклонения при наличии определенных условий, например, высокий возраст беременной женщины, дозы применяемых лекарств [6]. Препараты с тератогенными эффектами являются наиболее опасными, так как они действуют на плод во время гистогенеза и органогенеза. Таким образом нарушение дифференцировки тканей может привести к порокам опорно-двигательной системы, а также внутренних органов. К таким средствам относятся: противоэпилептические средства, препараты половых гормонов, антибиотики, антикоагулянты, анальгетики, антидепрессанты, противомалярийные и противоопухолевые средства. Также известно, что прием ретиноидов, которые оказывают тератогенный эффект, вызывал врожденные аномалии развития, даже если курс лечения был завершен до начала беременности. (Табл. 1) [2,7]. Фетотоксическое действие наблюдается с 14-ой по 38-ую неделю беременности. Вызывают дисфункцию жизненно-важных систем органов. Примеры препаратов: аминогликозидные антибиотики, бета-адреномиметики и т.д. ( Табл. 1) [2,7] Лекарственные препараты проникают в организм плода через систему «мать-плацента-плод». Безусловно, самым важным органом во время беременности является плацента. Она служит своеобразным барьером между организмом матери и плода. Изначально толщина плаценты достигает 25мкм, но ближе к завершению беременности плацента становится заметно тоньше, ее толщина достигает 2 мкм. Этот факт способствует более легкому проникновению лекарств через плацентарный барьер в кровь плода. Также на ослабление плацентарного барьера влияют различные заболевания, например, сахарный диабет. Способность к проникновению различных веществ через плаценту обусловлена различными факторами, среди которых морфофункциональное состояние плаценты, плацентарный кровоток, физико-химическая характеристика лекарственных веществ и т.д. Известно, что большей проницаемостью через плаценту обладают низкомолекулярные вещества. Проникновение различных веществ через плаценту возможно различными путями, среди которых пиноцитоз, диффузия, активный транспорт. После проникновения лекарственного препарата происходит его дальнейшее попадание в пупочную вену, поэтому препарат достигает главных органов, например, сердце и мозг, минуя печень. Также важной проблемой является то, что некоторые препараты могут несколько раз циркулировать по организму плода, вызывая у него больший риск возникновения аномалий и пороков [8].
Таблица 1. Влияние лекарственных препаратов на развитие плода в первом, втором и третьем триместре беременности [4,5,9].
Университет
100 раз все взвесить…
Сегодня, несмотря на все еще сохраняющийся отрицательный баланс рождаемость/ смертность, снижение численности населения республики приостановлено. Это связано с активной демографической политикой в Беларуси. Утверждена программа дембезопасности на 2011–2015 годы, определяющая стратегию развития нашего государства и здравоохранения. Она включает комплекс мероприятий, направленных на повышение рождаемости, материнского здоровья, сокращение инвалидности и борьбу за жизнь каждого человека.
К большому сожалению, почти треть пациентов с ревматическими заболеваниями (РЗ) — лица детородного возраста. Сама беременность оказывает разноплановое влияние на течение и исходы ряда РЗ. В некоторых случаях (у пациенток с системной красной волчанкой (СКВ), хронической ревматической болезнью сердца) она провоцирует обострение или прогрессирование болезни, а вот при ревматоидном артрите (РА) с высокой долей вероятности (до 96%) приводит к ремиссии.
Полезна или вредна беременность при различных РЗ, в последние годы эта тема особенно активно обсуждается, что связано с достижениями в лечении. Своевременная диагностика, адекватная фармакотерапия позволяют на ранней стадии взять заболевание под контроль и в ряде случаев достичь стойкой ремиссии, когда качество жизни,самочувствие больных мало чем отличается от здоровых людей. Естественно, в такой ситуации женщины ставят перед врачом вопрос о возможности иметь детей.
Большинство РЗ непосредственного влияния на фертильность не оказывают. Ее снижение происходит после осложнений, когда в процесс вовлекаются органы репродуктивной системы (например, вследствие яичникового венозного тромбоза при антифосфолипидном синдроме) или как побочное действие каких-то препаратов. В частности, уже доказано: высокие дозы глюкокортикоидов, циклофосфамида снижают фертильность.
И все-таки планирование беременности у пациенток с РЗ довольно сложный вопрос, требующий индивидуального подхода. Надо учитывать ряд факторов: характер и активность процесса, степень компенсации жизненно важных органов и систем, принимаемые лексредства. Важно оценить риск обострения основного заболевания во время беременности и после родов, возможные осложнения у ребенка. Очень внимательно следует отнестись к лекарственной терапии, особенно в период лактации.
РА является значимой общемедицинской и социальной проблемой современной ревматологии. Широкая распространенность в популяции, поражение лиц трудоспособного возраста, высокий риск инвалидизации не могут не тревожить. Частота встречаемости РА составляет 0,5–1%, т. е. из 100 заболевает в среднем 1 человек. По данным официальной статистики, в Беларуси с РА 19 500 человек. В основном это женщины детородного возраста. И для большинства проблема материнства острая.
Планирование ребенка. Нужно 100 раз все взвесить, ведь рассчитывать придется на помощь членов семьи. Каждая женщина должна четко знать о возможных последствиях (например, обострении заболевания). Дело в том, что пациентки с РА, не верифицированным вовремя, испытывают физические мучения. В 2010 году созданы новые классификационные критерии ACR/EULAR, и появилась возможность ставить диагноз на ранней стадии, вырос процент тех, кто, принимая лексредства, чувствует себя замечательно и мечтает о ребенке. РА — заболевание, при котором рождение детей не является противопоказанием.
К тому же, по данным статистики, у 70–90% женщин в период вынашивания плода наступает ремиссия, что связано с изменением эндокринного фона, иммунологического статуса, снижением уровня противоспалительных цитокинов, фактора некроза опухолей и улучшением состояния в целом.
Сама болезнь плоду не вредит. Но после родов в первые 3 месяца у 90% пациенток РА обостряется. Поэтому женщине, решившей заиметь ребенка, важно быть к обострению готовой, ведь спрогнозировать течение болезни сложно.
В тактике ведения таких пациенток важны индивидуальный подход, опыт врача и знание особенностей организма женщины. Нужно учесть, что забеременеть она сможет в случае, если у нее нет сопутствующих эндокринных, воспалительных гинекологических заболеваний и др. Беременность должна наступать при достижении клинической ремиссии, сохраняющейся не менее полугода до зачатия.
Необходимо определить препараты, безопасные для матери и плода, их дозировку, чтобы подавить активность РА. Что именно из лекарств использовать для наступления ремиссии? Этот вопрос пока не решен. С одной стороны, нужны действенные — независимо от их влияния на эмбрион и его дальнейшее развитие, а с другой — выбирать те, что не противопоказаны при беременности. Мы ориентируемся на рекомендации FDA (Food and Drug Administration), т. к. четких положений по данной проблеме сегодня нет. Считаю, что в такой ситуации правильно подходить индивидуально, учитывая активность заболевания и отдавая предпочтение лексредствам с меньшим тератогенным (негативным) действием на яйцеклетки. К разрешенным FDA препаратам относится сульфасалазин, он хорош при невысокой активности РА. При нем беременность не противопоказана, но если процесс полностью не остановлен, женщина не может зачать ребенка, заболевание выходит из-под контроля. В ряде случаев, когда видно, что сульфасалазин не будет эффективен в полной мере, важно не упустить время и перейти на другое лексредство. Главная цель — достичь ремиссии. Шансы пациенток на нее значительно повышает своевременная адекватная фармакотерапия, если не сформировался паннус (видоизмененная синовиальная оболочка, способная к инвазивному росту).
FDA не запрещены аминохинолиновые препараты; допустим плаквенил (гидроксихлорохин). Стратегия ведения пациенток с высокой активностью заболевания включает метотрексат или лефлуномид, в случае, когда они не помогают — средства биологической генно-инженерной (антицитокиновой) терапии. У нас есть положительный опыт лечения ими, более стойкая ремиссия достигается в короткий срок. Правда, они противопоказаны во время беременности, но при безрезультатном предшествовавшем лечении помогают. В частности, тоцилизумаб (препарат Актемра). Он эффективен в монотерапии; другие же применяются в комбинации с метотрексатом, что не очень хорошо для планируемого зачатия. Мы имеем опыт успешной беременности у 2 пациенток после курса Актемры (другими препаратами это не удавалось).
Подавив активность РА и планируя беременность, необходимо рассчитать период выведения из организма медикаментов. Например, у метотрексата он составляет 6 месяцев, у ритуксимаба — год. После лефлуномида следует сделать процедуру «отмывания» — употреблять активированный уголь либо другие сорбенты. Без этого с беременностью надо повременить около 2 лет. Принимающим сульфасалазин промежуток не требуется.
Женщине с РА, мечтающей о ребенке, важно знать, что нестероидные противовоспалительные препараты (НПВП) могут изменить день наступления овуляции. Тератогенным эффектом они не обладают, но к III триместру эту группу медикаментов нужно отменить (высок риск незаращения баталова протока, что потенциально опасно для плода). Из всех НПВП наибольшая доказательная база накоплена о действии неселективных препаратов (диклофенак, ибупрофен, напроксен). Предпочесть лучше небольшие дозы глюкокортикоидов — в этом случае они менее вредны.
Вопрос, волнующий женщину с РА после родов: давать ребенку грудь или нет? Рекомендаций о прекращении грудного вскармливания нет. Если положительное решение принято, но обострение болевого синдрома есть, то можно употреблять неселективные НПВП короткого действия перед кормлением малыша. Тогда в грудное молоко попадет минимум лекарства.
Для пациенток с СКВ с активным люпус-нефритом или другими органными поражениями беременность исключена, ведь она может закончиться летальным исходом. Причем риск одинаков и для ребенка, и для матери. Если заболевание в состоянии ремиссии, нужно учитывать спектр антител, которые есть у женщины: возможна проблема у плода. Прерывание беременности в таких случаях часто приводит к обострению люпус-нефрита. Поэтому необходима четкая тактика ведения этих пациенток двумя специалистами — гинекологом и ревматологом.
…Учесть противоречия…
Значительное количество женщин на момент беременности имеют или переносят в различные ее сроки экстрагенитальную патологию, когда без лекарственных средств (ЛС) не обойтись. Широкое использование ЛС для лечения будущих мам сегодня — объективная реальность, обусловленная снижением уровня здоровья женщин детородного возраста и увеличением числа «немолодых» первородящих.
Ближайшие и отдаленные последствия приема ЛС зависят от характеристики препарата, его дозы, длительности применения и срока беременности. Результатами воздействия ЛС могут быть выкидыши, недоношенность, внутриутробная гипотрофия, угнетение дыхания и сердечной деятельности плода и другие пороки развития. Известны случаи отдаленных последствий, когда у взрослых дочерей, матери которых получали во время беременности эстрогены, развивались опухоли гениталий; у сыновей обнаруживались кисты придатков яичка, нарушения полового развития.
Информация о возможном влиянии ЛС на течение и исход беременности очень актуальна, т. к. большинство женщин узнают о своем «интересном» положении через 2–3 недели после зачатия. К этому моменту эмбрион находится на этапе формирования нервной трубки и сердечно-сосудистой системы. Поэтому наиболее правильный путь — планирование рождения ребенка. По данным зарубежных фармако-эпидемиологических исследований, свыше 90% женщин прибегают к ЛС во время беременности; из них 35% принимают их по меньшей мере 1 раз, а 4% употребляют 10 и более различных ЛС за всю беременность. По результатам первого белорусского эпидемиологического исследования «Лекарственные средства и беременность» (2009–2010 гг.), 91,7% женщинам из 1 334 опрошенных назначались ЛС: 76% — от 1 до 4 препаратов, 23% — 5–9, 1% — 10 и более. Было установлено, что лишь 8,3% женщин во время беременности не принимали никаких ЛС.
Что пьют обычно в «положении»? Витамины, анальгетики, антибактериальные и противогрибковые средства, седативные, антацидные, антигистаминные, отхаркивающие, противорвотные, антигипертензивные ЛС. Весьма актуальная проблема — бесконтрольное употребление БАД, поливитаминов и лекарственных растений.
Риск для плода от ЛС, которые принимают беременные, условно разделяют на 5 уровней (категории FDA USA — Администрации США по лекарственным средствам и пищевым добавкам). Самые безопасные, но немногочисленные, препараты категории А, в контролируемых исследованиях не выявлено угрозы в I триместре (в других — доказательств нет). Затем следуют категории В (изучение на животных не обнаружило риска для плода) и С (наоборот, выявило). Для категории D доказательства опасности есть, но иногда польза от применения может ее превышать.
К категории Х относят ЛС с установленным нарушением развития плода в экспериментах на животных (было замечено и у людей). Риск применения их беременными превышает любую предполагаемую пользу. ЛС категории Х противопоказаны и здоровым женщинам, способным забеременеть.
Наиболее чувствителен плод с 18-й по 22-ю неделю внутриутробного развития (III критический период), когда медикаменты способны оказать токсическое действие на органы будущего ребенка, вызвать нарушение гемопоэза, продукции гормонов, изменение биоэлектрической активности головного мозга. Например, прием НПВП, в т. ч. ацетилсалициловой кислоты, может на поздних сроках стать причиной кровотечения у плода (влияние на функцию тромбоцитов), привести к перенашиванию беременности из-за уменьшения уровня простагландинов, стимулирующих тонус матки. Индометацин способствует внутриутробному закрытию артериального протока еще до наступления родов. Тетрациклин в ряде случаев вызывает задержку развития костной ткани, пигментацию зубов, гипоплазию эмали.
Особое внимание нужно обратить вот на что. Случайный прием потенциально тератогенных препаратов до того, как женщина узнала о своем положении, не является абсолютным показанием для прерывания беременности; подобное решение принимается на основании результатов обследования и оценки потенциального риска для плода. К тому же если ЛС способны оказывать негативное влияние на продукцию половых клеток, то рекомендуется забор и хранение яйцеклеток и спермы для их последующего использования в репродуктивных технологиях.
В любых ситуациях при РЗ, за исключением угрожающих жизни матери, следует избегать циклофосфамида, метотрексата и лефлуномида, относящихся к категории Х и абсолютно противопоказанных во время беременности.
Характер тератогенности препарата — дозозависимый. Метотрексат должен назначаться женщинам детородного возраста только под прикрытием безопасной контрацепции. Фолиевая же кислота необходима в течение всей беременности.
Установлено нарушение процесса эмбриогенеза от лефлуномида. Поэтому производителем данного препарата рекомендуется безопасная контрацепция при терапии у женщин и мужчин детородного возраста. При планировании зачатия лефлуномид должен быть отменен, т. к. его активный метаболит определяется в плазме до 2 лет после прекращения приема. Ускорит выведение холестирамин (в т. ч. у мужчин). Сведений о появлении лефлуномида в грудном молоке нет, но кормление грудью не рекомендуется.
Бисфосфонаты (категория С) вызывают нарушения имплантации, возможно их проникновение через плаценту, накопление в костной ткани, снижение массы плода, нарушение родоразрешения и т. д. Из-за недостаточной информации зачатие надо отложить на полгода после прекращения курса лечения. Рекомендуется прием внутрь препаратов кальция одновременно с витамином D и во время лактации.
К медикаментам, которые можно использовать беременным, относятся НПВП. Диклофенак, ибупрофен, кетопрофен, напроксен в первые 2 триместра принадлежат к категории В FDA. Но в некоторых случаях они способны нарушать имплантацию бластоцист (5–6-дневных эмбрионов) и повышать риск невынашивания, особенно с момента зачатия или при продолжительности курса лечения более 1 недели. Поэтому в течение менструального цикла, когда женщина с РА пытается забеременеть, все НПВП рекомендуется отменить. Прием можно возобновить, получив положительные результаты тестов на беременность или в случае начала менструального кровотечения.
Неселективные и селективные ингибиторы циклооксигеназы (ЦОГ) способны блокировать или удлинять овуляцию, но частота ее подавления неизвестна. Неселективные ингибиторы ЦОГ нетератогенны, к ним можно прибегать в I и II триместрах. Предпочтение отдавать препаратам с коротким периодом полувыведения. Пока нет достоверных данных о селективных ингибиторах ЦОГ 2, от них лучше воздержаться.
Сегодня для лечения и вторичной профилактики тромбоэмболических осложнений и патологий беременности, вызванных присутствием антифосфолипидных антител, наиболее широко применяются гепарины (нефракционированный и низкомолекулярные) и непрямые антикоагулянты. Однако, по имеющимся сведениям, новые антитромбоцитарные и антикоагулянтные препараты пока не рекомендуются во время беременности и лактации. Например, фондопаринукс может проникать через плаценту, хотя предполагается, что он менее безопасен, чем нефракционированный и низкомолекулярные гепарины.
По показаниям назначаются глюкокортикоиды (ГК) — преднизон, преднизолон и метилпреднизолон. Из фторсодержащих ГК при необходимости антенатальной терапии лучше предпочесть бетаметазон, а не дексаметазон. Стрессовые дозы гидрокортизона при родах рекомендуются больным с длительной ГК-терапией. ГК значимо не повышают риск врожденных аномалий. В случае применения фторсодержащих препаратов надо обсудить постнатальное назначение ГК новорожденному, если неонатолог подтвердит надпочечниковую недостаточность.
Азатиоприн по показаниям может использоваться в ежедневной суточной дозе, не превышающей 2 мг/кг.
Циклофосфамид обладает тератогенным действием, гонадотоксичен для мужчин и женщин. Поэтому внутривенная терапия циклофосфамидом должна начинаться только после отрицательного теста на беременность. Женщинам детородного возраста, получающим этот препарат, нужна безопасная контрацепция, попытки зачатия лишь спустя 3 месяца после терапии.
Циклоспорин при беременности используется в более низких дозах. Но под контролем артериального давления и функции почек у женщины.
Безопасность инфликсимаба недостаточно определена, об этанерцептоме информации очень мало, поэтому беременным их лучше вообще не назначать.
Хочу отметить, что рекомендации касательно отдельных препаратов нередко противоречивы и различаются не только в научных публикациях и сведениях производителей разных стран. Поэтому очень важно анализировать все возможные данные о потенциальных рисках лекарств: экспериментальные исследования in vitro и с участием животных, вести мониторинг безопасного использования с помощью специализированного регистра.
…И готовиться к беременности
Когда обращается женщина с ревматоидным заболеванием (РЗ), которая хочет, но не может забеременеть, приходится решать ряд вопросов: не противопоказано ли ей материнство, способна ли она выносить ребенка, какие методы лечения бесплодия для нее применять?
Чтобы определить, можно ли женщину включать в программу обеспечения ее детородной функции, требуется заключение врача-ревматолога (стадия процесса, проводимая терапия, рекомендации на период беременности, если таковая не противопоказана). Для начала определяем потенциал фертильности, репродуктивные планы и детородный прогноз, т. е. оптимальное время для зачатия, возможность успешного вынашивания и безопасного материнства. Пациентки с РЗ сталкиваются с определенными трудностями. Например, системный склероз увеличивает частоту недоношенности и гипотрофии плода. Риск бесплодия возрастает в 2–3 раза. При системной красной волчанке (СКВ) вероятность антенатальной гибели плода повышается на 45% и более, т. к. отмечается обострение заболевания (до 50%). Беременность зачастую протекает тяжело, особенно если волчаночный нефрит развивается впервые.
Тем, кому пока следует повременить с зачатием, надо подобрать правильную контрацепцию. Отмечу, что больным СКВ рекомендуется использовать гормональные препараты без эстрогенов и другие средства (внутриматочные спирали, презервативы).
Если женщина случайно забеременела, а сохранение плода невозможно из-за приема ЛС при РЗ, то показано медикаментозное прерывание. Медикаментозный аборт применяется в стране с 2011 года как наиболее безопасный, т. к. не требуется хирургического вмешательства, разрешен в сроке до 49 дней от первого дня последней менструации.
Проблема деторождения актуальна почти для 20% супружеских пар. Специализированную помощь при бесплодии могут оказать в областных консультациях «Брак и семья», на базе диагностических центров. Спектр лечебных мероприятий в нашем центре шире благодаря применению с 2007 года вспомогательных репродуктивных технологий (ВРТ).
С 19 июля с. г. в Беларуси вступил в силу Закон «О вспомогательных репродуктивных технологиях». В противопоказаниях (в п. 22 инструкции) указано, что в программу, среди прочих, нельзя включать женщин с острой ревматической лихорадкой, хроническим ревматическим перикардитом, болезнями (пороками) клапанного аппарата сердца с патологией кровообращения. Необходимо учитывать нарушение гемостаза, особенности медикаментозной агрессии при ЭКО, оценить репродуктивный прогноз. По закону, применение ВРТ допускается в отношении лиц 18–49 лет (фертильный возраст по ВОЗ). Ограничивается количество переносимых эмбрионов в матку: 2 — до 35 лет, женщинам старше 35 лет и в особых случаях — не более 3.
К видам ВРТ относятся: искусственная инсеминация спермой мужа или донора, экстракорпоральное оплодотворение (ЭКО) и суррогатное материнство. При подборе женщин для ЭКО проводится обследование и оценивается овариальный (яичниковый) резерв, который может быть снижен после приема лекарств у пациенток с ревматическими заболеваниями. Некоторым в связи с гинекологическими заболеваниями показана хирургическая подготовка к ЭКО — удаление труб, миомы матки и т. д., чтобы увеличить шанс забеременеть и снизить риск потерь.
В циклах ЭКО применяются аналоги гормонов гипофиза: фолликулостимулирующий, лютеинизирующий (иногда показаны высокие дозы). Образовавшиеся в яичниках фолликулы содержат ооциты. Яйцеклетки из яичников получают хирургическим путем, оплодотворение и выращивание эмбрионов происходит вне организма, эмбрионы переносят женщине в матку на 3–5-й день. Потом в больших дозах назначаются аналоги естественного прогестерона, обычно до определения теста на беременность. Если результат положительный, гестагенная поддержка продолжается.
После использования ВРТ потери беременности составляют в среднем до 15%. Причем у женщин с РЗ они могут достигать 30%.
Медицинский вестник, 23 августа 2012