Что такое инсульт, чем опасен и что важно о нем знать?
Нарушение мозгового кровообращения, то есть инсульт, входит в ТОП-10 заболеваний, приводящих к смерти. При этом, по последним научным данным, инсульт, считающийся недугом пожилого возраста, стабильно «молодеет». Поэтому вопросы, от чего бывает инсульт, как диагностировать и как оказывать первую помощь на сегодня актуальны для всех возрастных категорий.
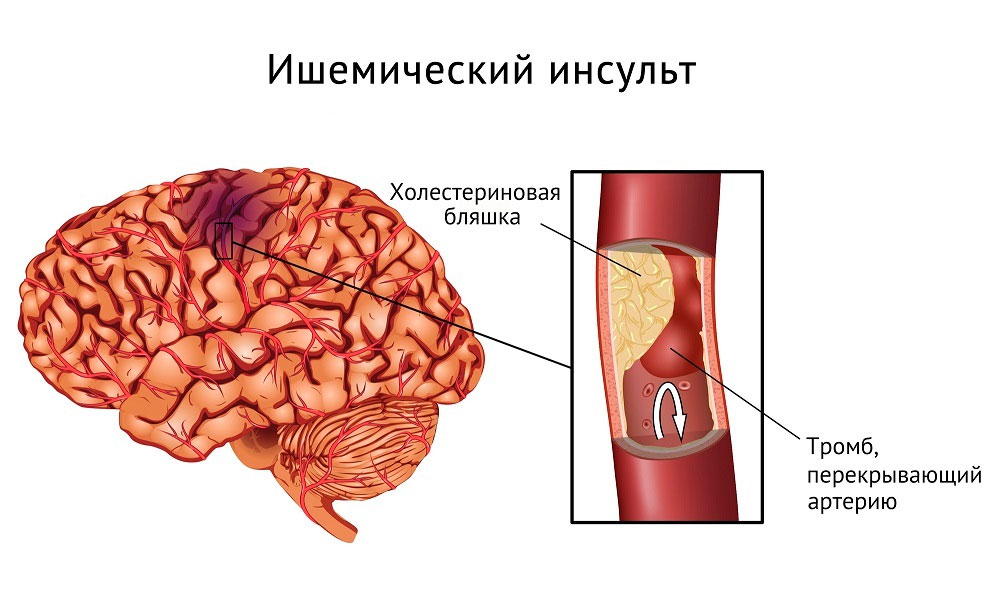
Изначально причин, почему в тканях мозга нарушается кровообращение, две: ишемия (отсутствие кровоснабжения) и кровоизлияние. Именно поэтому заболевание делится на два вида: ишемический и геморрагический. При ишемическом инсульте патологические изменения являются результатом закупорки сосуда, поставляющего кровь к тканям мозга. При этом перекрыть просвет сосуда может тромб, атеросклеротическая бляшка или стеноз (сужение) сосуда. Таким образом, клетки мозга остаются без необходимых для их функционирования веществ, которые поступали к ним с кровью — кислорода и питательных компонентов. В итоге, если ничего не предпринять, они отмирают. Этот вид инсультов встречается наиболее часто (около 80% от всех инсультов).
В случае с геморрагическим видом инсульта, механизм развития патологии другой. Здесь причиной нарушения функционирования нейронов является разрыв сосуда. В результате ткань мозга не только остается без кислорода и питательных веществ, но и находится под давлением накопившейся вокруг крови. Несмотря на то, что геморрагический инсульт возникает реже, чем ишемический, он все же более опасен и в плане летального исхода, и в плане необратимых изменений.
Причины
Необходимо знать, что есть определенные заболевания, которые могут способствовать возникновению инсульта. Ученые выделили их и назвали факторами риска. Лидером в этой группе является артериальная гипертензия. Именно постоянное высокое давление крови на стенки сосудов мозга, а тем более – его резкие скачки, способствует тому, что сосудистые стенки теряют свою эластичность и могут в какой-то момент разорваться.
Рискуют получить инсульт и люди, имеющие сердечные заболевания, особенно связанные с нарушениями сердечного ритма. В этом случае в сосудах часто образуются тромбы, один из которых и может послужить причиной инсульта. Не менее опасен в этом отношении и атеросклероз, когда из-за повышенного уровня холестерина в крови стенки сосудов «обрастают» отложениями, называемыми атеросклеротическими бляшками. Именно эти бляшки сужают просвет сосуда или могут вообще перекрыть его, приводя к ишемии.
Осторожным нужно быть и больным сахарным диабетом, поскольку это заболевание патологически влияет и на стенки сосудов. В результате они истончаются, становятся хрупкими и, как следствие, больше подвержены разрывам. Подобным образом, то есть разрывом, может однажды отреагировать и аневризма мозгового сосуда, то есть расслоение участка сосудистой стенки.
Привести к ишемическому инсульту могут и заболевания, провоцирующие сгущение крови. В этом случае причиной нарушения кровообращения в тканях мозга может стать тромб, образовавшийся из-за нарушения свертываемости крови.
Обратите внимание, что к факторам риска возникновения инсульта отнесены и ожирение, приводящее и к гипертонии, и к повышению холестерина в крови, и избыточное употребление соли, которое также способствует повышению давления. Сюда же зачислены малоподвижный образ жизни, курение, чрезмерное употребление алкоголя и стрессы, также не лучшим образом влияющие на состояние мозговых сосудов. И конечно же, возраст – уже после 30-ти лет современному человеку нужно уделять особое внимание своим сосудам.
Симптомы инсульта
Сам инсульт происходит без симптомов. Только когда клетки мозга начинают отмирать, можно наблюдать проявления инсульта.
Жизненно важно сразу определить, что это не что иное, как инсульт. Всегда помните: у вас есть всего ТРИ ЧАСА, когда можно избежать необратимых процессов.
Поэтому, если есть хотя бы два из перечисленных симптома, не взирая ни на какие отговоры со стороны больного, срочно вызывайте скорую помощь для госпитализации.
Первая помощь при инсульте
Внимание!
Профилактика или как избежать инсульта
Инсульт намного легче предупредить, чем лечить или реабилитировать больного после приступа. Поэтому при любых нарушениях мозгового кровообращения нужно срочно заняться профилактикой инсульта.
Но-Шпа: противопоказания, от чего помогают
Препарат «Но-Шпа» относится к спазмолитическим медикаментам. Он облегчает болевой синдром при спазмах гладкой мускулатуры. Средство принимают для купирования болей при заболеваниях желудка, кишечника, печени, почек и других внутренних органов. Средство редко дает побочные действия и при этом отличается эффективностью.
«Но-Шпа»: состав и другие характеристики
Препарат относится к категории спазмолитиков. Выпускается в форме таблеток (по 6, 10, 24 штуки в одной упаковке) или в форме уколов (по 25 ампул объемом 2 мл каждая).
Действующим веществом является дротавертин (представлен гидрохлоридом). В каждом таблетке, содержится по 40 мг, в растворе каждой ампулы – по 20 мг. В разновидности «Но-Шпа Форте» (дозировка увеличена в 2 раза – 80 мг).
Таблетки могут иметь желтоватую, зеленоватую или оранжевую окраску. Форма таблеток округлая, обе поверхности выпуклые. С одной стороны идет линия разлома посередине, с другой – монолитная поверхность с надписью «NOSPA». Раствор в ампулах также окрашен в оттенки желтого и зеленого.
Срок годности зависит от формы выпуска. Таблетки можно хранить в течение 5 лет, а ампулы – 3 лет с момента выпуска. Препарат берегут от света, хранят при комнатной температуре в диапазоне от 15 до 25 градусов.
Таблетки можно приобрести без получения рецепта врача, а инъекции – только по рецепту.
От чего помогают таблетки «Но-Шпа»
Препарат принимают таблетками, а также в виде инъекций (как внутримышечно, так и внутривенно) для быстрого снятия спазма гладкой мускулатуры. Это необходимо для облегчения болевого синдрома, проявляющегося на фоне таких болезней:
«Но-Шпу» используют и для купирования спазмов, связанных с патологиями желудка, кишечника. Такие симптомы могут проявляться на фоне запора, язв, колита, СРК и других нарушений. Еще одно показание к применению – головная боль и дисменорея. Однако в этом случае препарат подействует только, если боль связана со спазмом сосудов (ощущается как напряжение в голове).
В обычных случаях используют форму «Но-Шпа». Усиленную концентрацию в составе препарата «Но-Шпа Форте» применяют при необходимости обеспечить стойкий длительный эффект (на дни, недели вперед). Также «Форте» принимают, если нужно сократить кратность, например, до 1 раза в сутки.
Противопоказания к приему
Противопоказаниями к применению средства являются такие заболевания и особенности:
низкий сердечный выброс;
тяжелые заболевания почек и печени (недостаточность);
повышенная чувствительность к действующему веществу (дротаверин) либо к другим компонентам в составе таблетки;
лактазная недостаточность (нарушения обмена галактозы, глюкозы).
Во время беременности (любой срок) средство принимают с осторожностью, аналогичные рекомендации для детей и лиц с пониженным давлением. Рекомендуется предварительно посоветоваться с врачом.
Побочные эффекты от приема таблеток «Но-Шпа»
В большинстве случаев побочных эффектов не наблюдается. Но при длительном приеме, а также в силу индивидуальных особенностей организма, состояния человека могут проявиться такие последствия:
повышение сердечного пульса;
снижение кровяного давления;
нарушения работы кишечника (запор);
В случае введения укола дополнительно может наблюдаться местная реакция (покраснение, посторонние ощущения).
Инструкция по применению «Но-Шпа»
Дозировка и правила приема зависят от формы препарата и возраста человека:
Суточная дозировка действующего вещества для взрослого человека лежит в диапазоне 120-240 мг, что соответствует 3-6 таблеткам обычного препарата и 2-3 таблеткам разновидности «Форте». При этом за один раз допускается употреблять не более 40 мг, т.е. максимум 2 таблетки.
Для детей до 11 лет включительно оптимальной дозой является 80 мг – это количество принимают за 2 раза в течение суток.
Для детей старше лет показана доза 160 мг с распределением на 2-4 раза.
Общий курс терапии (при самостоятельном лечении) не более 2 суток. Если в течение этого времени самочувствие не улучшилось, необходимо обратиться к специалисту для возможной замены препарата, проведения диагностики. Если «Но-Шпа» используется как дополнительный медикамент в составе комплексной терапии, то курс без консультации специалиста может длиться до 3 суток.
Случаи передозировки
При нарушении указанной дозировки может наблюдаться сердечная аритмия, ухудшение проводимости тканей сердца, редко –полная блокада пучков Гипса, что приведет к остановке сердца и летальному исходу. При этом смертельной дозой действующего вещества является количество от,6 до 2,4 г, что соответствует 40-60 таблеткам, принятым за один раз.
Взаимодействие с другими лекарствами
«Но-Шпу» можно применять в сочетании с другими спазмолитическими медикаментами, поскольку в этом случае обезболивающий эффект становится более выраженным. Если применять препарат вместе с лекарствами против болезни Паркинсона, это может привести к усилению тремора и ригидности.
Особые указания
В составе «Но-Шпы» присутствует лактоза, поэтому пациентам с нарушениями всасывания глюкозы и галактозы таблетки можно принимать с осторожностью и только после одобрения врача.
Если вводить раствор внутривенно, пациент должен полежать несколько минут в состоянии покоя. При наличии повышенного давления прием допускается только по согласованию с врачом.
Раствор для укола содержит метабисульфит натрия, который может вызывать аллергическую реакцию. В редких случаях (особенно при наличии бронхиальной астмы, хронической аллергии) возможен спазм бронхов и наступление отдельных признаков анафилактического шока.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Chinoin Pharmaceutical and Chemical Works Private Co. Ltd
Реабилитация после инсульта в домашних условиях
Реабилитация после инсульта в домашних условиях
Нарушение мозгового кровообращения приводит к таким последствиям, как частичный или полный паралич, потерю речи, памяти, слуха. Но грамотная реабилитация после инсульта позволяет вернуть человеку утраченные способности. В домашних условиях провести полноценное лечение и обеспечить последующее восстановление возможно, если заранее понять, что ожидает людей, близких больному, какие мероприятия потребуется проводить.
Длительность восстановительного периода
Сколько времени нужно для реабилитации после перенесенного инсульта, зависит от обширности повреждений, степени проявления возникших нарушений, возраста пациента и других факторов. Постепенно на месте погибших нейронов могут образоваться новые. Часть функций, выполняемых поврежденными отделами мозга, может быть перенесена на здоровые структуры.
При легкой форме ишемического инсульта, в результате которой у человека возникает нетяжелый паралич конечностей, лицевых мышц, нарушение зрения и координации, для частичного восстановления понадобится один-два месяца. Для полного – около трех месяцев.
Если последствия нарушения мозгового кровообращения проявляются в виде стойких нарушений координации, грубого паралича, срок реабилитации будет длиться не менее полугода. При этом шанс на возвращение всех утраченных навыков минимален.
После тяжелого инсульта, повлекшего паралич одной стороны тела и другие проблемы, от начала лечения до возвращения больному способности сидеть и обслуживать себя проходит от одного до двух лет. О полном исцелении в данном случае говорить невозможно.
Уровни восстановления нормальных функций организма у людей, перенесших инсульт, делятся на три группы:
Основным условием для успешной реабилитации после инсульта является готовность самого больного и близких ему людей пройти долгий путь, не сдаваясь и не прерывая занятий.
Как предотвратить инсульт?
Ученый Дмитрий Напалков: семь правил помогают предотвратить инсульт
О мерах профилактики инсульта изданию «Собеседник» рассказал профессор кафедры факультетской терапии №1 лечебного факультета Первого МГМУ имени И. М. Сеченова Дмитрий Напалков.
Каждый год в мире регистрируется около 12 миллионов случаев инсульта. В России каждые полторы минуты у кого-то случается инсульт. Эта коварная болезнь может случиться с кем угодно независимо от возраста и генетики. Когда это происходит с близким или знакомым человеком, мы хватаемся за голову: ну ведь можно же было все предотвратить? Можно! Только для этого нужно соблюдать несколько важных условий.
У одного моего знакомого случился инсульт, когда тот находился в командировке. Работал целыми сутками без отдыха. Резко заболела голова, помутилось сознание так, что не мог выговорить и двух предложений. Коллеги вызвали скорую не сразу. Дали какую-то таблетку: «Отлежись, все пройдет». Через пару часов ситуация ухудшилась настолько, что откачать моего знакомого смогла только реанимация.
Доктор медицинских наук, профессор кафедры факультетской терапии №1 лечебного факультета Первого МГМУ имени И. М. Сеченова Дмитрий Напалков на наш вопрос – как предотвратить инсульт? – ответил вот что:
– Все хотят предостеречь себя от инсульта, но мало кто что-то делает для этого. Сердечно-сосудистые заболевания зависят преимущественно от образа жизни. Недостаток физической активности, нездоровое питание, наличие вредных привычек – очень серьезные факторы риска. Однако при серьезных нарушениях в работе сердца и сосудов одно только питание и физические нагрузки не помогут. Необходимо принимать лекарства по назначению врача. И быть очень внимательными! Например, известный антикоагулянт (антагонист витамина К), применяющийся для профилактики инсульта, налагает большие ограничения в питании: малина, зеленый чай, зеленые овощи, капуста, яйца и другие продукты, богатые витамином К, нежелательны. Однако наука на месте не стоит, и сейчас создано новое поколение препаратов – например на основе прямых ингибиторов тромбина. Они ограничений в диете не требуют.
Не стоит пренебрегать такими мерами, как: сокращение количества соли в рационе до 5 г в день (около половины чайной ложки), о тказ от продуктов с высоким содержанием холестерина.
Добавление в повседневный рацион фруктов, овощей, цельнозерновых и обезжиренных молочных продуктов, а также одной порции рыбы два-три раза в неделю.
Регулярно проходите осмотр у специалиста. Важна консультация не только терапевта, но и врача-невролога. Необходимо сделать УЗИ сосудов шеи и получить на руки карту здоровья.
Следите за кровяным давлением. Артериальная гипертония в несколько раз увеличивает риск развития инсульта. Поэтому желательно измерять уровень артериального давления хотя бы раз в неделю. Даже если вы хорошо себя чувствуете и у вас отсутствуют такие симптомы гипертонии, как головная боль, чувство усталости и нарушения сна, повышение показателей давления в состоянии покоя выше значения 140/90 мм рт. ст. – это уже повод обратиться к врачу.
Мировая практика показывает, что благодаря одному лишь контролю уровня артериального давления удается снизить риск инсульта на 50%.
Контролируйте свой вес. Неврологи сходятся во мнении, что снижение веса – одна из самых действенных мер в профилактике инсульта. Избыточная масса тела способствует развитию высокого артериального давления, возникновению диабета и создает повышенную нагрузку на сердечную мышцу.
Понятно, что уменьшить свой вес мы не сможем без правильного рациона питания. Стоит отказаться от жирной и тяжелой пищи, чтобы снизился уровень сахара и холестерина в крови. Для получения результата необходимо придерживаться диеты не менее 3–4 месяцев.
Будьте активны. Гиподинамия, или слишком низкий уровень физической активности, – это бич нашего времени. Поэтому важно делать физические упражнения продолжительностью свыше 30 минут не менее 5 раз в неделю.
Для профилактики инсульта лучше всего подходит аэробная нагрузка – это повторяющиеся упражнения, при которых увеличивается поступление кислорода в организм. Лучше всего физические упражнения подберет вам врач с учетом возраста и имеющихся заболеваний.
Ну а эти правила доступны каждому: пользуйтесь лестницей вместо лифта, лучше выйдите на одну остановку раньше и пройдитесь пешком, найдите время, чтобы прогуляться в обеденный перерыв.
Лечите диабет. У тех, кто страдает сахарным диабетом существенно возрастает риск возникновения инсульта. Больные с сахарным диабетом переносят инсульт значительно тяжелее, чем все остальные. Это связано с тем, что из-за атеросклероза многие артерии неспособны перемещать кислород. И увы, прогноз инсульта при сахарном диабете в большинстве случаев будет значительно хуже.
Меньше употребляйте алкоголя. До недавнего времени взаимосвязь между потреблением алкоголя и инсультом оставалась под вопросом, но сегодня сомнений не осталось: алкоголь значительно повышает риск развития инсульта.
Откажитесь от курения. У курящих людей инсульт случается в 2–3 раза чаще, чем у некурящих. Вывод: чем больше вы курите, тем выше риск инсульта! К тому же большое значение имеет возраст курильщика: у курящих мужчин и женщин в возрасте до 55 лет курение является главным фактором риска развития инсульта.
В поврежденной сосудистой стенке развивается атеросклероз (утолщение стенки и уменьшение просвета), а это повышает риск образования тромба в сосудах мозга. Курение влияет на свойства особых клеток крови – тромбоцитов, в результате повышается риск образования тромбов в крупных артериях, несущих кровь к мозгу и сердцу. И еще курение повышает артериальное давление, являющееся одним из важнейших факторов риска развития инсульта.
Кстати! Изучение тысяч пациентов в течение 35 лет (Nurses’ Health Study) показало, что обычное питание европейца, включающее большое количество мяса, яиц, жареной и соленой пищи, очищенный хлеб, жирные молочные продукты, сладкие десерты и чипсы, увеличивает риск инсульта на 58%. В то время как употребление продуктов из цельных зерен, фруктов, овощей и рыбы снижает этот риск на 30%.
Постинсультный болевой синдром
В статье рассматриваются клинические проявления, особенности диагностики и лечения постинсультной боли. Структура постинсультного болевого синдрома гетерогенна и может включать в себя в разных комбинациях центральную постинсультную боль, спастическую боль
The article covers clinical manifestations, features of diagnostics and treatment of post-stroke pain. The structure of post-stroke pain syndrome is heterogeneous and can include, in different combinations, central post-stroke pain, spastic pain, humeral pain, tension headache and complex regionar pain syndrome. Complicated nature of post-stroke pain requires complex long-term therapy.
В 1906 г. J. J. Dejerine и G. Raussy [1] впервые дали развернутую клиническую характеристику болевому синдрому после перенесенного инсульта. Синдром Дежерина–Русси (центральный или таламический болевой синдром), представлял собой интенсивную непереносимую боль у пациентов с инфарктом таламуса, который включал: острые жгучие боли по гемитипу, снижение всех видов чувствительности, гиперпатию, гемипарез, легкую гемиатаксию, мышечную дистонию. Наряду с двигательными и сенсорными расстройствами такой пациент также испытывает выраженные когнитивные нарушения и депрессию [2]. При этом считается, что тяжесть испытываемой боли коррелирует с тяжестью когнитивных нарушений и депрессии [3]. Постинсультная боль может стать причиной суицидальных попыток. Развитие постинсультной боли отмечается у 12–55% пациентов. Обычно болевой синдром развивается в течение 3–6 месяцев после инсульта [4], однако нередки случаи появления боли и в течение первого месяца. Постинсультный болевой синдром с точки зрения патогенеза является гетерогенным, и в его структуре можно выделить центральную боль, постинсультную боль, боль, связанную со спастичностью, боль в плече, головные боли напряжения, комплексный регионарный болевой синдром.
Долгое время развитие центральной постинсультной боли связывали только с поражением таламуса. Однако внедрение в современную клиническую практику методов нейровизуализации позволило установить, что центральная постинсультная боль развивается как при поражении таламуса, так и вне таламических структур. Центральная постинсультная боль может возникнуть при поражении соматосенсорного анализатора на любом уровне — коры головного мозга, ядер таламуса, структур продолговатого и спинного мозга. По данным эпидемиологических исследований центральная постинсультная боль развивается у 1–12% пациентов. Ряд авторов считает, что ишемический инсульт чаще приводит к развитию центральной боли, чем геморрагический инсульт [5]. Центральная постинсультная боль относится к группе невропатических болевых синдромов и по определению экспертов Международной ассоциации по изучению боли (The International Association for the Study of Pain, IASP) является прямым следствием поражения или заболевания центральных отделов соматосенсорной системы [6].
Наиболее часто цитируемой гипотезой о природе центральной невропатической боли является концепция Хэда и Холмса о нарушении тормозного влияния лемнисковой соматосенсорной системы на восходящую палеоспиноталамическую систему [7]. Более поздние гипотезы о механизмах формирования центральной боли по существу являются детализацией концепции Хэда и Холмса о взаимодействии «специфических» латеральных и «неспецифических» медиальных структур мозга. Например, Л. А. Орбели (1935) [8] придавал важное значение в механизмах развития центральной боли нарушению баланса между лемнисковой и экстралемнисковой системами мозга. K. Winther (1972) [9] существенное место отводит нарушению афферентного взаимодействия между импульсными потоками эпикритической и протопатической боли. Электрофизиологические исследования, проведенные у пациентов с центральными болевыми синдромами, позволили высказать предположение, что гиперактивация нейронов медиального таламуса при повреждении латеральных таламических ядер происходит через ретикулярное таламическое ядро [10, 11]. Согласно гипотезе об ограничении термосенсорного входа [12], центральная боль возникает вследствие снижения холодового тормозного влияния на процессы обработки болевой информации. Предположение автора основывается на том, что при центральных болевых синдромах снижение температурной чувствительности происходит раньше, чем болевой, а в ряде случаев является единственным сенсорным дефицитом. В большинстве случаев пациенты с центральным болевым синдромом испытывают жгучие или леденящие боли в зоне снижения температурной чувствительности, при этом степень боли пропорциональна температурной гипестезии.
Повреждение центральных структур соматосенсорной системы приводит к нарушению механизмов контроля возбудимости ноцицептивных нейронов в центральной нервной системе и изменяет характер взаимодействия в системах, осуществляющих регуляцию болевой чувствительности. Вследствие нарушения тормозных и возбуждающих процессов развивается центральная сенситизация ноцицептивных нейронов с длительной самоподдерживающейся активностью. Повышение возбудимости и реактивности ноцицептивных нейронов при центральном болевой синдроме наблюдается в дорсальном роге спинного мозга, таламических ядрах и соматосенсорной коре большого мозга.
Центральная постинсультная боль может иметь ограниченную зону и локализоваться в какой-либо части тела или распространяться по гемитипу. У пациентов с поражением ствола мозга боль может быть ограничена половиной лица или локализоваться на противоположной стороне туловища или конечностей [2]. Распределение боли по гемитипу характерно для таламического поражения.
Представленность центральной постинсультной боли полностью или частично соответствует локализации чувствительных нарушений и соотносится с областью цереброваскулярного поражения [13]. Примерно 80% центральной постинсульной боли приходится на поражение париетальной коры [14]. Для центральной постинсультной боли характерно сочетание негативных и позитивных сенсорных феноменов в области локализации боли [15]. Расстройства температурной (холодовой) и болевой чувствительности отмечаются более чем у 90% пациентов, в то время как нарушение других видов чувствительности (тактильной, вибрационной) встречается реже [16]. Одновременно в болезненной зоне диагностируется аллодиния, гипералгезия, гиперпатия. У одного больного могут наблюдаться несколько типов болевых ощущений. Постоянная спонтанная боль описывается чаще как жгучая, покалывающая, холодящая и давящая, а периодическая боль носит разрывающий и стреляющий характер [4]. Интенсивность боли может варьировать в течение дня, под воздействием провоцирующих факторов. Основными факторами, приводящими к усилению болевого синдрома, могут быть холод, эмоциональный стресс, физическая нагрузка, усталость, изменение погоды. Тревожно-депрессивная симптоматика усугубляет течение болевого синдрома. Боль может снижаться при отдыхе, отвлечении внимания, исчезает во сне. Многим пациентам приносит облегчение тепло.
Многие пациенты после инсульта также испытывают «спастическую» боль [17]. Проспективное обсервационное исследование продемонстрировало тесную связь между развитием спастичности и боли. У 72% пациентов со спастичностью развивается боль, при этом только 1,5% больных без спастичности испытывают боль [18].
В настоящее время считается, что постинсультная спастичность является отражением сочетанного поражения пирамидных и экстрапирамидных структур головного мозга, приводящего к снижению тормозных влияний преимущественно на α-мотонейроны спинного мозга [19]. Развитие спастичности ухудшает двигательные функции, способствует развитию контрактуры и может сопровождаться болезненными мышечными спазмами [20]. Спастическая дистония и боль приводят к снижению функциональных возможностей больных и их реабилитации. Риск развития спастичности выше у пациентов с выраженным парезом, низкими баллами по шкалам Бартеля, постинсультной центральной болью и сенсорным дефицитом. Ведущую роль в лечении постинсультной спастичности имеет лечебная гимнастика, которая должна начинаться уже с первых дней развития инсульта и быть направлена на тренировку утраченных движений, самостоятельное стояние и ходьбу, а также профилактику прогрессирования спастичности и развития контрактур. В клинической практике для лечения постинсультной спастичности наиболее часто используются миорелаксанты (толперизон, тизанидин, баклофен), применение которых может улучшить двигательные функции, облегчить уход за обездвиженным пациентом, снять болезненные мышечные спазмы, усилить эффект лечебной физкультуры и предупредить развитие контрактур.
В настоящее время получены прямые доказательства того, что миорелаксирующий эффект толперизона связан не только с торможением активности потенциал-зависимых Na+-каналов, но и снижением выброса возбуждающих нейромедиаторов. В частности, на модели изолированного нерва [21] было установлено, что добавление толперизона в инкубируемую среду в дозе 100 µмоль/л снижает проницаемость ионов натрия на 50%. Сравнительное изучение влияния толперизона и лидокаина на семь типов потенциал-зависимых натриевых каналов показало, что толперизон, также как и лидокаин, оказывает блокирующее действие на активность натриевых каналов, однако степень блокирования у толперизона выражена в меньшей степени. Значительные различия между двумя препаратами в восстановлении активности натриевых каналов были продемонстрированы для трех типов натриевых каналов — Nav1.3, Nav1.5 и Nav1.7, не имеющих отношения к проведению болевой импульсации, в то время как продолжительность инактивации для каналов типа Nav1.8, имеющих отношение к ноцицептивной импульсации, у лидокаина и толперизона была схожей [22].
Исследования, проведенные на клетках ганглиев задних корешков, обнаружили, что толперизон угнетает потенциал-зависимую натриевую проводимость в концентрациях, в которых он ингибировал спинальные рефлексы. Более того, толперизон оказывал значительное воздействие на потенциал-зависимые кальциевые каналы. Эти данные позволили авторам утверждать, что толперизон реализует свое миорелаксирующее действие преимущественно путем ингибирования пресинаптического высвобождения нейромедиаторов из центральных терминалей афферентных волокон путем комбинированного влияния на потенциал-зависимые натриевые и кальциевые каналы [23].
Таким образом, толперизон, блокируя натриевые и кальциевые каналы в ноцицептивных афферентах, способен подавлять секрецию возбуждающих аминокислот из центральных терминалей первичных афферентных волокон, ослаблять частоту потенциалов действия мотонейронов и тем самым тормозить моно- и полисинаптические рефлекторные реакции в ответ на болевые стимулы. Такое действие толперизона обеспечивает эффективный контроль над спастичностью и мышечной болью.
Помимо действия на мышечный тонус, толперизон обладает способностью усиливать периферическое кровообращение. Данный эффект связан с блокадой альфа-адренорецепторов, локализованных в сосудистой стенке. Усиление кровообращения в мышце может быть дополнительным фактором, препятствующим сенситизации мышечных ноцицепторов при мышечной спастичности в условиях болевой импульсации.
Препарат селективно ослабляет патологический спазм мышц, не влияя в терапевтических дозах на нормальные сенсорные и двигательные функции центральной нервной системы (мышечный тонус, произвольные движения, координацию движений) и не вызывая седативного эффекта, мышечной слабости и атаксии. Толперизона гидрохлорид в отличие от других миорелаксантов вызывает мышечное расслабление без симптомов отмены, что было доказано в двойном слепом, плацебо-контролируемом исследовании, проведенном по критериям GCP [24].
В зависимости от доказанной эффективности и степени безопасности препараты были отнесены к той или иной линии терапии (табл.).
Как видно из табл., к препаратам первой линии терапии невропатической боли были отнесены габапентин, прегабалин, дулоксетин, венлафаксин и ТАД.
Авторы рекомендаций отмечают, что выбор того или иного препарата в каждом конкретном случае определяется совокупностью различных факторов, включающих возможные риски нежелательных явлений, наличия коморбидных расстройств (депрессии и нарушений сна), особенности лекарственных взаимодействий, возможность передозировки или лекарственных злоупотреблений.
В качестве терапии первой линии у пациентов с центральной постинсультной болью рекомендуется применение ТАД, прегабалина, габапентина. Селективные ИОЗСН, ламотриджин, опиоиды и их комбинации могут также использоваться при недостаточном эффекте препаратов первой линии.
Важным аспектом при лечении центральной постинсультной боли является четкая постановка реальных целей терапии боли и формирование адекватных ожиданий у пациента и родственников. Учитывая торпидный характер течения центральной постинсультной боли, целью терапии будет не устранение боли, а снижение интенсивности болевого синдрома, расширение функциональных возможностей пациента, улучшение качества жизни. Соблюдение режима дозирования и титрации препаратов, основанного на индивидуальной чувствительности больного, позволит сохранить комплаентное отношение больного к проводимой терапии. Низкие показатели эффективности фармакотерапии невропатической боли по данным ряда исследований, как правило, обусловлены неоптимальным дозированием и преждевременным прекращением приема назначенных лекарственных средств [27, 28]. Использование препаратов с различными механизмами действия при проведении комплексной фармакотерапии может способствовать повышению эффективности лечения. Врач также должен обеспечить постоянное мониторирование терапевтических и побочных эффектов. При мониторинге необходимо оценивать не только интенсивность боли, но и качественные сенсорные характеристики боли (жгучий характер, прострелы, дизестезии, аллодиния, онемение), качество сна, выраженность тревоги и депрессии, функциональные возможности и социальную адаптацию. При неэффективности консервативной медикаментозной и немедикаментозной терапии необходимо направить пациента в альгологические центры для решения вопроса об инвазивных методах лечения.
Литература
М. Л. Кукушкин, доктор медицинских наук, профессор
ФГБНУ НИИОПП, Москва






.gif)



