«Ловушки», в которые можно угодить при лечении бронхиальной астмы
Рисунок 1. Зачастую у больных астмой снижены виды на будущее, хотя некоторые склонны недооценивать тяжесть симптомов своего заболевания Какова дифференциальная диагностика между бронхиальной астмой и ХОЗЛ? С чем связаны возможны
 |
| Рисунок 1. Зачастую у больных астмой снижены виды на будущее, хотя некоторые склонны недооценивать тяжесть симптомов своего заболевания |
Какова дифференциальная диагностика между бронхиальной астмой и ХОЗЛ?
С чем связаны возможные ошибки в диагностике?
Какова основная роль b-агонистов в терапии бронхиальной астмы?
Как назначаются кортикостероиды?
Несмотря на возросшую компетентность врачей и доступность эффективных методов лечения, смертность от бронхиальной астмы остается высокой. Предотвратить многие смертельные исходы и даже избежать большинства случаев госпитализации можно было бы при проведении правильного лечения.
Необходимо помнить, что ведение больных астмой — процесс сложный и длительный.
Недооценка степени несостоятельности дыхания. Тяжесть состояния пациента и степень несостоятельности его дыхательной системы можно не распознать, если пренебречь тщательным выяснением всех проявлений болезни и построением диаграммы измерений максимальной скорости потока (МСП) выдыхаемого воздуха.
Зачастую у больных астмой снижены виды на будущее, хотя некоторые и склонны недооценивать серьезность симптомов своего заболевания. Чтобы выявить такую недооценку, нужно подробно расспросить пациента, бывает ли у него кашель или хриплое дыхание ночью или при физической нагрузке.
Если пациентам не удается достичь наилучшей возможной функции легких, то для коррекции этого состояния необходимо для начала вычислить нормальную МСП выдыхаемого воздуха для данного пациента, пользуясь диаграммой, прилагаемой к пикфлуометру.
Если измеренная МСП более чем на 20% меньше вычисленной, стоит провести исследование обратимости этого состояния, что делается путем сопоставления МСП или жизненной емкости легких (ЖЕЛ) до и после лечения.
Необходимая терапия может состоять всего лишь в однократном приеме бронходилятатора, но если это не увеличивает МСП на 20%, то есть до вычисленного уровня, могут понадобиться более серьезные меры, например трехнедельный курс системных кортикостероидов (30 мг преднизолона в день для взрослых). Таким образом выясняется наилучший достижимый уровень МСП, на который ориентируются в последующем лечении.
Иногда пациенты сообщают об уменьшении одышки, но при этом значения МСП не изменяются. В таких случаях необходимо провести измерение ЖЕЛ с помощью спирометра, которое может подтвердить улучшение, не определяемое по МСП (рис. 2). Спирометрами в настоящее время укомплектованы все врачебные приемные.
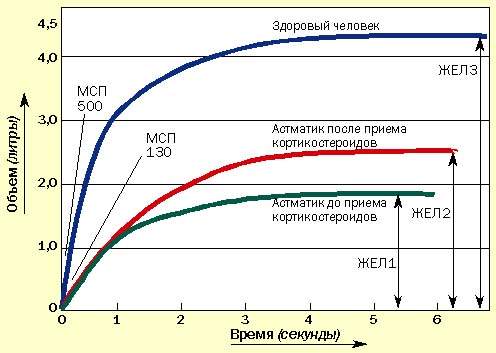 |
| Рисунок 2. Изменение ЖЕЛ под влиянием курса кортикостероидов. МСП может не измениться, но увеличение ЖЕЛ свидетельствует об улучшении состояния |
Бронхиальная астма, замаскированная под хроническое обструктивное заболевание легких (ХОЗЛ). Страдающие одышкой пациенты, которым поставлен диагноз ХОЗЛ или эмфизема, могут иметь скрытый бронхоспастический элемент, обусловленный бронхиальной астмой.
Таким пациентам необходимо провести исследование обратимости процесса, как описано выше. Любое улучшение функции легких можно поддержать, проводя адекватное лечение бронхиальной астмы. При отсутствии улучшения легочной функции назначение кортикостероидов ничем не оправдано, а только приводит к нежелательным побочным эффектам, таким как остеопороз.
Что должен помнить врач, наблюдающий больных с бронхиальной астмой
Постоянный прием b-агонистов короткого действия. Показано, что лечение астмы постоянным приемом b-агонистов увеличивает гиперреактивность легких и утяжеляет бронхиальную астму [1]. Если пациент использует b-агонисты скорее регулярно, чем случайно, их применение должно сопровождаться назначением ингаляционных кортикостероидов или, если кортикостероиды уже применяются, увеличением их дозы до достаточной, чтобы контролировать астму. Таким образом, b-агонисты оставляют на случаи одышки и хрипов.
Последние методические указания по лечению бронхиальной астмы в Британии рекомендуют начинать с высокой дозы ингаляционных или системных кортикостероидов для достижения быстрого контроля, затем постепенно снижать дозу до минимальной, обеспечивающей нормальное самочувствие пациента и оптимальные значения МСП или ЖЕЛ на фоне минимального применения бронходилятатора (рис. 3). Быстрое облегчение состояния, достигаемое при применении кортикостероидов, улучшает настроение пациента и увеличивает его доверие к лечению.
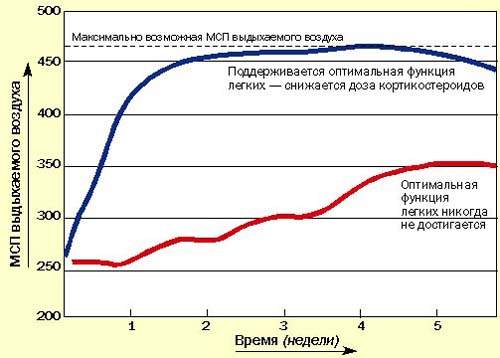 |
| Рисунок 3. Рекомендуется начинать с высоких доз кортикостероидов, а затем постепенно снижать дозу до минимальной (оптимальные значения МСП или ЖЕЛ) |
Последние данные свидетельствуют о том, что назначать кортикостероиды нужно как можно раньше всем астматикам, и не только для контролирования симптомов, но и для предотвращения прогрессирующих структурных повреждений легких, обусловленных хроническим воспалением [2,3]. Это означает, что кортикостероиды следует предпочесть b-агонистам, как только диагноз подтверждается МСП-диаграммой. b-агонисты остаются препаратами резерва на крайний случай.
Возможность альтернативного лечения. Хотя ингалируемые кортикостероиды должны быть краеугольным камнем в лечении астмы, в случаях, трудно поддающихся лечению, можно использовать и некоторые другие препараты. Доказано, что противовоспалительным эффектом обладают теофиллины в достаточно небольших дозах, но надо учитывать в каждом индивидуальном случае их возможное взаимодействие с другими препаратами.
Пожилым пациентам целесообразно назначать ипратропиум. Иногда оказываются эффективными недокромил и кромогликат.
Бронходилятаторы длительного действия, такие как сальметерол, могут облегчать состояние, особенно ночью, блокируя бронхоконстрикторные механизмы. Однако необходимо, чтобы все вышеперечисленные препараты сопровождались применением адекватных доз кортикостероидов.
Техника ингаляции. Нужно добиться, чтобы у пациентов выработались правильные навыки обращения с ингалятором. Врач должен помочь подобрать тот тип ингалятора, который наиболее удобен пациенту, и проверить его работоспособность. Для этого в кабинете врача должен быть полный набор ингаляторов.
Спейсеры. Применяемые вместе с аэрозольными ингаляторами, спейсеры облегчают проникновение препарата в легкие и снижают как накопление его в глотке, так и системное всасывание за счет проглатывания.
Спейсеры помогают координировать выброс препарата со вдохом. Это особенно важно при ингалировании кортикостероидов. Так как кортикостероиды применяются только дважды в день, громоздкий спейсер можно хранить дома.
Спейсеры обеспечивают лучшее накопление препарата в легких, чем распылители. Необходимо правильно их применять: встряхнуть ингалятор, чтобы лекарство смешалось с носителем, и однократно впрыснуть смесь с последующим скорейшим вдохом [4].
Триггерные факторы. Нераспознанные триггерные факторы могут быть и дома, и на работе, и на отдыхе, то есть практически в любом месте. Выявить источник поможет анамнез. Например, при профессиональной бронхиальной астме состояние улучшается во время отпуска и в выходные дни. Отсутствие раздражителя уменьшает или устраняет проявления болезни и снижает необходимость в лекарствах.
Проблемой, которую часто не принимают во внимание, может быть пассивное курение. Такие препараты, как b-блокаторы и нестероидные противовоспалительные средства (НПВС), также могут вызывать астму.
Использование распылителей (небулайзеров) без фоновой кортикостероидной терапии. При лечении острого астматического приступа без назначения пероральных кортикостероидов все еще используют распылители, которые обеспечивают проникновение более высокой дозы b-агонистов. Это действительно снимает бронхоспазм, но поскольку высокая доза b-агонистов не воздействует на сопутствующий воспалительный процесс, необходимо сразу же дать больному кортикостероиды внутрь, чтобы предотвратить нарастание приступа; эффект бронходилятаторов снижается по мере увеличения отека слизистой.
Если тяжесть приступа такова, что требуется небулайзер, необходимо назначить системные кортикостероиды. Даже при умеренном приступе бронходилятаторы сами по себе приносят лишь временное облегчение и есть опасность повторения приступа — возможно, глубокой ночью!
Несвоевременное назначение оральных кортикостероидов. Если не проводить противовоспалительной терапии, у больных нарастает отек слизистой, что приводит к повторению приступов. Такие пациенты часто нуждаются в госпитализации и назначении высоких доз кортикостероидов в течение нескольких дней, прежде чем у них наступит стабилизация состояния.
Пациенты, подверженные быстроразвивающимся приступам, нуждаются в как можно более раннем назначении кортикостероидов и бронходилятаторов. Они должны уметь распознавать ухудшение состояния, всегда иметь под рукой кортикостероиды и знать, как их использовать. Не следует заставлять этих пациентов дожидаться прихода к ним врача (рис. 4).
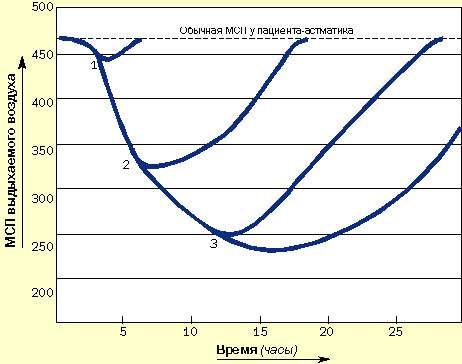 |
| Рисунок 4. Зависимость развития острых приступов от времени назначения кортикостероидов и как результат применения длительных курсов системной кортикостероидной терапии. (1) Кортикостероиды назначены сразу после возникновения приступа: выздоровление наступает быстро. (2) Кортикостероиды назначены через 6 часов: выздоровление замедлено. (3) Кортикостероиды назначены позже чем через 12 часов: приступ тяжелый и длительный, выздоровление наступает медленно |
Пациенты с постепенным развитием приступов могут подождать и посмотреть, помогает ли увеличенная доза ингаляционных кортикостероидов в сочетании с бронходилятаторами.
Неадекватный курс системных кортикостероидов. Иногда назначенные кортикостероиды отменяют до полного купирования приступа, что ведет к сохранению гиперреактивности бронхов и очередному приступу.
Подобная цепь событий может привести пациента к ложному заключению, что у него бронхиальная астма, трудно поддающаяся лечению.
Ситуацию можно исправить длительным курсом кортикостероидов, продолжающимся в течение нескольких дней после стабилизации состояния, и снижением их дозы постепенно до достижения минимальной поддерживающей.
Прекращение наблюдения за пациентом после острого приступа или госпитализации. Трудности возникают при отмене системного кортикостероида и назначении ингаляционного. В этот переходный период необходимо тщательное наблюдение; по достижении стабилизации состояния дозу ингалируемого кортикостероида постепенно снижают до минимально необходимой, чтобы заболевание никак себя не проявляло и функция легких была оптимальной.
Целью последующего лечения становится поддержание наивысшей МСП, достигнутой в больнице после курса системных кортикостероидов.
Консультация, проведенная через некоторое время после выписки, дает хорошую возможность проверить план ведения пациента, выяснить, что не так, и внести соответствующие поправки.
Кашель и хрипы с гнойной мокротой иногда принимают за легочную инфекцию. Однако мокрота больных астмой содержит гораздо больше эозинофилов, чем полиморфных клеток и бактерий. В пожилом возрасте левожелудочковая недостаточность и сердечная астма должны наводить на мысль о предшествующей бронхиальной астме. Будьте осторожны с b-блокаторами!
Внезапная одышка может быть обусловлена пневмотораксом или легочной эмболией. Хрипы встречаются при туберкулезе легких, бронхиальной карциноме или инородном теле и могут быть четко локализованы. Следовательно, у любого пациента с астмой, развившейся во взрослом возрасте, необходимо провести рентгенологическое исследование органов грудной клетки.
После установления диагноза основная цель врача — освободить пациента от проявлений болезни и оптимизировать функцию легких, а также установить контроль за болезнью. Для этого специально обученный медперсонал должен обучать больных и проверять правильность выполнения ими всех назначений.
Конечно, в некоторых случаях это может оказаться затруднительным, однако план предписанных действий способно усвоить абсолютное большинство больных.
Все пациенты должны:
Литература
1. Sears M. R., Taylor D. R. et al. Regular inhaled b-agonist treatment in bronchial asthma. Lancet 1990;336:1491–1396.
2. Tari Haahtela et al. Comparinson of terbutaline with budesonide in newly detected asthma. N Engl J Med 1991;325:388–392.
3. Redingon A. K., Howarth P. H. Airway remodelling in asthma. Thorax 1997;52:310–312.
4. O’Callaghan C., Barry P. Spacer devices in the treatment of asthma. BMJ 1997;314:1061–1062.
Спирометрия при хронической бронхиальной астме
Бочкообразная грудная клетка при хронической бронхиальной астме возникает из-за задержки воздуха в периферических отделах легких, что приводит к постоянному поддержанию грудной клетки в состоянии вдоха. Задержанный воздух не выдыхается и бесполезно занимает большую часть легких (остаточный объем). Это снижает объем воздуха (жизненную емкость легких), входящего в легкое.
Воздух задерживается из-за хронического воспаления, вызывающего отек слизистой периферических бронхиол. При лечении кортикостероидами отек спадает и воздух высвобождается. Это доказывается увеличением ЖЕЛ, определенной спирометрически. МСП может не изменяться (см. рис. 2.)
Обратите внимание!
Приступ астмы
Хроническая астма/ХОЗЛ
Аспирин – пить или не пить, чтобы хорошо и долго жить?
Не один раз на приеме сталкивалась с ситуацией, когда пациент без явной патологии сам себе назначил кардиомагнил (или тромбоАСС, аспирин кардио и пр.), будучи уверенным, что абсолютно всем в его возрасте (то есть «после 45–50 лет») нужна именно такая профилактика заболеваний. Ведь сосед тоже пьет, по телевизору говорят, что нужно, и прочее…
Нужна ли на самом деле?
Дело в том, что современные рекомендации по лечению заболеваний(ССЗ) говорят о необходимости пожизненного приема аспирина теми людьми, которые уже перенесли события. К ним относятся инфаркт, инсульт, транзиторные ишемические атаки. Что же касается применения аспирина людьми, у которых в анамнезе вообще нет никаких заболеваний, в том числе и вышеперечисленных, то на сегодняшний день рутинное назначение аспирина (или других антитромботических препаратов) таким пациентам не рекомендовано отсутствия доказательной базы, подтверждающей прежде всего безопасность такой профилактики у данной категории пациентов.
Наиболее частым побочным эффектом при приеме аспирина является негативное влияние на слизистую оболочку желудка. Также при его длительном приеме увеличивается риск кровотечений различной локализации (, геморроидальных, носовых и пр.), и этим фактом никак нельзя пренебрегать, потому что в определенных ситуациях такие кровотечения могут стать жизнеугрожающими.
В связи с этим перед тем, как назначить пациенту аспирин, врач должен оценить пользу и риск от его приема. Доказано, что у пациентов, перенесших инфаркт или инсульт, польза профилактического приема аспирина перевешивает возможный риск кровотечений, следовательно, его прием рекомендован. И не до конца изучена роль аспиринау лиц, не имеющих в анамнезе ни того, ни другого. Те научные данные, которые мы имеем на сегодняшний день, говорят об отсутствии явной пользы от такой профилактики и при этом о повышении риска возникновения кровотечений различной локализации. Тем не менее, вопрос пока остается малоизученным, продолжаются крупные исследования, и мы ждем их результатов.
Что касается пациентов старших возрастных групп, имеющих факторы риска развития заболеваний (артериальная гипертензия, повышенный уровень холестерина крови и пр.), пациентов с сахарным диабетом, то ситуация примерно та же: до сих пор не было выявлено, что польза от приема аспирина превышает риск возникновения кровотечений у таких пациентов, в связи с чем его прием также не может быть рекомендован рутинно.
Когда еще не нужно принимать аспирин?
— При высоком артериальном давлении.
Потому что его прием может увеличить в данном случае риск возникновения геморрагического инсульта. При наличии гипертонии принимать аспирин нужно только тогда, когдадостигнут адекватный контроль артериального давления.
— При подозрении на инсульт.
Если мы имеем дело с подозрением на инсульт (у человека внезапно развились сильная слабость в руке или ноге, речевые, двигательные нарушения, опущен уголок рта, он не может улыбнуться и пр.), ни в коем случае в данной ситуации нельзя давать аспирин. Не существует объективных признаков, позволяющих однозначно отдифференцировать геморрагический (связанный с кровоизлиянием в мозг) и ишемический (связанный с закупоркой церебральной артерии атеросклеротической бляшкой) тип инсульта. А если инсульт геморрагический, и мы дадим такому человеку аспирин, то страшно представить, чем это может закончиться…
Все, что нужно сделать, если Вы подозреваете у человека инсульт — это уложить его в горизонтальное положение, постараться успокоить и как можно скорее вызвать скорую помощь.
Когда нужно принимать аспирин?
Только тогда, когда его назначил врач, оценивший пользу и риск от его приема и знающий показания к его назначению. Уровень тромбоцитов крови, прием других лекарств из группы нестероидных противовоспалительных препаратов, функция почек также всегда должны учитываться перед назначением данного препарата.
Как правило, всегда показан прием аспирина при ишемической болезни сердца, перенесенном инфаркте, некардиоэмболическом ишемическом инсульте или транзиторной ишемической атаке, при атеросклерозе артерий, стентировании артерий.
Если Вы решили всерьез заняться своим здоровьем, узнать, какие меры по профилактике заболеваний Вам необходимо предпринять, лучше обратиться к терапевту или кардиологу. Доктор назначит Вам необходимые анализы, электрокардиограмму и другие нужные обследования, измерит артериальное давление, выявит, есть ли у Вас факторы риска возникновения заболеваний, рассчитает Ваш риск и на основании этого даст необходимые рекомендации по профилактическим мероприятиям. И, поверьте, самое главное, о чем приходится говорить чаще всего — это об изменении образа жизни. Отказ от курения, нормализация массы тела, регулярные аэробные физические нагрузки (ходьба минимум 30 минут в день), диета с ограничением животных жиров — это основные мероприятия, без которых профилактика ССЗ будет считаться как минимум неполноценной, как максимум — неэффективной. А прием медикаментов может и вообще не понадобится, если все эти меры будут соблюдаться!
Лечение головной боли напряжения и мигрени
Головную боль можно назвать одной из наиболее частых жалоб при обращении к врачу. К самым распространенным первичным цефалгиям относится головная боль напряжения [G44.2]. Выделяют эпизодическую и хроническую формы головной
Головную боль можно назвать одной из наиболее частых жалоб при обращении к врачу.
К самым распространенным первичным цефалгиям относится головная боль напряжения [G44.2]. Выделяют эпизодическую и хроническую формы головной боли напряжения [1, 6].
Диагностические критерии эпизодической головной боли напряжения следующие.
1. Как минимум 10 эпизодов головной боли в анамнезе, отвечающих пунктам 2–4. Число дней, в которые возникала подобная головная боль — менее 15 в месяц (менее 180 в год).
2. Длительность головной боли от 30 мин до 7 дней.
3. Наличие как минимум 2 из нижеперечисленных характеристик:
4. Наличие перечисленных ниже симптомов:
5. Наличие как минимум одного из перечисленных ниже факторов:
Эпизодическая головная боль напряжения встречается у людей всех возрастов независимо от пола.
Чаще всего эпизодическая головная боль провоцируется усталостью, длительным эмоциональным напряжением, стрессом. Механизм ее возникновения связан с длительным напряжением мышц головы.
Боль отличается постоянством и монотонностью, сдавливающим или стягивающим характером. Локализуется в затылочно-шейной области, часто становится диффузной.
Эпизодическая головная боль напряжения проходит после однократного или повторного приема ацетилсалициловой кислоты (АСК) — АСК «Йорк», анопирина, аспирина, упсарина упса, ацифеина (для детей старше 2 лет разовая доза составляет 10–15 мг/кг, кратность приема — до 5 раз в сутки; для взрослых разовая доза варьирует от 150 мг до 2 г, суточная — от 150 мг до 8 г, кратность применения — 2–6 раз в сутки) или ацетаминофена: панадола, парацетамола, проходола, цефекона, далерона, эффералгана (разовые дозы для детей 1–5 лет — 120–240 мг, 6–12 лет — 240–480 мг, взрослым и подросткам с массой тела более 60 кг — 500 г, кратность назначения препарата — 4 раза в сутки), а также после полноценного отдыха и релаксации.
Хроническая головная боль напряжения аналогична эпизодической головной боли, однако средняя частота эпизодов головной боли значительно выше: более 15 дней в месяц (или более 180 дней в год) при длительности заболевания не менее 6 мес.
Хроническая головная боль напряжения возникает на фоне продолжительного стресса и не проходит до тех пор, пока не будет устранена вызвавшая ее причина.
Пациенты с хронической головной болью испытывают тревогу и подавленность. Головная боль всегда двусторонняя и диффузная, но наиболее болезненная зона может мигрировать в течение дня. В основном головная боль тупая, средней степени выраженности, возникает в момент пробуждения и может длиться в течение всего дня, но не усиливается при физической нагрузке. Большинство пациентов описывают головную боль как ежедневную, непрекращающуюся в течение длительного времени с короткими интервалами ремиссий. Очаговая неврологическая симптоматика при этом заболевании не выявляется. Рвота, тошнота, фото- и фонофобия и транзиторные неврологические нарушения не характерны.
Диагноз хронической головной боли напряжения следует рассматривать в качестве диагноза исключения. В первую очередь данное заболевание стоит дифференцировать с мигренью и состоянием, вызванным отменой анальгетиков. Оба заболевания могут сосуществовать с хронической головной болью напряжения. С помощью нейрорадиологических методов исследования следует исключить такую возможную причину повышения внутричерепного давления, как опухоль мозга.
Хроническая головная боль плохо поддается лечению. Большинство пациентов еще до обращения к врачу начинают принимать большое количество обезболивающих препаратов, и поэтому сопутствующим состоянием часто является головная боль вследствие отмены анальгетиков. Использование лекарственных средств, уменьшающих мышечное напряжение, и более сильных анальгетиков не всегда приносит успех, но может привести к осложнениям со стороны желудочно-кишечного тракта. Наиболее эффективным препаратом является амитриптилин в дозе 10–25 мг 1–3 раза в сутки. При его неэффективности целесообразен курс психотерапии.
Мигрень [G43] — это хроническое состояние с непредсказуемыми, остро возникающими приступами головной боли.
Слово «мигрень» имеет французское происхождение («migraine»), а во французский язык оно пришло из греческого. Термин «гемикрания» впервые был предложен Галеном. Первая клиническая характеристика мигрени («гетерокрании») относится ко II в. нашей эры и принадлежит Areteus из Cappadocia. Однако уже в папирусах древних египтян были обнаружены описание типичной мигренозной атаки и рецепты лекарственных средств, применяемых для устранения головной боли.
По данным разных авторов, распространенность мигрени колеблется от 4 до 20% случаев в общей популяции. Мигренью страдают 6–8% мужчин и 15–18% женщин. Она является вторым по частоте видом первичной головной боли после головной боли напряжения. Принято считать, что каждый восьмой взрослый страдает от мигрени. По данным мировой статистики, 75–80% людей хотя бы один раз в жизни испытали приступ мигрени [1, 2, 10, 19].
Мигрень — заболевание лиц молодого возраста, первый приступ отмечается до 40-летнего возраста, а пик заболеваемости приходится на 12–38 лет. До 12 лет мигрень чаще встречается у мальчиков, после пубертата — у лиц женского пола. У женщин приступы мигрени регистрируются в 2–3 раза чаще, чем у мужчин [14].
Немаловажную роль в развитии мигрени играет наследственная предрасположенность. У 50–60% больных родители страдали мигренью. У детей заболевание встречается в 60–90% случаев, если приступы мигрени отмечались у обоих родителей. В 2/3 случаев заболевание передается по линии матери, в 1/3 случаев — по линии отца [17, 23].
Патогенез мигрени чрезвычайно сложен, многие его механизмы до конца не изучены [4, 16, 20, 21, 22, 24]. Для возникновения приступа мигрени необходимо взаимодействие множества факторов: нейрональных, сосудистых, биохимических. Современные исследователи полагают, что церебральные механизмы являются ведущими в возникновении приступа мигрени.
С 1988 г. применяют классификацию и критерии диагностики мигрени, предложенные Международным обществом по изучению головной боли [15, 18]. Таким образом, в настоящий момент выделяют:
80% всех случаев мигрени приходятся на мигрень без ауры. Диагностическими критериями этой формы мигрени являются следующие.
1. Не менее 5 приступов, соответствующих перечисленным в пунктах 2–5 критериям.
2. Длительность головной боли от 4 до 72 ч (без терапии или при неэффективной терапии).
3. Головная боль соответствует не менее чем 2 из нижеперечисленных характеристик:
4. Головная боль сочетается с одним из нижеперечисленных симптомов:
5. Как минимум один фактор из нижеперечисленных:
Мигрень с аурой встречается значительно реже (20% случаев). Диагностические критерии мигрени с аурой идентичны мигрени без ауры, но в первом случае добавляются дополнительные критерии, характеризующие ауру.
В зависимости от характера фокальных неврологических симптомов, возникающих во время ауры, выделяют несколько форм мигрени: наиболее часто встречающуюся — офтальмическую (ранее «классическую») и редкие (2% случаев мигрени с аурой) — гемиплегическую, базилярную, офтальмоплегическую и ретинальную.
Факторы, провоцирующие возникновение приступа мигрени, многообразны: психотравмирующая ситуация, страх, положительные или отрицательные эмоции, шум, яркий мерцающий свет, переутомление, недосыпание или избыточный сон, голод, употребление в пищу шоколада, какао, кофе, орехов, сыра, красного вина, пребывание в душном помещении, резкие запахи, определенные климатические и метеорологические условия, применение препаратов, активно влияющих на состояние сосудов (нитроглицерин, гистамин и др.), менструальный цикл [24].
Клинические проявления мигрени подразделяются на 4 фазы, большинство из которых незаметно переходят одна в другую на протяжении всей атаки. Продромальную фазу испытывают 50% больных. Симптомы ее возникают скрытно и развиваются медленно на протяжении 24 ч. Клиническая картина включает в себя изменения эмоционального состояния (обостренное или сниженное восприятие, раздражительность), снижение работоспособности, тягу к конкретной пище (особенно сладкой), чрезмерную зевоту. Часто эти симптомы удается выявить только при целенаправленном опросе пациента.
Зрительные симптомы являются наиболее часто описываемыми нарушениями мигренозного приступа с аурой.
В типичных случаях пациент видит вспышки света (фотопсии), мерцающие зигзагообразные линии. Сенсорные симптомы могут возникать в виде покалывания и онемения в руках, дисфазии и других речевых расстройств, которые вызывают сильный стресс у больного. Эти симптомы длятся не менее 4 и не более 60 мин и фаза головной боли возникает не позже, чем через 60 мин после ауры. Головная боль пульсирующего характера, чаще локализуется в одной половине головы, но может быть и двусторонней, усиливается при движении и физическом напряжении, сопровождается тошнотой и рвотой, свето- и шумобоязнью. Является наиболее стойким симптомом мигрени и длится от 4 до 72 ч. В постдромальной фазе, длительностью до 24 ч, после стихания головной боли, больные испытывают сонливость, вялость, разбитость, боль в мышцах. У некоторых пациентов возникают эмоциональная активация, эйфория.
К осложнениям мигрени относят мигренозный статус и мигренозный инсульт. Мигренозный статус — это серия тяжелых, следующих друг за другом приступов, сопровождающихся многократной рвотой, со светлыми промежутками, длящимися не более 4 ч, или 1 тяжелый и продолжительный приступ, продолжающийся более 72 ч, несмотря на проводимую терапию. Риск возникновения инсульта у пациентов, страдающих мигренью без ауры, не отличается от такового в популяции. При мигрени с аурой мозговой инсульт возникает в 10 раз чаще, чем в популяции. При мигренозном инсульте один или более симптомов ауры не исчезают полностью через 7 дней, а нейрорадиологические методы исследования выявляют картину ишемического инсульта.
В межприступном периоде в неврологическом статусе больных мигренью, как правило, отклонений не наблюдается. В 14–16% случаев, по данным О. А. Колосовой (2000), имеют место нейроэндокринные проявления гипоталамического генеза (церебральное ожирение, нарушения менструального цикла, гирсутизм и т. п.), у 11–20% больных в соматическом статусе выявляется патология желудочно-кишечного тракта.
Данные дополнительных методов исследований не информативны. С помощью исследования, проведенного нейрорадиологическими методами в межприступный период, патологических изменений обнаружить не удается. Лишь при частых и тяжелых приступах мигрени в веществе головного мозга выявляют участки пониженной плотности, расширение желудочков мозга и субарахноидальных пространств [3, 11].
При анализе характера приступа мигрени и критериев его диагноза необходимо обращать внимание на такие симптомы, как:
Данные симптомы требуют детального неврологического обследования и проведения нейрорадиологических методов исследования (КТ, МРТ) для исключения текущего органического процесса.
Дифференциальный диагноз мигрени проводят: с головной болью при органическом поражении мозга (опухоль, травма, нейроинфекция); головной болью при синуситах; головной болью при артериальной гипертензии; головной болью напряжения и пучковой (кластерной) головной болью; эпилепсией; абузусной головной болью.
Методы лечения мигрени подразделяется на превентивную терапию и терапию острого болевого приступа. Превентивная терапия направлена на снижение частоты, длительности и тяжести приступов и применяется у больных в следующих случаях:
При проведении профилактического курса препараты рекомендуется принимать ежедневно, а лечение считается успешным, если частота, длительность и интенсивность приступов снижаются на 50% или более. Если в течение нескольких месяцев (обыкновенно 6 или более) приступы мигрени хорошо контролируются или не беспокоят пациента, дозы препаратов постепенно сокращаются и решается вопрос о целесообразности их дальнейшего применения.
При выборе лекарственных препаратов опираются на патогенез мигрени, а также учитывают наличие сопутствующих заболеваний у пациента и побочных действий лекарственных средств. Препараты следует назначать в минимальных дозировках, постепенно увеличивая их до максимально рекомендуемых, либо до появления побочных реакций или достижения терапевтического эффекта. Курс профилактической терапии может длиться от 2 до 6 мес.
Наиболее широко используемыми лекарственными средствами являются:
Для профилактической терапии используются как лекарственные, так и немедикаментозные методы лечения. Например, диета с ограничением продуктов, содержащих тирамин (красное вино, шоколад, сыр, орехи, цитрусовые и др.); лечебная гимнастика с акцентом на шейный отдел позвоночника; массаж воротниковой зоны; водные процедуры; иглорефлексотерапия; биологическая обратная связь, психотерапия.
Для купирования приступов мигрени используют 3 группы препаратов [4, 8, 12, 19]. Оценивается эффективность препарата, согласно международным стандартам, по следующим критериям:
Первая группа. При легких и средних по интенсивности приступах могут быть эффективны парацетамол, ацетилсалициловая кислота и ее производные, а также комбинированные препараты: седальгин, пенталгин, спазмовералгин и др. Действие препаратов этой группы направлено на уменьшение нейрогенного воспаления, подавление синтеза модуляторов боли (простагландинов, кининов и др.), активацию антиноцицептивных механизмов мозгового ствола. При их применении необходимо помнить о противопоказаниях к назначению ацетилсалициловой кислоты: наличие заболеваний желудочно-кишечного тракта, склонность к кровотечениям, повышенная чувствительность к салицилатам, аллергия, а также о возможности развития абузусной головной боли при длительном и бесконтрольном применении этих средств.
Вторая группа. Препараты дигидроэрготамина (редергин, дигидроэрготамин, дигидергот) обладают мощным сосудосуживающим действием, благодаря влиянию на серотониновые рецепторы, локализованные в сосудистой стенке, предотвращают нейрогенное воспаление и тем самым купируют мигренозную атаку. Дигидроэрготамин является неселективным агонистом серотонина и обладает также допаминергическим и адренергическим действием. При передозировке или повышенной чувствительности к эрготаминовым препаратам возможны загрудинная боль, боли и парестезии в конечностях, рвота, понос (явления эрготизма). Наименьшими побочными действиями обладает назальный спрей дигидроэрготамина. Достоинством данного препарата является удобство применения, быстрота действия и высокая эффективность (75% приступов купируются в течение 20–45 мин) [7].
Третья группа. Селективные агонисты серотонина (имигран, нарамиг, зомиг). Обладают избирательным воздействием на серотониновые рецепторы мозговых сосудов, блокируют выделение субстанции Р из окончаний тройничного нерва и предотвращают нейрогенное воспаление. Побочными явлениями агонистов серотониновых рецепторов являются: чувство покалывания, давления, тяжести в разных частях тела, гиперемия лица, усталость, сонливость, слабость. Противопоказаны при сопутствующей патологии сердечно-сосудистой системы и диабете [9].
Существенным для проведения эффективной терапии селективными агонистами серотонина является соблюдение следующих правил [4]:
Имигран (суматриптан) применяется в таблетированной (50, 100 мг), инъекционной форме по 6 мг для подкожного введения и в виде назального спрея. Эффективность имиграна при любой форме применения равна 70–80%. Работоспособность пациентов восстанавливается, как правило, через 1–2 ч при подкожном и через 3–4 ч при пероральном применении, причем независимо от дозы [4, 5].
Нарамиг (наратриптан) — таблетки по 2,5 мг. Поскольку у наратриптана период полувыведения равен 5 ч, препарат может быть эффективен при купировании продолжительных мигренозных атак. «Возврат головной боли» в ближайшие 24 ч отмечается в меньшем проценте случаев, чем при приеме имиграна [6, 13].
Зомиг (золмитриптан) — таблетки по 2,5 мг. Эффект наступает через 20–30 мин. Преимуществами золмитриптана по сравнению с другими триптанами являются: более высокая клиническая эффективность при пероральном приеме, более быстрое достижение терапевтического уровня препарата в плазме крови, меньшее вазоконстрикторное влияние на коронарные сосуды [9].
Препараты второй и третьей групп являются в настоящее время базовыми средствами, используемыми для купирования мигренозных приступов.
Превентивная терапия, а также эффективное и безопасное купирование приступов головной боли у пациентов с частыми приступами позволяют в значительной степени улучшить качество жизни больных с мигренью.
По вопросам литературы обращайтесь в редакцию.
М. Ю. Дорофеева
Е. Д. Белоусова, кандидат медицинских наук
МНИИ педиатрии и детской хирургии МЗ РФ, Детский научно-практический противосудорожный центр МЗ РФ, Москва




