Что такое стеноз почечных артерий? Причины возникновения, диагностику и методы лечения разберем в статье доктора Илларионовой И. Н., сосудистого хирурга со стажем в 6 лет.
Определение болезни. Причины заболевания
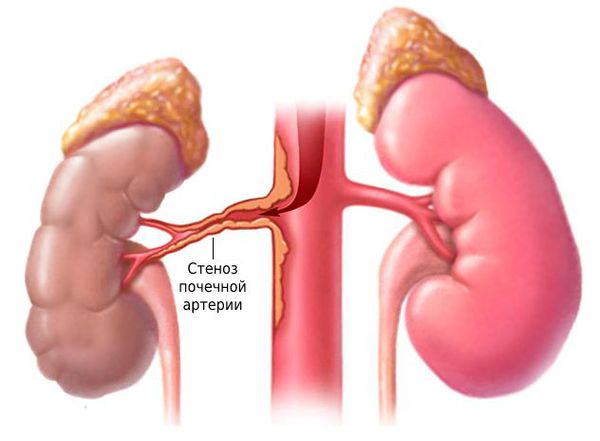
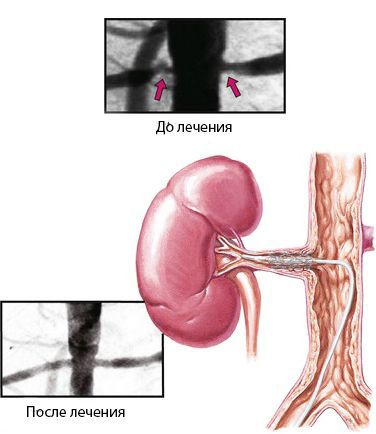
Стеноз почечной артерии — это патология, при которой сужается просвет и уменьшается кровоток в одной или обеих почечных артериях и их ветвях. Заболевание часто приводит к устойчивому повышению артериального давления.
Причины заболевания
Примерно 90 % случаев стеноза почечной артерии вызваны атеросклерозом. Он может быть изолированным или поражать несколько сосудов. Чаще всего причиной атеросклеротического стеноза становятся бляшки, которые образуются на стенке аорты и разрастаются в просвет почечной артерии.
Другие причины, такие как системные васкулиты, частичное закрытие артерий тромбом и опухолевые заболевания, к стенозу почечной артерии приводят значительно реже.
Распространённость
Факторы риска
Симптомы стеноза почечных артерий
Первое время стеноз почечной артерии протекает без выраженных симптомов. В дальнейшем болезнь проявляется в зависимости от её причины и возраста, в котором она началась.
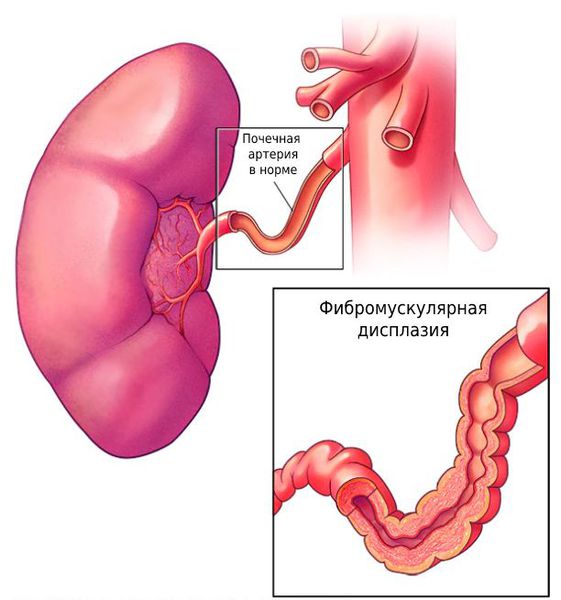
Симптомы при фибромускулярной дисплазии
Фибромускулярной дисплазией преимущественно страдают женщины 30–50 лет. Болезнь чаще всего протекает со вторичной злокачественной гипертонией, то есть повышением артериального давления выше 180/120 и повреждением внутренних органов.
Симптомы при атеросклеротическом поражении почечной артерии
Заболевание зачастую развивается у пациентов старше 55 лет. Оно сопровождается тяжёлой артериальной гипертонией, устойчивой к лечению, и ухудшением работы почек.
В запущенной стадии при отёке лёгких появляется кашель с мокротой, окрашенной кровью, бледность и цианоз кожи, выраженная потливость. Пульс учащается, артериальное давление повышается. Могут появиться выраженные свистящие хрипы (сердечная астма) и признаки правожелудочковой недостаточности, например набухание вен шеи и отёки рук и ног.
Патогенез стеноза почечных артерий
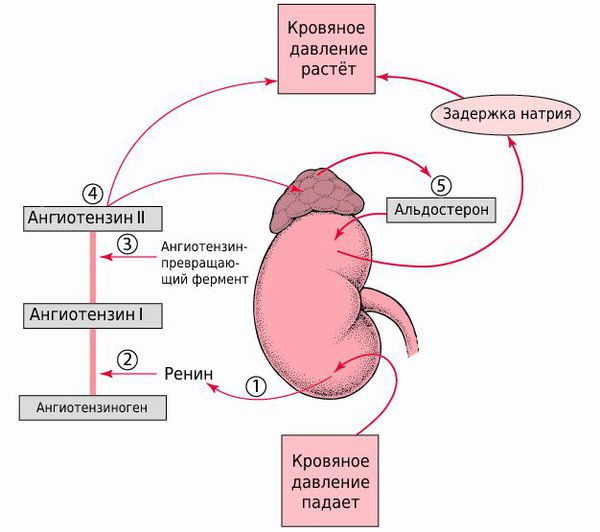
При стенозе почечной артерии уменьшается кровоснабжение тканей почек и активируется ренин-ангиотензин-альдостероновая система (РААС) — гормональные факторы, регулирующие объём крови и кровяное давление. При этом почка длительное время продолжает стабильно работать.
Активация ренин-ангиотензин-альдостероновой системы ускоряет развитие хронической почечной недостаточности.
При дальнейшем развитии стеноза резко снижается приток крови, что приводит к декомпенсации РААС. В результате уменьшается кровенаполнение клубочков, скорость клубочковой фильтрации и растёт уровень сывороточного креатинина — остаточного продукта, который образуется в мышцах при разрушении креатина. Он входит в цикл, снабжающий организм энергией для сокращения мышц. После интенсивной физической нагрузки креатинфосфат превращается в креатин, а затем — в креатинин, который фильтруется в почках и выделяется с мочой. Он почти полностью выводится почками, поэтому его уровень в крови показывает их функцию.
При последующем развитии стеноза почечной артерии:
Классификация и стадии развития стеноза почечных артерий
Стеноз почечной артерии относится к реноваскулярным, то есть почечно-сосудистым заболеваниям.
По причине развития выделяют:
Стеноз почечных артерий подразделяется на односторонний и двусторонний, гемодинамически значимый и незначимый.
При гемодинамически значимом стенозе артерия сужается более чем на 70 %, кровоток ускоряется.
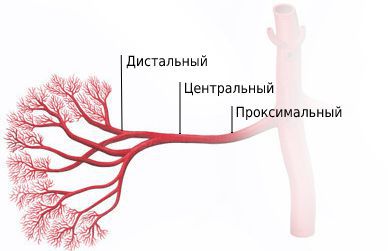
Стеноз может поражать проксимальный отдел артерии, центральный и дистальный или охватывать всю артерию, а также распространяться на её ветви. Обычно развивается проксимальный стеноз почечной артерии.
Стадии артериальной гипертензии при стенозе почечной артерии:
Осложнения стеноза почечных артерий
К осложнениям стеноза почечной артерии относятся: прогрессирующая нефропатия, отёк лёгких, синдром Пикеринга и артериальная гипертензия.
Нефропатия
Основное осложнение стеноза почечной артерии — прогрессирующая нефропатия. При заболевании уменьшаются размеры и ухудшается работа почки, затем она полностью перестаёт выполнять свои функции.
Прогрессирующая почечная недостаточность приводит к сердечно-сосудистым осложнениям, таким как устойчивая сердечная недостаточность и внезапный отёк легких.
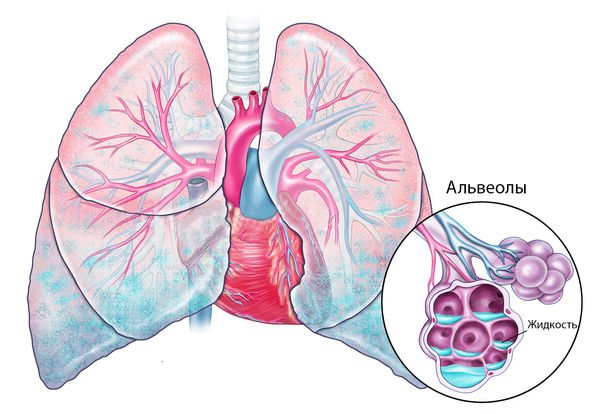
Отёк лёгких
Патогенез отёка лёгких недостаточно изучен. Предполагают три основных механизма его развития: задержка в организме натрия, развитие дисфункции сердца и повреждение барьера между воздухом в альвеолах и кровью.
При одностороннем стенозе почечных артерий функции повреждённой почки берёт на себя противоположная, увеличивая выделение натрия.
Пациенты с двухсторонним стенозом почечных артерий склонны к избыточному накоплению воды во внеклеточном пространстве с развитием отёка лёгких. Патология развивается из-за сниженного давления в почечных артериях, что приводит к росту уровня ангиотензина II, который, в свою очередь, вызывает рост артериального давления и задержку натрия.
Синдром Пикеринга
Впервые описан в 1998 году Томасом Пикерингом и его коллегами. Включает гипертонию, внезапный отёк лёгких и двусторонний стеноз почечной артерии.
Артериальная гипертензия
При стенозе почечной артерии часто наблюдается устойчивая к терапии артериальная гипертензия. Она приводит к дисфункции и выраженному увеличению объёма и массы левого желудочка. Возникающая диастолическая дисфункция (нарушение расслабления) способствует увеличению диастолического давления левого желудочка, давления в полости левого предсердия и лёгочных венах. Кроме диастолической дисфункции, при отёке лёгких снижается систолическая функция левого желудочка. Это приводит к тому, что уменьшается кровенаполнение почек, и в результате возникает порочный круг.
Диагностика стеноза почечных артерий
Ультразвуковое триплексное ангиосканирование — неинвазивный, безрадиационный и доступный метод диагностики, который может применяться при почечной недостаточности и аллергии на контрастное вещество. Позволяет оценить строение почечных артерий и движение крови по сосудам.
Недостатки метода: требует много времени, точность результатов сильно зависит от квалификации оператора, процедура технически сложна для пациентов с ожирением и метеоризом.
Компьютерная томографическая ангиография — отличный метод визуализации почечных артерий и окружающих структур. Позволяет быстро и с высокой точностью обнаружить стеноз почечной артерии.
Недостатки метода: использование йодированного контраста и ионизированного излучения. Кроме того, выраженный кальциноз почечной артерии может скрывать сужение просвета сосуда и затруднять оценку стеноза.
Магнитно-резонансная ангиография — неинвазивный метод, который позволяет получить качественные анатомические изображения почечных артерий и окружающих структур. Его точность в меньшей степени, чем ультразвукового триплексного ангиосканирования, зависит от оператора. Исследование высокочувствительно и специфично для обнаружения стеноза почечной артерии.
Недостатки метода: высокая цена; противопоказана пациентам с ферромагнитными имплантатами и нарушением функции почек со скоростью клубочковой фильтрации м² ; не используется для оценки стеноза при установленном стенте.
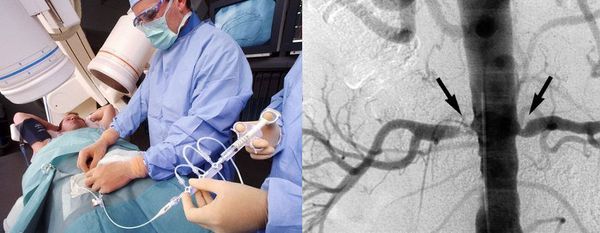
Катетерная ангиография почек — оптимальный метод диагностики стеноза почечной артерии. Позволяет измерить движение крови по сосудам и при необходимости восстановить проходимость артерии.
Недостатки метода: инвазивность, использование йодсодержащего контраста и ионизированного излучения, риски кровотечения, расслоения и повреждения сосудов, иногда требующие хирургического вмешательства.
Лабораторные исследования
При лабораторном обследовании можно выявить синдром почечной недостаточности — снижение скорости клубочковой фильтрации с умеренной азотемией (повышенным уровнем в крови азотистых продуктов обмена, выводимых почками).
Лечение стеноза почечных артерий
Цель лечения — контролировать уровень артериального давления и сохранить функции почек. Оно включает медикаментозную терапию, хирургическую реконструкцию и восстановление проходимости артерий (реваскуляризацию) со стентированием или без него.
Медикаментозная терапия
Для лечения гипертензии, вызванной стенозом почечной артерии, применяют:
Если нет противопоказаний, то предпочтительны ИАПФ или БРА. Однако высокое давление при стенозе почечной артерии часто плохо снижается и приходится назначать несколько антигипертензивных средств. Дозировку и препараты врач подбирает индивидуально. Также пациентам может быть назначен аспирин и гиполипидемические препараты, чтобы замедлить развитие атеросклероза.
Образ жизни
Пациентам с атеросклеротическим стенозом почечной артерии важно отказаться от курения, контролировать вес и уровень сахара в крови.
Хирургические методы
Хирургическая реваскуляризация включает:
Прогноз. Профилактика
Эффективность лечения и прогноз зависят от коррекции факторов риска: избыточного веса, уровня холестерина и сахара в крови. Своевременная диагностика и приём лекарств, назначенных врачом, позволяют снизить риск развития почечных и сердечно-сосудистых осложнений. Вероятность, что они могут возникнуть без лечения, крайне высока, поэтому пациентам необходимо ежегодно проходить обследование.
Основные методы профилактики:
Применение ингибиторов АПФ в клинической практике
Ингибиторы ангиотензинпревращающего фермента (АПФ) применяются в кардиологии в течение почти 30 лет. За это время благодаря большому количеству крупных исследований была доказана эффективность этой группы препаратов при лечении артериальной гипертонии
Ингибиторы ангиотензинпревращающего фермента (АПФ) применяются в кардиологии в течение почти 30 лет. За это время благодаря большому количеству крупных исследований была доказана эффективность этой группы препаратов при лечении артериальной гипертонии (АГ), сердечной недостаточности (СН), дисфункции левого желудочка (ЛЖ), гипертонической и диабетической нефропатии.
В настоящее время к ингибиторам АПФ относятся большое количество лекарственных средств, различающихся по физико-химическим и фармакокинетическим свойствам. В зависимости от характера группы, которая непосредственно связывается с активным центром АПФ, все ингибиторы АПФ делятся на три категории: сульфгидрильную (беназеприл, каптоприл), карбоксильную (цилазаприл, эналаприл, лизиноприл, периндоприл, рамиприл, спираприл, трандолаприл) и фосфонильную (фозиноприл). Большинство ингибиторов АПФ, кроме каптоприла и лизиноприла, являются пролекарствами и превращаются в активные метаболиты в печени или желудочно-кишечном тракте. Пролекарства более липофильны и после превращения в активные метаболиты лучше проникают в органы-мишени, однако у пациентов с заболеваниями и нарушениями функции печени наблюдается торможение активации ингибиторов АПФ при первом прохождении через нее, что необходимо учитывать при выборе препарата.
В основном ингибиторы АПФ и их метаболиты выводятся почками, а такие из них, как фозиноприл, трандолаприл и спираприл, — как с мочой, так и с желчью.
Капотен обладает небольшой продолжительностью действия, в связи с чем его необходимо назначать 3–4 раза в сутки, остальные ингибиторы АПФ характеризуются пролонгированным действием и их можно назначать 2 или 1 раз в сутки.
Все ингибиторы АПФ обладают одинаковым механизмом действия — ингибированием АПФ что приводит к уменьшению образования ангиотензина II из ангиотензина I благодаря снижению его уровня в крови и тканях. При этом снижаются как секреция альдостерона и вазопрессина, так и активность симпатической нервной системы. Ингибиторы АПФ подавляют кининазу II, вследствие чего происходит торможение распада брадикини-
на — мощного стимулятора высвобождения эндотелийзависимых факторов релаксации: оксида азота, эндотелийзависимого фактора гиперполяризации и простациклина.
Основные терапевтические эффекты ингибиторов АПФ следующие:
Исследования CONSENSUS и SOLVD продемонстрировали, что назначение эналаприла приводит к достоверному уменьшению смертности у пациентов с хронической СН, независимо от функционального класса. В исследовании CONSENSUS принимали участие пациенты с IV функциональным классом. Включение в стандартную схему терапии дигоксином и диуретиками эналаприла через 6 мес привело к значительному уменьшению смертности [7]. Результаты исследования SOLVD подтвердили благоприятное влияние эналаприла на выживаемость при хронической недостаточности кровообращения у больных II–III функционального класса [8]. В рамках исследования SOLVD также было доказано снижение смертности и прогрессирования СН у пациентов, перенесших инфаркт миокарда с дисфункцией ЛЖ без клинических признаков СН. Улучшение выживаемости в ранние сроки после инфаркта миокарда (на 3–15-й день заболевания) было продемонстрировано в ходе исследования AIRE (терапия рамиприлом), в которое были включены пациенты с клиническими признаками СН, а также исследований SAVE (терапия капотеном) и TRACE (терапия трандолаприлом), проводившихся у пациентов с систолической дисфункцией ЛЖ.
Применение ингибиторов АПФ в группе больных высокого риска
Долгое время обсуждалась проблема целесообразности назначения ингибиторов АПФ пациентам с сердечно-сосудистыми заболеваниями без СН. Окончательный ответ на этот вопрос дали исследования HOPE (терапия рамиприлом) и EUROPA (терапия периндоприлом), которые убедительно доказали пользу применения ингибиторов АПФ у пациентов с коронарной болезнью сердца и другими формами атеросклероза.
В исследовании HOPE [9] принимали участие пациенты старше 55 лет с различными формами атеросклероза (коронарная болезнь сердца, поражение периферических артерий, инсульт) или сахарным диабетом, имевшие, по крайней мере, еще один фактор риска. При этом клинические признаки СН или снижения фракции выброса ЛЖ отсутствовали. В течение 5 лет больным назначались рамиприл или плацебо. Лечение рамиприлом достоверно уменьшило риск развития смерти от сердечно-сосудистых причин, инфаркта миокарда и инсульта. Снижение АД в группе рамиприла было сравнительно небольшим, поэтому улучшение отдаленного исхода у пациентов с высоким риском развития ССО, по результатам этого исследования, нельзя объяснить только гипотензивным действием препарата.
Доказательства эффективности ингибиторов АПФ у больных стабильной ишемической болезнью сердца удалось получить в ходе исследования EUROPA, в которое были включены пациенты, страдавшие стабильной коронарной болезнью сердца без СН. В течение 4 лет им проводилось лечение периндоприлом или плацебо, которые добавлялись к стандартной схеме терапии. На фоне приема периндоприла снизились показатели смертности от сердечно-сосудистых заболеваний, инфаркта миокарда и число внезапных смертей [10].
Полученные результаты, возможно, связаны с наличием каких-то дополнительных эффектов, например с улучшением эндотелиальной функции, так как в настоящее время дисфункция эндотелия рассматривается в качестве раннего фактора риска развития атеросклероза и атеротромбоза [10].
Таким образом, суммируя все вышесказанное, можно отметить, что ингибиторы АПФ представляют собой класс препаратов, которые хорошо переносятся пациентами, вызывают наименьшее количество побочных эффектов, метаболически нейтральны. Кроме того, их эффективность убедительно доказана благодаря огромному количеству крупных исследований, проводившихся среди больных с сердечно-сосудистой патологией.
Литература
Д. В. Небиеридзе, доктор медицинских наук, профессор
Ф. С. Папова, кандидат медицинских наук
ГНИЦПМ, Москва
Ингибиторы ангиотензинпревращающего фермента в кардиологической практике
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
И нгибиторы ангиотензинпревращающего фермента (иАПФ) применяются в клинической практике c 1975 года и к настоящему времени стали одной из наиболее часто используемых групп лекарственных средств для лечения артериальной гипертензии (АГ) и сердечной недостаточности (СН). В патогенезе этих состояний важную роль играет активация двух нейрогуморальных систем организма: ренин–ангиотензин–альдостероновой (РААС) и симпато–адреналовой (САС).
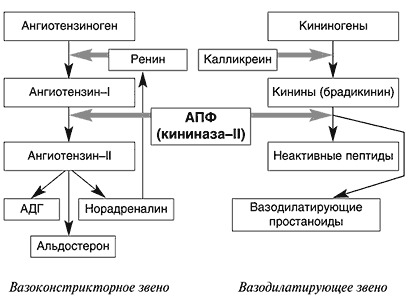
Процесс активации вызывается такими неблагоприятными факторами, как снижение сердечного выброса, ишемия жизненно важного органа, потеря натрия и воды, значимое изменение рH и др. В результате происходит образование биологически активного вещества–ангиотензина II, которое является мощным вазоконстриктором, стимулирует выброс альдостерона, а также способно повышать активность САС (стимулировать выброс норадреналина). Норадреналин, в свою очередь, может активировать РААС (стимулирует синтез ренина). В конечном итоге повышение активности этих двух систем организма, вызывая мощную вазоконстрикцию, увеличение ЧСС, сердечного выброса, поддерживает функцию кровообращения на оптимальном уровне, сохраняет гомеостаз организма. В норме активации прессорных систем организма (РААС и САС) «противостоит» действие депрессорной системы (калликреин–кининовой: ключевое звено–брадикинин), вызывающее системную вазодилатацию. Однако при длительном действии различных патологических факторов, описанных выше, нормальная регуляция нарушается и преобладают эффекты прессорных систем.
иАПФ тормозят эффекты прессорных систем и одновременно являются активаторами депрессорных систем.
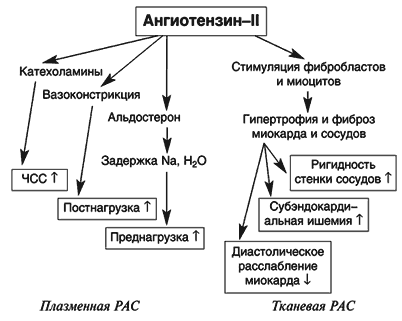
Основные эффекты иАПФ обусловлены блокадой ангиотензинпревращающего фермента (рис. 1): устранение вазопрессорного, антидиуретического и антинатрийуретического действия ангиотензина II, усиление сосудорасширяющего, диуретического и натрийуретического действия брадикинина и других эндогенных вазодилататоров (простагландинов J2 и E2, натрийуретического пептида, эндотелиального фактора релаксации), а также опосредованной блокадой активности САС путем торможения синтеза норадреналина. В середине 80–х годов выявлены локальные гормональные системы (прежде всего РААС) в различных органах и тканях организма. Активация тканевых РААС происходит параллельно плазменной (циркулирующей), но действие этих систем различается. Плазменная РААС активируется быстро, но оказывает кратковременные эффекты (рис. 2). Активность тканевых РААС нарастает постепенно, однако сохраняется долговременно. Синтезирующийся в миокарде ангиотензин II активирует протоонкогены и стимулирует гипертрофию и фиброз мышечных волокон. Кроме того, он активирует локальный синтез норадреналина. Аналогичные изменения наблюдаются в гладкой мускулатуре периферических сосудов и приводят к её гипертрофии (рис. 2).
Рис. 1. Нейрогуморальные взаимодействия: ренин-ангиотензин-альдостероновая, симпато-адреналовая и калликреин-кининовая системы
Рис. 2. Системные и локальные эффекты ренин-ангиотензин-альдостероновой системы
V. Dzau выделяет следующие сердечно–сосудистые эффекты иАПФ:
– системная артериальная вазодилатация (уменьшение посленагрузки на левый желудочек) без развития рефлекторной тахикардии;
– венозная вазодилатация (увеличение емкости венозной системы, уменьшение преднагрузки);
– предотвращение дилатации желудочков (кардиопротекция);
– обратное развитие гипертрофии желудочков (кардиопротекция) и стенки артерий и артериол;
– подавление реперфузионных желудочковых аритмий (кардиопротекция);
– предотвращение развития толерантности к нитратам и потенцирование вазодилатирующего действия нитратов;
– уменьшение задержки натрия и воды, увеличение содержания калия.
Первые клинические испытания каптоприла (с 1975 года) показали высокую эффективность при АГ, в том числе резистентной к другим методам лечения. Коммерческий успех каптоприла стимулировал усилия других компаний по поиску новых иАПФ. В 1980 году был синтезирован эналаприл – иАПФ следующего поколения, характеризующегося пролонгированным действием. В настоящее время разрешено клиническое применение более 10 препаратов этой группы различных фирм–производителей: эналаприл, рамиприл, лизиноприл, цилазаприл, квинаприл, беназеприл, периндоприл и т.д. Наряду со свойствами, характерными для каптоприла, они имеют отличительные черты. Для большинства из них характерен пролонгированный эффект, более высокая ингибирующая АПФ активность, различные фармакокинетические свойства. Однако фармакодинамические эффекты этих препаратов сходны между собой.
Классификация (общепринятой не существует) основана на химической структуре части молекулы, связывающейся с ангиотензинпревращающим ферментом. Препараты подразделяют на 3 группы:
– иАПФ, содержащие сульфгидрильную группу (каптоприл);
– иАПФ, содержащие карбоксильную группу или карбоксиалкилдипептиды (лизиноприл, эналаприл, рамиприл, периндоприл, цилазаприл, беназеприл, квинаприл, трандолаприл, спираприл);
– иАПФ, содержащие фосфорильную группу (фозиноприл).
Реальное клиническое значение имеют некоторые особенности фармакокинетики иАПФ: биодоступность, биотрансформация (действует препарат самостоятельно, т.е. является ли он активным веществом или пролекарством, которое превращается в организме в активные метаболиты), пути элиминации и продолжительность торможения активности ангиотензинпревращающего фермента.
Каптоприл действует как активный препарат, биодоступность – 60%, быстро всасывается, но всасывание его уменьшается на 30–40% при одновременном приеме пищи, поэтому его следует принимать натощак, за 1–1,5 часа до приема пищи. Максимум концентрации в крови наступает через 1 час после перорального приема. Активность каптоприла (то есть самого вещества) делает реальным его применение в качестве препарата «скорой помощи», в частности, для купирования гипертонических кризов при сублингвальном приеме. Эффект отмечается через 15–20 минут. Каптоприл имеет короткий период полувыведения из плазмы (2 часа), поэтому требует 3–4–кратного приема в сутки, выделяется преимущественно с мочой.
Все карбоксиалкилдипептиды превосходят каптоприл по длительности действия, так как имеют более длительный период полувыведения и поэтому применяются 1–2 раза в сутки. Они меньше связываются с белками пищи, следовательно, их можно принимать независимо от еды. Все карбоксиалкилдипептиды за исключением лизиноприла являются пролекарствами, т.е. для образования активных метаболитов требуется биотрансформация этих препаратов в печени. Из этого следует, что данные препараты необходимо с осторожностью применять у лиц с печеночной недостаточностью, а также то, что они не могут быть использованы в качестве средств «скорой помощи». Основной путь элиминации практически всех иАПФ, а также их активных и неактивных метаболитов – почечная экскреция. Поэтому у больных с явной или скрытой почечной недостаточностью, особенно у пожилых пациентов, дозы иАПФ должны быть уменьшены. До начала терапии и в течение первой недели лечения иАПФ желательно контролировать не только уровень креатинина, но и скорость клубочковой фильтрации (проба Реберга). Кроме этого, необходимо не допускать развития гипотензии (АД менее 100/60 мм рт.ст.), не назначать одновременно другие гипотензивные препараты (в частности, диуретики и т.д.).
В отличие от большинства иАПФ новые препараты – спираприл, фозиноприл, трандолаприл – преимущественно инактивируются печенью и выводятся с желчью через кишечник. Следовательно, являются весьма перспективными препаратами для лечения лиц пожилого и старческого возраста, так как у этого контингента больных нередко имеется явная или скрытая почечная недостаточность.
Эналаприл – «пролекарство», в печени превращается в активное вещество – эналаприлат. Биодоступность – 40%, не изменяется при приеме пищи. Максимальная концентрация эналаприлата – через 2–4 часа, период полувыведения – 11 часов. Поражение печени или почек увеличивает время начала и длительность действия.
Периндоприл. При пероральном приеме происходит быстрое всасывание препарата. Биодоступность – 65–70%. Прием пищи замедляет метаболизм периндоприла. Активная форма – периндоприлат, его максимальная концентрация в плазме достигается через 3–4 часа после приема препарата, выводится из организма через почки.
Цилазаприл. Одновременный прием препарата с пищей несколько замедляет абсорбцию. Биодоступность – 45%. В печени цилазаприл метаболизируется в активную форму – цилазаприлат. Выводится – почками, период полуэлиминации составляет 7,5 часов.
Лизиноприл. Его выдающимися фармакокинетическими особенностями являются очень низкая жирорастворимость, отсутствие метаболизма в организме (вследствие низкой липофильности) и экскреция с мочой. Биодоступность – 30–50% и, вероятнее всего, что прием пищи на нее не влияет. Пик концентрации в крови отмечается через 6 часов после приема препарата. Период полувыведения – 12,5 часов.
Хинаприл=квинаприл быстро абсорбируется из желудочно–кишечного тракта, и прием пищи не влияет на абсорбцию. В печени препарат гидролизуется в квинаприлат. Пиковая концентрация квинаприлата в крови регистрируется через 2 часа после перорального приема. Выводится – через почки.
Беназеприл. Биодоступность – 17%. В печени превращается в беназеприлат. Период полувыведения – 11 часов. Экскретируется почками.
Рамиприл. Одновременный прием пищи не влияет на абсорбцию препарата. В печени происходит превращение в рамиприлат, который выводится в основном почками с клиренсом 80–130 мл/мин. Частично экскретируется с калом.
Спираприл в печени гидролизуется в спираприлат, выделяется преимущественно с желчью.
Трандолаприл в печени превращается в активную форму – трандолаприлат, экскретируется преимущественно с желчью.
Фозиноприл при приеме внутрь медленно всасывается, биодоступность 36% и прием пищи снижает ее до 20%, является «пролекарством», в печени метаболизируется в фозиноприлат, который экскретируется почти равномерно в мочу и желчь. Однако при наличии почечной недостаточности фозиноприл фактически полностью элиминируется через желудочно–кишечный тракт, что практически полностью снимает ограничения на его применение у больных с нарушенной функцией почек.
Побочные эффекты иАПФ
иАПФ обладают относительно небольшим количеством побочных эффектов. К основным из них относятся: гипотензия, гиперкалиемия, повышение уровня креатинина, сухой кашель, аллергические реакции. Гипотензия нередко развивается на фоне комбинированной терапии с применением диуретиков, блокаторов медленных кальциевых каналов и т.д. или у пациентов, имеющих АД не более 110/70 мм рт.ст., и, как правило, носит дозозависимый характер. Поэтому в начале лечения рекомендуется использование малых доз короткодействующего иАПФ каптоприла. Гиперкалиемия, как правило, встречается на фоне дополнительного приема калийсберегающих диуретиков, а применение препаратов с внепочечным путем выведения снимает ограничения на использование иАПФ у больных с почечной недостаточностью. Сухой кашель отмечается у 9–26% больных. Считается, что сухой кашель развивается в ответ на чрезмерную концентрацию брадикинина в слизистой бронхов. В 90–е годы было обнаружено учащение случаев кашля у больных с ХСН и нарушенной функцией почек. При выраженном кашле целесообразно заменять прием иАПФ антагонистами рецепторов ангиотензина II.
Побочные эффекты каптоприла, связанные с приемом высоких доз (более 150 мг/сут.), как правило, объясняются наличием сульфгидрильной группы и проявляются протеинурией, кожными высыпаниями, нарушением вкусовых ощущений, нейтропенией.
Противопоказания для назначения иАПФ:
– двусторонние стенозы почечных артерий или стеноз артерии единственной почки;
– тяжелый аортальный или митральный стеноз, обструктивная кардиомиопатия;
– исходная гипотензия (АД менее 100/60 мм рт. ст.);
Лечение артериальной гипертензии ингибиторами АПФ
Опыт лечения АГ с помощью различных иАПФ показывает, что гипотензивное действие развивается у 50–75% больных с различными формами АГ (независимо от активности ренина плазмы крови). Комбинация с другими препаратами повышает эффективность иАПФ до 75–90%. В настоящее время выпускается много комбинированных препаратов: иАПФ в сочетании с салуретиком, иАПФ в комбинации с антагонистами кальция.
Гипотензивное действие иАПФ обусловлено снижением ОПСС. Однако не отмечается развития рефлекторной тахикардии, так как блокируется выброс катехоламинов. ЧСС, как правило, остается неизменной. Обычно наблюдается увеличение сердечного выброса.
Обоснованием применения иАПФ для лечения больных с сердечной недостаточностью явилось изменение представлений о патофизиологических процессах, происходящих при НК. Наибольшее признание в настоящее время получила нейрогуморальная модель развития НК, где РААС и САС отводится ведущая роль. Положительный эффект иАПФ у больных с НК обусловлен их способностью снижать пред– и постнагрузку на сердце. Снижение преднагрузки выражается в венодилатации, уменьшении венозного возврата, уменьшении конечно–диастолического объема левого желудочка, снижении давления в системе легочных сосудов. Уменьшение постнагрузки выражается в снижении АД, периферического сосудистого сопротивления. Это ведет к увеличению сердечного выброса, уменьшению объемов сердца.
Клинические эффекты иАПФ (уменьшение одышки, увеличение переносимости нагрузок) при ХСН зависят от исходной активности РААС. При высокорениновой НК эффективность иАПФ превосходит 90%, при норморениновой приближается к 70%. Это очень важно, так как при высокорениновой форме ХСН иАПФ являются единственным средством эффективного лечения, а использование сердечных гликозидов, вазодилататоров и мочегонных практически недейственно. В то же время иАПФ эффективны и при начальных стадиях заболевания и при нормальной активности плазменной (циркулирующей) РААС.
Широкомасштабные испытания, охватывавшие тысячи больных, несмотря на различия в протоколах, критериях включения пациентов, степенях декомпенсации, в дозах препаратов, с использованием разных иАПФ, показали способность всего класса лекарственных препаратов не только улучшать самочувствие, но и повышать выживаемость больных с ХСН. Кроме этого, исследования SAVE и SOLVD prevention продемонстрировали, что при применении иАПФ в ранних стадиях НК (у больных с левожелудочковой дисфункцией, сниженной ФВ, но при отсутствии клинических симптомов застойной сердечной недостаточности) замедляют прогрессирование сердечной недостаточности. Наряду с регрессией ГЛЖ лизиноприл вызывает обратное развитие миокардиального фиброза – патологического процесса, ведущего неизбежно к значительному нарушению диастолической функции сердца. В проспективном рандомизированном двойном слепом исследовании в течение 6 месяцев сравнивалось действие лизиноприла и гидрохлортиазида у пациентов с АГ, ГЛЖ и дисфункцией левого желудочка. На фоне лечения выявлено уменьшение объемной фракции коллагена на 8,7% (р
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.