Управление Роспотребнадзора по Республике Марий Эл
Управление Роспотребнадзора по Республике Марий Эл
Влияние жесткой воды на здоровье человека
Влияние жесткой воды на здоровье человека
Человек на 70-80% состоит из воды, которая является основным растворителем. С помощью нее в организме переносятся кислород, ферменты, гормоны, соли. В связи с этим особенно важным становится химический состав воды: чем больше в ней посторонних примесей, тем хуже она растворяет полезные вещества.
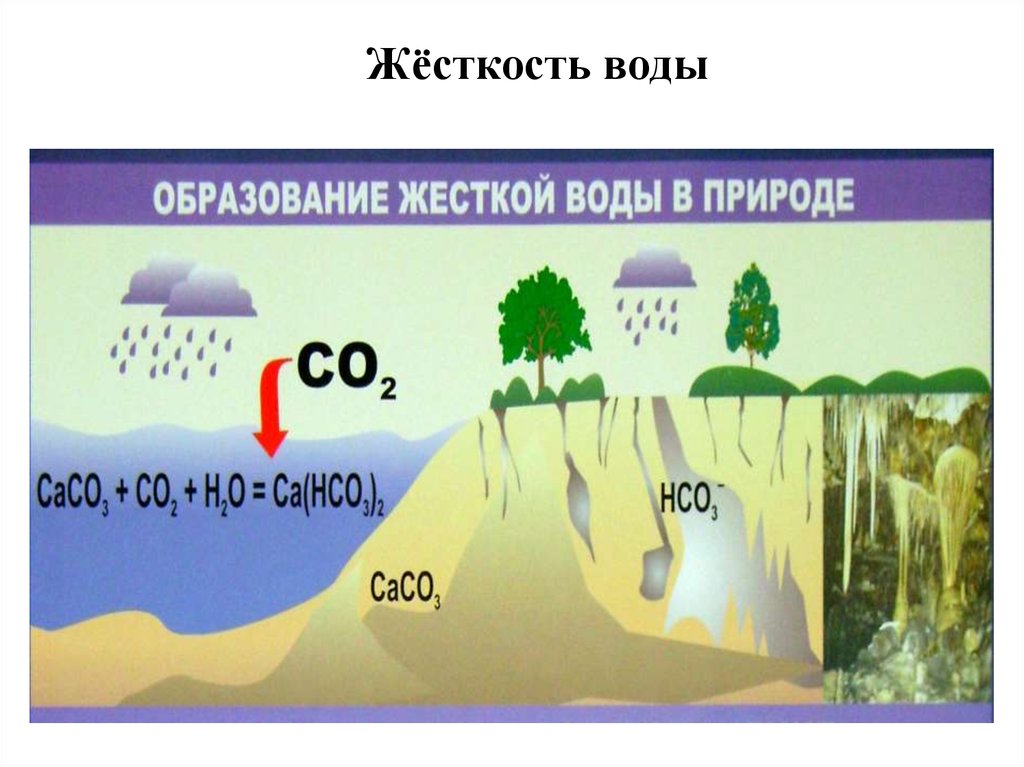
Абсолютно чистая вода в природе не встречается. Соприкасаясь с другими макро- и микроэлементами, она обогащается различными минералами, в частности, солями кальция и магния. Именно их содержанием обусловлено такое свойство, как жесткость: чем больше в воде солей кальция и магния, тем она жестче.
В нашей стране жесткость воды выражается в миллиграммах-эквивалентах на литр (мг-экв/л). Очень мягкая вода – до 1,5 мг-экв/л, мягкая – от 1,5 до 4 мг-экв/л, вода средней жесткости – от 4 до 8 мг-экв/л, жесткая – от 8 до 12 мг-экв/л и очень жесткая – более 12 мг-экв/л. Допустимый предел жесткости воды для централизованного водоснабжения – 7 мг-экв/л.
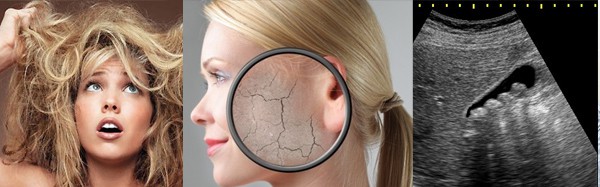
Доказано, что жесткая вода негативно влияет на организм. При взаимодействии с мылом образуются «мыльные шлаки», которые не смываются с кожи, разрушают естественную жировую пленку, защищающую от старения и неблагоприятных климатических факторов, забивают поры, образуют на волосах микроскопическую корку, тем самым вызывая сыпь, зуд, сухость, перхоть, шелушение. Кожа не только преждевременно стареет, но и становится чувствительной к раздражениям и расположенной к аллергическим реакциям.
Высокая жесткость ухудшает органолептические свойства питьевой воды, придавая ей горьковатый вкус и оказывая отрицательное действие на органы пищеварения. Соли кальция и магния, соединяясь с животными белками, которые мы получаем из еды, оседают на стенках пищевода, желудка, кишечника, осложняют их перистальтику (сокращение), вызывают дисбактериоз, нарушают работу ферментов и в конечном итоге отравляют организм. Постоянное употребление воды с повышенной жесткостью приводит к снижению моторики желудка и накоплению солей в организме.
От воды, переполненной ионами кальция и магния, чрезмерно страдает сердечно-сосудистая система. Продолжительное использование жесткой воды чревато возникновением заболеваний суставов (артритов, полиартритов), образованием камней в почках и желчных путях.
Кроме того, что жесткая вода отрицательно влияет на здоровье, еще приносит много неприятностей в быту. Она нежелательная для мытья посуды и стирки – посуда тускнеет, а ткани быстро изнашиваются. Огромный вред наносится бытовой технике: бойлерам, стиральным и посудомоечным машинам, электрочайникам и кофеваркам. Соли кальция и магния, осаждаясь на нагревательных элементах, образуют твердые известковые отложения (накипь) и довольно скоро выводят оборудование из строя.
Следы жесткой воды видны невооруженным глазом: появляется белый налет на трубах, сантехнике, в системе отопления, бытовой технике, увеличивается расход моющих средств, «сворачивается» мыло при мытье и стирке, образуются пенообразные шлаки на коже и поверхностях.
Питьевая вода на отдельных территориях Республики Марий Эл отличается природным повышенным содержанием жесткости. Нестандартные пробы по показателю общей жесткости обнаруживаются санитарными врачами в рамках социально-гигиенического мониторинга, в ходе контрольно-надзорных мероприятий и рассмотрения обращений граждан.
Проводить очистку воды перед подачей населению должны соответствующие ресурсоснабжающие организации.
С жалобами на ненадлежащее качество питьевой воды можно обращаться в Управление Роспотребнадзора по Республике Марий Эл.
Чем опасна жесткая вода?
Обратноосмотические мембраны создавались для того, чтобы обессоливать воду. Это свойство снимает массу проблем с тех, у кого питьевая вода очень жесткая. Обратноосмотические системы уберут не только накипь, но и максимум вредных примесей, которыми награждает воду цивилизованный мир. Эта способность мембран значительно превышает возможности классических сорбционных фильтров.
Цена литра очищенной с использованием мембраны воды будет незначительно выше, чем у сорбционного водоочистителя. При этом сравнивать степень очистки нужно уже с бутилированной водой из магазина, поскольку покупная очищена по той же обратноосмотической технологии. Сегодня бытовые осмотические системы доступны как никогда. А системы АКВАФОР серии DWM не имеют аналогов по скорости, экономичности и компактности.
Обратноосмотические мембраны создавались для того, чтобы обессоливать воду. Это свойство снимает массу проблем с тех, у кого питьевая вода очень жесткая. Обратноосмотические системы уберут не только накипь, но и максимум вредных примесей, которыми награждает воду цивилизованный мир. Эта способность мембран значительно превышает возможности классических сорбционных фильтров.
Цена литра очищенной с использованием мембраны воды будет незначительно выше, чем у сорбционного водоочистителя. При этом сравнивать степень очистки нужно уже с бутилированной водой из магазина, поскольку покупная очищена по той же обратноосмотической технологии. Сегодня бытовые осмотические системы доступны как никогда. А системы АКВАФОР серии DWM не имеют аналогов по скорости, экономичности и компактности.
Вред жесткой воды для здоровья









По вкусу жесткую воду отличить очень легко – он крайне горькая. Иногда встречающийся горький вкус родниковой воды обусловлен именно наличием солей жесткости.
По внешнему виду можно узнать после кипячения. В этом случае соли выпадают в осадок, которой легко виден на дне любого сосуда.
В России жесткость воды измеряют в градусах жесткости, но она так же может быть выражена в объемной доле или массовым числом.
Официально принятая единица измерения, которая используется в системе СИ ( международная система единиц ) – моль на кубический метр. Но на практике не используют перечисленные единицы измерения, предпочитая миллиэквивалент на литр (мг-экв./л).
По уровню жесткости воду делят на четыре типа:
Эта классификация называется американской и при оценке жесткости воды используется чаще всего.
Те же показатели в Европе не могут быть больше 1,2 миллиэквивалентов на литр. Это значит, что европейцы пьют мягкую воду, жесткость которой почти в шесть раз меньше установленной в России.
Общая жесткость воды вычисляется путем суммирования показателей карбонатной и некарбонатной жесткости.
Самые высокие показатели жесткости из-за обилия растворенных солей определяют в морской и океанической воде. Жесткость поверхностных вод обычно в несколько раз меньше грунтовых вод и влаги из подземных источников.
Рассмотрим негативное воздействие чрезмерно жесткой воды на организм человека, бытовую технику и коммуникации. Чем выше параметр жесткости, тем сильнее будет значение каждого вида вредного воздействия.
Но при этом, не нужно забывать, что показатель жесткости должен равняться определенному среднему значению. Слишком мягкая вода также не несет никакой пользы. Она повышает риск развития сердечно сосудистых заболеваний у человека, вымывает соли из организма, вызывая быстрое развитие рахита и истончение костей. В коммуникационных системах мягкая вода вызывает коррозию металлических труб.
Почему нельзя пить жесткую воду
Жёсткость воды – совокупность ее химических и физических свойств, связанных с содержанием в ней растворённых солей щёлочноземельных металлов, главным образом, кальция и магния.
По величине общей жёсткости различают:
С 1 января 2014 года в России введен межгосударственный стандарт ГОСТ 31865-2012 «Вода. Единица жесткости». По новому ГОСТу жесткость выражается в градусах жесткости (°Ж). 1 °Ж соответствует концентрации щелочноземельного элемента, численно равной 1/2 его миллимоля на литр (1 °Ж = 1 мг-экв/л).
По величине общей жёсткости различают воду:
У одного и того же водоисточника жесткость воды может меняться в течение года. Например, весной, в период паводка, жесткость воды, особенно в поверхностных источниках, уменьшается. А жарким летом в связи с повышенным испарением воды с поверхности водоема, а так же из-за редких дождей жесткость воды, наоборот, увеличивается.
В подземных источниках жесткость воды практически не меняется в течение года, и, как правило, очень высокая (до 80-100 мг-экв/л).
Жёсткая вода при умывании сушит кожу, в ней плохо образуется пена при пользовании мылом. Использование жёсткой воды вызывает появление осадка (накипи) на стенках котлов, в трубах и т.п. В то же время, использование слишком мягкой воды может приводить к коррозии труб. В этом случае отсутствует кислотно-щелочная буферность, которую обеспечивает гидрокарбонатная жёсткость.
В различных информационных источниках можно встретить информацию, что жесткая вода способствует образованию камней в мочеполовой системе, а мягкая увеличивает риск сердечно-сосудистых заболеваний. Многие люди отмечают, что умываясь водой с повышенном содержанием солей, кожа лица становится суше. Однако, достоверных клинических исследований о вреде такой воды на организм человека не существует. Поэтому, вероятнее всего, потребление и использование в быту жёсткой или мягкой воды не является опасным для здоровья.
А вот бытовой технике или водопроводной системе жесткая или мягкая вода может нанести существенный вред.
Нередки случаи, кода чайник или стиральная машина выходят из строя в связи с использованием жесткой воды. Жёсткая вода вызывает появление осадка (накипи) на нагревательных элементах бытовых приборов, стенках котлов, в трубах. Особенно часто это наблюдается при использовании для бытовых и хозяйственных нужд подземных водоисточников.
В то же время, использование слишком мягкой воды может привести к коррозии труб, так как, в этом случае отсутствует кислотно-щелочная буферность, которую обеспечивает гидрокарбонатная жёсткость.
Вкусовые качества воды тоже значительно отличаются друг от друга именно из-за отсутствия или наличия в ней тех или иных солей.
Вот почему родниковая или минеральная вода нам часто очень нравится – она более насыщена солями.
Способы устранения жесткости воды:
Термоумягчение.
Самый доступный и наиболее часто используемый в быту способ. Основан на кипячении воды. В результате термически нестойкие гидрокарбонаты кальция и магния разлагаются с образованием накипи.
Реагентное умягчение.
Метод основан на добавлении в воду различных реагентов, например, кальцинированной соды, гашёной извести или ортофосфата натрия. Последний, часто входит в состав бытовых средств, которые мы используем для предотвращения образования накипи в стиральных, посудомоечных машинах или других бытовых приборах.
Метод основан на использовании ионообменной гранулированной загрузки (чаще всего ионообменные смолы). Такая загрузка при контакте с водой поглощает катионы солей жёсткости (кальций и магний, железо и марганец). Взамен, в зависимости от ионной формы, отдаёт ионы натрия или водорода.
Этот метод используется в промышленности.
Метод основан на прохождении воды через полупроницаемые мембраны (как правило, полиамидные). Вместе с солями жёсткости удаляется и большинство других солей. Эффективность очистки может достигать 99,9 %. Этот метод является дорогостоящим.
Обратноосмотические фильтры часто применяются нами в быту.
Такая вода становится практически дистиллированной.
Электродиализ
Основан на удалении из воды солей под действием электрического поля.
Дистилляция – полностью очищает воду от солей.
Часто, для смягчения воды в быту применяются механические фильтры.
Жесткость воды: воздействие на здоровье и сантехнику
Введение
Жесткость воды — одно из важнейших свойств, имеющее большое значение при водопользовании. Если в воде находятся ионы металлов, образующие с мылом нерастворимые соли жирных кислот, то в такой воде затрудняется образование пены при стирке белья или мытье рук, в результате чего возникает ощущение жесткости. Жесткость воды пагубно сказывается на трубопроводах тепловых сетей, приводя к образованию накипи. По этой причине в воду приходится добавлять специальные «смягчающие» химикаты.
Жесткость воды обусловлена присутствием растворимых и малорастворимых солей-минералов, главным образом кальция (Са2+) и магния (Mg2+). Кроме указанных, к солям жесткости относят также соли стронция (Sr 2+ ), цинка (Zn 2+ ) и др., однако в поверхностных и грунтовых природных водах из перечисленных катионов в заметных концентрациях присутствуют только кальций и магний.
Суммарная жесткость воды, то есть общее содержание растворимых солей кальция и магния, получила название «общей жесткости». Ввиду того, что солями жесткости являются соли разных катионов, имеющие разную молекулярную массу, концентрация солей жесткости, или жесткость воды, измеряется в единицах эквивалентной концентрации — количеством г-экв/л или мг-экв/л.
При жесткости до 4 миллиграмм эквивалент/литр вода считается мягкой; от 4 до 8 миллиграмм эквивалент/литр — средней жесткости; от 8 до 12 миллиграмм эквивалент/литр — жесткой; более 12 миллиграмм эквивалент/литр — очень жесткой.
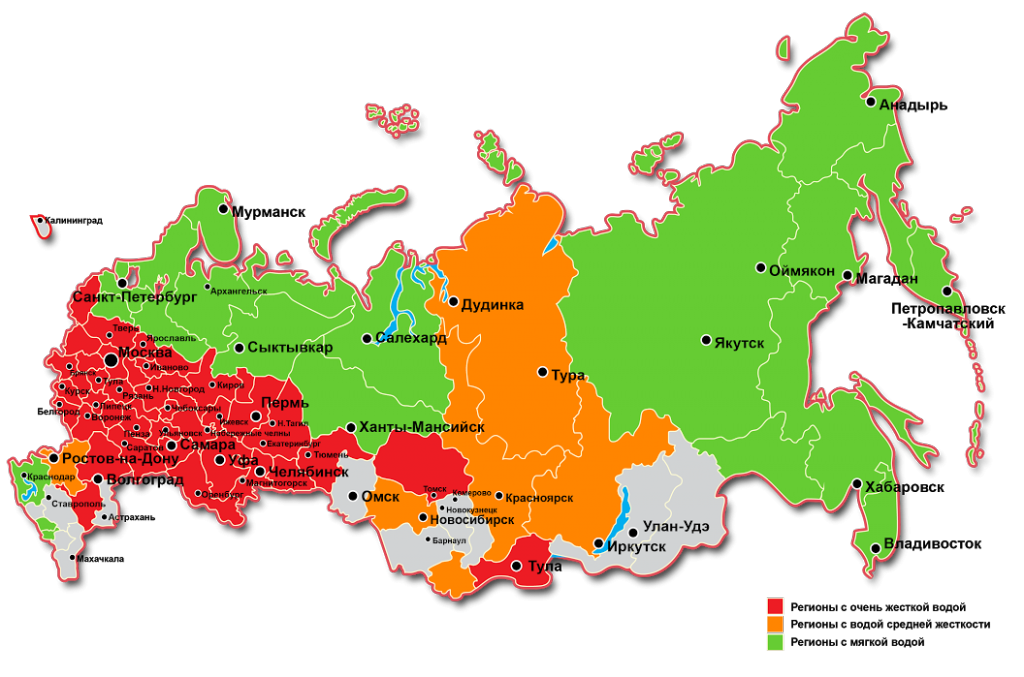
В различных регионах России жесткость поверхностных и грунтовых вод отличается: преимущественно мягкие воды географически приурочены к районам севера Европейской части России, а также Восточной Сибири. В центре и на юге Европейской части России, а также в южных регионах Западной Сибири вода преимущественно жесткая. В естественных условиях ионы кальция, магния и других щелочноземельных металлов, обусловливающих жесткость, поступают в воду в результате взаимодействия растворенного диоксида углерода с карбонатными минералами и других процессов растворения и химического выветривания горных пород. Источником этих ионов являются также микробиологические процессы, протекающие в почвах на площади водосбора, в донных отложениях, а также сточные воды различных предприятий. Различные типы пород, залегающих на территории водосборов, а также взаимосвязанные с ними свойства почвенного покрова непосредственно обуславливают различия в жесткости вод в регионах нашей страны.
Воздействие жесткости на организм
Поиск причинно-следственных связей между жесткостью воды и сердечно-сосудистой патологией был результативным. В ряде исследований установлена статистически достоверная, хотя и не тесная, обратная корреляционная связь между жесткостью воды и частотой инфаркта миокарда. Поскольку в других, не менее тщательно выполненных исследованиях, такой связи не было установлено, считается, что патогенетическим агентом могли быть не сами соли жесткости, а коррелирующие с ними какие-либо другие микроэлементы. Что касается других проявлений вредного влияния жестких вод, то статистическими исследованиями установлено и экспериментально подтверждено их влияние на частоту возникновения мочекаменной болезни. В этом случае не идет речи о прямой детерминированности степени жесткости воды и заболеваний мочекаменной болезнью. Решающую роль играют другие сопутствующие факторы, в частности состояние минерального обмена конкретного человека, потребляющего жесткую воду. Высокое содержание в питьевой воде солей кальция и магния является фактором риска мочекаменной болезни.
Воздействие жесткости на сантехнику
Воздействие повышенной жесткости воды на контактирующие с ней приборы и сантехнику приводят к следующим последствиям:
Жёсткость воды из-за образующихся отложений негативно влияет на котельное оборудование. В России введены строгие требования к качеству воды по жёсткости для котлов ТЭЦ, электростанций, промышленных водонагревателей. Поэтому умягчение воды (водоподготовка) является в этом случае обязательным условием.
Способы умягчения воды
Умягчение воды может быть осуществлено следующими основными способами:
Нередко представляется целесообразным комбинировать эти способы, удаляя часть солей жесткости реагентным способом, а остаток их — катионированием, либо применять реагентный способ в комбинации с термическим способом умягчения воды.
Из реагентных способов умягчения наиболее распространен известково-содовый способ. Сущность его состоит в переводе растворенных в воде солей Са 2+ и Mg 2+ в малорастворимые СаСОз и Mg(OH)2, выпадающие в осадок.
Катионитовый способ умягчения воды заключается в фильтровании жесткой воды через мелкозернистую загрузку некоторых веществ (сульфоуголь, искусственные смолы). Эти вещества обладают способностью обменивать катионы содержащегося в них натрия Na + или водорода Н + на катионы кальция Са 2+ или магния Mg 2+ солей жесткости, растворенных в воде. Таким образом, различают процесс Na-катионирования и Н-катионирования.
Когда обменная способность катионитового фильтра исчерпана, производят регенерацию катионитовой загрузки. Na-катионитовые фильтры регенерируются раствором поваренной соли NaCl, а Н-катионитовые — растворами серной H2SO4 или соляной HCl кислот.
Вода после Na-катионитовых фильтров обычно имеет повышенную щелочность (рН>7), а после Н-катионитовых — повышенную кислотность (рН