Влияние мелатонина на иммунную систему
Механизмы участия мелатонина в иммунорегуляции.
Взаимодействие между нейроэндокринной системой и иммунной заслуживает большое внимание вследствие выявления все большего количества аутоиммунных патологий. Серии экспериментов показали тесную связь между регуляцией иммунитета и гормонами, такими как мелатонин, кортизол, половые гормоны. В частности, при удалении эпифиза или химическом подавлении синтеза и секреции мелатонина в шишковидной железе наблюдалась выраженная иммуносупрессия. Иммуносупрессивный статус при этом был обратим при назначении мелатонина. (Carrillo-Vico et al. 2006) Выявлено, что рецепторы этого гормона экспрессируются в том числе и на поверхности CD4 T и CD8 T клеток, а также В-лимфоцитов.( Lissoni et al. 2008). При этом опытным путем in vivo установлено, что в условиях увеличения концентрации мелатонина увеличивается пролиферация Т-лимфоцитов, продукция NK-клеток (natural killer) и моноцитов в костном мозге мышей. У людей возможно увеличение концентрации цитокинов в периферическом кровотоке при увеличении количества рецепторов мелатонина. В противоположность этому, при лечении мелатонином отмечалось снижение экспрессии интерлейкина-2, интерферона-гамма, однако отмечалась активация Т-хелперов 2 типа, выделение ими цитокинов, таких как интерлейкин-4 и интерлейкин-10. Также этот гормон даже в небольших концентрациях способен снижать эффект от приема глюкокортикоидов. Множество исследований, большинство из которых все-таки выполнялось на мышах, продемонстрировали его протективный эффект в отношении вирусного энцефалита, септического шока, бактериальных инфекций, (Raghavendra et al.2010). Обсуждается применение мелатонина для стимуляции ответа у лиц со снижением иммунитета при бактериальных и вирусных инфекциях.
Применение мелатонина при аутоиммунных заболеваниях.
Таким образом, на сегодня действие мелатонина на иммунную систему окончательно не установлено, в последних работах по этой проблеме (Gu-Jiun Lin et al. 2013) отмечено, мелатонин вероятнее всего имеет дихотомический эффект на иммунную систему, одновременно активируя и подавляя определенные ее звенья. Требуются дальнейшие исследования для введения в терапию мелатонина в качестве активатора иммунитета во избежание серьезных побочных эффектов от такой терапии.
Forrest C. et al. Inflammatory status and kynurenine metabolism in rheumatoid arthritis treated with melatonin. Br J Clin Pharmacol. 2007
Gu-Jiun Lin et al. Modulation by Melatonin of the Pathogenesis of Inflammatory Autoimmune Diseases. Int J Mol Sci. 2013 June
Почему нельзя принимать мелатонин при аутоиммунных заболеваниях
Рассеянный склероз (РС) — аутоиммунное заболевание, связанное с демиелинизацией нервных волокон. Одним из факторов, который может служить индуктором или провоцирующим агентом для данной патологии, является мелатонин — гормон, синтезируемый преимущественно эпифизом, а также эктопически — сетчаткой глаза, слезными железами, некоторыми клетками желудочно-кишечного тракта, тромбоцитами и другими клетками и тканями [1, 2]. На участие мелатонина в развитии РС указывает ряд данных. Показано, в частности, что у мышей с экспериментальным аутоиммунным энцефаломиелитом (ЕАЕ, модель РС у животных) уровень мелатонина повышен, а введение антагонистов мелатониновых рецепторов или пинеалэктомия предупреждают развитие ЕАЕ или смягчают его проявления [3, 4]. Объяснить эти эффекты непосредственным действием мелатонина на клетки ЦНС нельзя, поскольку в опытах in vitro и in vivo, моделирующих различные варианты поражения мозга, гормон, как правило, выступает в качестве нейропротектора. Он повышает выживаемость незрелых нейронов и их предшественников [5, 6], подавляя демиелинизацию [5], промотирует процессы миелинизации и поддерживает проводимость аксонов за счет снижения нейровоспаления и стимуляции созревания олигодендроцитов [7, 8]. Предполагают, что участие мелатонина в развитии РС связано с его иммуномодулирующими эффектами, в частности гормонзависимой регуляцией аутоиммунных процессов. Наиболее очевидной мишенью действия мелатонина в иммунной системе при данной патологии является субпопуляция Т-лимфоцитов, продуцирующих IL-17 (Th17). С одной стороны, теоретически, эта субпопуляция должна находиться под непосредственным контролем мелатонина [9, 10]. С другой стороны, именно Th17-клеткам в настоящее время отводится ключевая роль в патогенезе РС — активация Th17 провоцирует нейровоспаление, а сдвиг баланса между Th17 и регуляторными Т-клетками (Treg) приводит к срыву иммунной толерантности и, как следствие, развитию аутоиммунных процессов [11, 12].
Таким образом, мелатонинзависимая регуляция дифференцировки Th17 является, возможно, новым, ранее не известным механизмом индукции и/или прогрессирования РС.
Мелатонин в контроле иммунной системы
Практически все типы клеток иммунной системы экспрессируют рецепторы для мелатонина [13—15] и, как следствие, чувствительны к действию гормона [16—18]. Поэтому любые колебания его уровня должны сопровождаться изменением реактивности иммунной системы, в том числе в отношении аутоантигенов.
Рецепторы для мелатонина и неспецифические мишени действия гормона в иммунной системе
У млекопитающих идентифицировано два типа мембранных рецепторов для мелатонина, МТ1 и МТ2 [19]. Это типичные G-белок-связывающие рецепторы, имеющие 55% идентичности [19]. МТ1 и МТ2 реализуют свои эффекты через ингибиторные G-белки (Gi-белки), активация которых приводит к снижению уровня цАМФ в цитоплазме и ингибированию цАМФ-зависимой протеинкиназы, РКА [19], но в некоторых типах клеток могут связываться также и со стимуляторными G-белками Gs, Gz и G16, участвуя в регуляции фосфолипаз С и А2, гуанилатциклазы, а также калиевых и кальциевых каналов. МТ1 и МТ2 различаются по аффинности к естественному лиганду. Для человеческих рецепторов константы ингибирования составляют 80,7 и 383 pM соответственно [20]. Рецепторы MT1 и MT2 широко представлены в иммунной системе и экспрессируются клетками как адаптивного, так и врожденного иммунитета [13, 14, 18, 21].
Наряду с мембранными идентифицированы и высокоаффинные ядерные рецепторы для мелатонина. Это транскрипционные факторы, принадлежащие подсемейству рецепторов ретиноидов Z, или сиротских рецепторов ретиноидов (retinoic acid receptor-related orphan receptor, ROR/RZR) — RORα и RORβ [21, 22]. По сравнению с МТ1/МТ2 аффинность ядерных рецепторов для мелатонина в 100—1000 раз ниже. RORβ представлен в ЦНС, в том числе эпифизе, тогда как RORα участвует в основном в контроле иммунной системы — его экспрессия выявлена как в лимфоидных, так и миелоидных клетках [13, 21]. RORα-связывающие сайты имеются в регуляторных районах многих генов, однако прямая транскрипционная регуляция показана лишь для некоторых, и один из них — IL-17 [23].
Важно отметить, что все специфические мелатониновые рецепторы имеют разную аффинность и могут запускать различные сигнальные механизмы с соответствующим выходом. Более того, недавно описаны дополнительные внутриклеточные мишени действия мелатонина в микромолярном диапазоне — кальмодулин и гидрохинон [15]. Поскольку эти факторы имеют широкое распространение, большинство клеток является потенциальными мишенями действия мелатонина. Однако их низкая аффинность предполагает наличие продуктивных взаимодействий с мелатонином только в концентрациях, значительно превышающих те, которые обеспечиваются эпифизом.
Мелатонинзависимая регуляция иммунной системы
Данные, касающиеся иммуномодулирующей активности гормона, довольно противоречивы. В норме или условиях иммунодефицита эффекты мелатонина, как правило, стимулирующие: гормон усиливает пролиферативный ответ лимфоцитов [17], стимулирует развитие T-хелперов 1-го класса (Th1-клетки), продуцирующих провоспалительные цитокины [16], и ингибирует апоптоз лейкоцитов [18]. Более того, лимфоциты человека при культивации in vitro сами активно синтезируют и секретируют мелатонин [21], который в свою очередь модулирует IL-2/IL-2R-систему за счет рецепторопосредованных интра-, ауто- и/или паракринных механизмов [21, 24]. Тем не менее имеются данные, свидетельствующие об иммуносупрессивной активности мелатонина. Показано, в частности, что гормон снижает продукцию провоспалительных цитокинов, сдвигая иммунный ответ в направлении развития Т-хелперов 2-го класса (Th2), продуцентов противовоспалительных цитокинов, — эти эффекты фиксируются в условиях острого или хронического снижения активности иммунной системы, например при септическом шоке [24]. Противоречия в данных по направленности иммуномодулирующих эффектов мелатонина объясняются, видимо, не только различиями в исходной иммунореактивности, но и его способностью индуцировать синтез других гормонов и факторов системы гипоталамус/гипофиз/надпочечники, многие из которых сами являются эффективными иммуномодуляторами. Вследствие этого на прямое стимулирующее действие мелатонина in vivo накладываются эффекты других медиаторов, в первую очередь глюкокортикоидов, работающих, как правило, в противофазе с мелатонином и обладающих выраженной иммуносупрессивной активностью. Следует напомнить, что иммунокомпетентные клетки имеют несколько типов мелатониновых рецепторов, а также неспецифических мишеней с разными аффинностью, внутриклеточной сигнализацией и последствиями стимуляции.
Th17-клетки и баланс Th17/Treg — новая мишень действия мелатонина
Субпопуляция Th17 идентифицирована недавно как отдельная Т-хелперная субпопуляция с уникальным набором продуцируемых цитокинов, включая IL-17А, IL-17 °F, IL-22 и ряд других, причем все они вовлечены в развитие тканевого воспаления [25, 26]. Дифференцировка Th17 опосредуется линиеспецифичными транскрипционными факторами. Первым из них был идентифицирован RORγ’, однако его дефицит не отменяет полностью продукцию Th17-цитокинов [27]. Позже была выявлена экспрессия другого ядерного фактора того же семейства — RORα [9]. Подобно RORγ’ экспрессия нового фактора индуцировалась цитокинами TGFβ и IL-6 и опосредовалась STAT3-зависимыми механизмами [9]. Показано, что избыточная экспрессия RORα промотирует дифференцировку Th17 и значительно усиливает продукцию IL-17 и IL-17 °F, тогда как его дефицит сопровождается снижением экспрессии IL-17 in vitro и in vivo [9, 23]. Более того, в случае коэкспрессии RORα и RORγ’ синергично усиливают дифференцировку Th17, а дефицит обоих факторов ведет к почти полному подавлению генерации данного типа клеток. И наконец, прямая активация RORα в культуре Т-лимфоцитов индуцирует продукцию IL-17 [9, 23]. Таким образом, RORα наряду с RORγ’ играет ключевую роль в дифференцировке Th17-клеток.
Одновременно с этим RORα, как упоминалось ранее, является высокоаффинным рецептором для мелатонина [21, 22], что указывает на непосредственное его участие в индукции развития Th17. Удивительно, что при этом Th17-клетки — пожалуй, единственная на сегодняшний день лимфоцитарная субпопуляция, не изученная в плане мелатонинзависимой регуляции.
Клетки Th17 являются ключевыми элементами в иммунной системе. Они участвуют в противоинфекционной защите организма, развитии воспаления, аутоиммунных заболеваний, канцерогенезе, а также трансплантационном иммунитете. Поэтому любые колебания активности данной Т-клеточной субпопуляции должны иметь множественные проявления. И именно она находится, по-видимому, под прямым контролем мелатонина — гормона, уровень которого имеет заметные суточные и сезонные вариации, а также существенно изменяется при некоторых физиологических или патологических условиях.
Возможные последствия мелатонинзависимого контроля генерации Th17
Во-первых, это участие мелатонинзависимой дифференцировки клеток Th17 в циркадных, а также сезонных колебаниях активности иммунной системы. Недавними исследованиями было показано, что ряд параметров иммунной системы существенно варьирует в зависимости от времени суток [28], и мелатонин играет, по-видимому, существенную роль в этом процессе [29] наряду с другими эндокринными механизмами или непосредственным контролем экспрессии ряда иммуноактивных молекул компонентами циркадной системы [28]. Исследование суточной ритмичности субпопуляционного состава лимфоцитов человека, а также цитокиновой продукции выявило сильную позитивную корреляцию некоторых характеристик структуры лимфоцитарных субпопуляций, а также пика соотношения IFNγ/IL-10 с уровнем мелатонина в плазме [29], указывая на наличие причинно-следственной связи мелатонина с активацией Th17. Наряду с этим иммунорегуляторное действие мелатонина имеет сезонную зависимость [30]. Как следствие, суточные и/или сезонные колебания показателей состояния иммунной системы определяют эффективность противоинфекционной защиты [30], а также предрасположенность к развитию и прогрессированию иммунозависимых патологий, таких как опухолевые [31] или аутоиммунные [30] заболевания, и мелатонинзависимый контроль активности Th17 может вносить вклад в этот процесс.
Во-вторых, функционирование Th17 может подвергаться изменениям в условиях, связанных с более выраженным и устойчивым изменением уровня мелатонина, в частности при его последовательном снижении с возрастом [32] или резком и длительном — в результате ишемического инсульта [32]), и, напротив, в случае возрастания его уровня при некоторых аутоиммунных заболеваниях, таких как ревматоидный артрит [33] или РС [34].
Наконец, мелатонин рассматривается как перспективный фармацевтический препарат — благодаря своей антиоксидантной [35, 36], иммуномодулирующей [15, 36] и цитопротективной [24] активности. Показана эффективность гормона в антивирусной, антибактериальной и антипаразитарной защите [37, 38], предупреждении опухолей [39, 40], терапии ряда нейродегенеративных заболеваний, таких как болезни Альцгеймера и Паркинсона [41, 42].
Мелатонинзависимая регуляция Th17 и баланса Th17/Treg как возможный механизм развития РС
Роль мелатонина в развитии РС заслуживает отдельного внимания. Ряд данных указывает на его возможное участие в развитии этой патологии. С одной стороны, уровень мелатонина повышен у пациентов с РС [34], а также у мышей с EAE, причем введение антагонистов мелатониновых рецепторов или пинеалэктомия предупреждают развитие патологии в такой модели либо снижают выраженность ее проявления [3, 4]. С другой стороны, Th17-клетки, потенциальные мишени действия мелатонина, играют важную роль в развитии аутоиммунных заболеваний, в частности РС [11]. Экспрессия IL-17 повышена как у мышей с ЕАЕ, так и пациентов с РС [12, 43] и коррелирует с тяжестью заболевания [43], тогда как дефицит IL-17 в экспериментальной животной модели ассоциирован с устойчивостью к развитию ЕАЕ [11, 43]. Таким образом, мелатонинзависимая регуляция дифференцировки Th17 может быть еще одним, ранее не известным механизмом индукции и/или прогрессирования РС.
Важно отметить, что в настоящее время активно обсуждается возможность использования мелатонина в лечении Р.С. По крайней мере, показана его эффективность в купировании таких осложнений заболевания, как депрессия [44] или офтальмопатия [45], главным образом за счет антиоксидантных эффектов гормона. Кроме того, мелатонин, как отмечалось выше, является эффективным нейропротектором, способным в том числе тормозить процесс демиелинизации нервных волокон и даже стимулировать их миелинизацию [7, 8] Более того, в литературе имеются отдельные сообщения [46] о позитивном действии мелатонина на течение заболевания. Однако иммунорегуляторная активность мелатонина, прежде всего — индукция дифференцировки Th17, являясь одним из патогенетических механизмов развития РС, может перекрыть все позитивные эффекты гормона, в том числе нейропротективные.
Мелатонин: При депрессии, аутоиммунных заболеваниях и раке
Рецидивы рассеянного склероза, которые случаются весной и летом, как правило, менее распространены при более высоком уровне витамина D и могут быть связаны со снижением уровня мелатонина.
Гормон мелатонин играет важную роль для вашего здоровья, помогает лучше спать, укрепляет иммунную систему, замедляет старение головного мозга, уменьшает частоту и силу приступов мигрени, поддерживает массу костей и предотвращает развитие рака. Отсутствие солнечного света в течение дня в сочетании с искусственным освещением по вечерам сбивают ваши биологические часы и, следовательно, нарушают производство мелатонина, и это может спровоцировать ряд неблагоприятных последствий для здоровья.
Польза мелатонина для здоровья
Фактически, мелатонин был предметом доклинических исследований о его влиянии на более чем 100 различных заболеваний, многие из которых идут рука об руку с потребностью во сне.
Мелатонин для сна и прочего
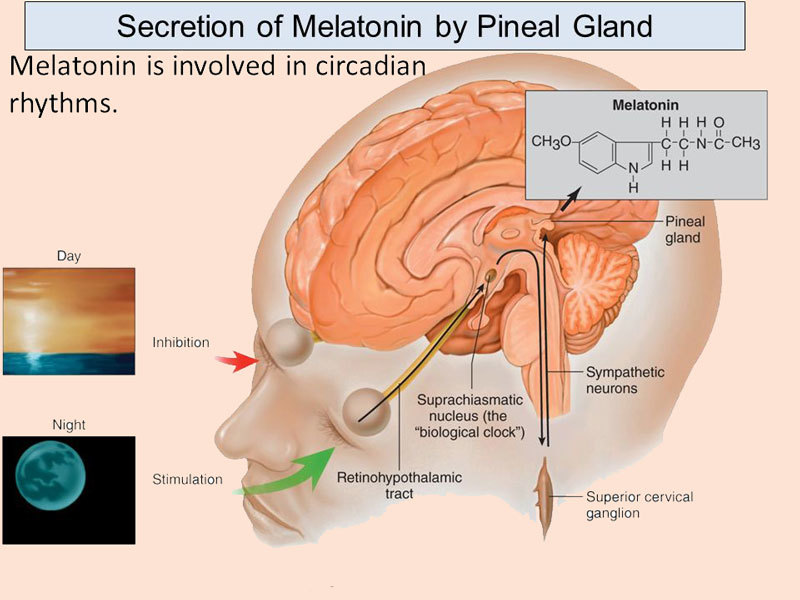
Ваши основные биологические часы находятся в супрахиазматическом ядре мозга (СХЯ), которое является частью гипоталамуса. Основываясь на сигналах света и темноты, СХЯ сообщает шишковидному телу, когда нужно секретировать мелатонин и когда перестать.
В научных исследованиях было показано, что добавка мелатонина помогает людям быстрее засыпать и лучше спать, испытывать меньше беспокойства и предотвращает усталость в течение дня.
Имейте в виду, что вам может потребоваться минимальная доза. Я рекомендую начать с 0,25 или 0,5 мг и дальше корректировать количество. Более высокие дозы, такие как 3 мг, могут заставить вас быть более бодрым, а не сонливым, поэтому начинайте с минимума и изменяйте дозу по необходимости.
Было также обнаружено, что мелатонин снижает эффекты джет лэга при смене часовых поясов. Согласно последним исследованиям, дети, страдающие экземой, болезнью, которая часто мешает хорошему сну, лучше спят после приема добавки мелатонина.
Нормализация циркадной системы помогает облегчить симптомы депрессии
Ваш уровень мелатонина обратно пропорционально растет и падает со светом и темнотой, и физическое и психическое здоровье неразрывно связано с этим ритмом. В темноте он увеличивается, поэтому вы можете чувствовать усталость, когда солнце начинает садиться.
И наоборот, когда вы перед сном подвергаетесь воздействию яркого искусственного освещения, включая синий свет, излучаемый телевизорами и электронными гаджетами, у вас могут возникнуть проблемы с засыпанием из-за подавления производства мелатонина.
Освещение в помещении в тот момент когда вы просыпаетесь ночью, также может быть проблематично, как я объясняю в видео выше. Однако вам не обязательно спотыкаться в темноте, так как красные и оранжевые волны не будут понижать уровень.
Вы можете использовать красный свет, чтобы попасть в ванную комнату. Если в вашей спальне есть часы, убедитесь, что у них красный светодиодный дисплей. Синий свет хуже всего, так как он наиболее эффективно останавливает производство мелатонина.
САР от зимней печали
Сезонное аффективное расстройство (САР, также называемое «зимней печалью») связано с отсутствием солнечного света, и ученые обычно рекомендуют для его лечения световую терапию полного спектра вместо СИОЗС, таких как прозак или золофт.
Интересно, что недавние исследования показывают, что светотерапия может быть предпочтительна даже при большом депрессивном расстройстве, и по эффективности превосходит прозак для пациентов с умеренной и тяжелой депрессией. Одна из причин, по которой она работает, вполне вероятно, связана с тем, что яркий свет помогает сбросить ваши биологические часы или циркадный ритм.
Добавка мелатонина может помочь в определенной степени, но не так эффективно, как воздействие яркого света в дневное время, который может работать аналогично антидепрессантам, регулируя функции нейротрансмиттера.
Световая терапия более эффективна, чем прозак
Исследование, о котором мы говорим, сравнивает эффективность светотерапии по отдельности и в сочетании с антидепрессантом флуоксетином (прозак).
Восьминедельное тестирование включало 122 взрослых в возрасте от 19 до 60 лет, которым был поставлен диагноз умеренной и тяжелой депрессии.
Участники были разделены на четыре группы и они получали:
Световую терапию (30 минут в день по пробуждении с использованием классической модели лампы дневного света марки Carex мощностью 10 000 люкс) и таблетку плацебо
Прозак (20 мг / день) плюс дезактивированный генератор отрицательных ионов, служащий в качестве светового устройства-плацебо
Светотерапию и прозак
Световое устройство-плацебо плюс таблетку-плацебо (контрольная группа)
Вот именно, лекарства были наименее эффективны и НЕ ТАК эффективны, как плацебо! В конце исследования ремиссия происходила:
Только у 19 процентов в группе исключительно прозака
У 30 процентов в группе плацебо
Почти у 44 процентов в группе исключительно световой терапии
Почти у 59 процентов в группе активной комбинации
Роль мелатонина в борьбе с раком
Увеличивает производство иммуномодулирующих веществ, таких как интерлейкин-2, который помогает идентифицировать и атаковать мутировавшие клетки, которые приводят к злокачественным раковым опухолям
Ингибирует развитие новых кровеносных сосудов в опухолях (ангиогенез опухоли), что замедляет распространение рака
Задерживает развитие рака, активируя цитокиновую систему, которая помогает ингибировать рост опухоли и стимулирует цитотоксическую активность макрофагов и моноцитов
Благодаря его антиоксидантному действию он также ограничивает окислительное повреждение ДНК
Ингибирует рост опухоли, противодействуя эстрогену. (Ночью, на пике производства мелатонина, деление клеток замедляется. И когда мелатонин закрепляется на клетке рака молочной железы, он противодействует тенденции эстрогена стимулировать рост клеток)
Некоторые исследования влияния мелатонина на рак молочной железы включают следующее:
Журнал «Эпидемиология» сообщил о повышенном риске рака молочной железы среди женщин, которые работают преимущественно в ночные смены
Согласно данным израильского исследования, женщины, живущие в районах с большим количеством ночного освещения, чаще имеют рак молочной железы, чем те, кто живет в там, где преобладает темнота по ночам
Из исследования здоровья медсестер выяснилось, что те, кто работает по ночам, имеют на 36% более высокие показатели рака молочной железы
У слепых женщин, чьи глаза не могут обнаружить свет и, следовательно, они имеют устойчивое производство мелатонина, показатели рака молочной железы ниже среднего
Когда большинство эпидемиологических исследований оценивается в совокупности, у женщин, которые работают в ночную смену, уровень рака молочной железы на 60 процентов выше нормы, даже если учитываются другие факторы, такие как различия в рационе.
Мелатонин может улучшить результаты лечения пациентов с раком легких
Другим видам рака мелатонин также может принести пользу. В 2004 году Фонд продления жизни сотрудничал с Центрами лечения рака в Америке в первом клиническом исследовании, посвященном влиянию мелатонина на пациентов с раком легких.
Результаты, которые были опубликованы совместно с Американским обществом клинической онкологии в 2014 году, обнаружили реакцию образования опухолей у более 29 процентов тех, на кого воздействовал мелатонин ночью, по сравнению с менее чем 8 процентами пациентов, подвергавшихся его воздействию утром, и 10,5 процентами принимавших плацебо.
Как сообщает Life Extension Magazine:
«Европейские клинические исследования показывают, что из пациентов с метастатическим немелкоклеточным раком легких пятилетняя выживаемость и общая частота регрессии опухолей были выше у тех, кто дополнительно лечился мелатонином, чем у пациентов, проходивших только химиотерапию.
В то время как ни один пациент, проходивший химиотерапию, не прожил больше двух лет, пятилетняя выживаемость была достигнута у 3 из 49 пациентов, подвергавшихся химиотерапии и мелатонину.
Исследователи надеются, что аналогичные многообещающие результаты могут в конечном итоге убедить традиционных врачей назначать лечение мелатонином в сочетании со стандартными схемами лечения рака на ранних стадиях».
Важность света и темноты для синхронизации ваших внутренних часов
Производство мелатонина стимулируется темнотой и подавляется светом, поэтому его уровень выше всего перед сном. Эта прекрасно организованная система позволяет вам заснуть, когда солнце садится и проснуться с восходом солнца, а также обеспечивает эффекты против старения и борьбы с болезнями.
Если у вас проблемы со сном, это является сигналом о том, что производство мелатонина остановлено и я предлагаю вам засыпать в полной темноте и выключить свет как минимум за час перед сном. Также избегайте просмотра телевизора и использования компьютеров и других электронных гаджетов, по крайней мере, за час до отхода ко сну.
Все эти устройства излучают синий свет, что уменьшает уровень мелатонина, если вы будете работать в темноте, поэтому в идеале стоит отключить их после того, как солнце сядет. Если вам нужно их использовать, вы можете носить желтые очки, которые фильтруют синие волны и / или использовать бесплатное программное обеспечение, например f.lux.
Чтобы освещать комнаты в ночное время, используйте «бледно голубые» лампочки, которые излучают янтарный свет вместо синего, который подавляет производство мелатонина. Не менее важным фактором является качество света в течение дня. Без достаточного количества солнечного света ваш циркадный ритм может рассинхронизироваться.
Использование ламп полного спектра в доме и офисе может помочь с недостатком качественного солнечного света в течение дня, но не может полностью его заменить. Поэтому старайтесь выходить на улицу не менее чем на 30-60 минут каждый день в самую яркую часть дня, то есть около полудня. Это поможет «завести» ваш циркадный будильник и лучше спать.
Для поддержания оптимального здоровья вы должны хорошо спать
Помните, что когда ваш циркадный ритм нарушен, ваше тело вырабатывает меньше мелатонина, а это означает, что у него меньше возможностей бороться с раком и защищаться от свободных радикалов, которые могут ускорить старение и развитие болезней.
Если вы внесли необходимые изменения в свой обряд отхода ко сну и обнаружили, что у вас все еще есть проблемы, может быть полезна высококачественная добавка мелатонина.
Его количество, которое вы создаете и выпускаете каждую ночь, зависит от вашего возраста. У детей обычно гораздо более высокий уровень мелатонина, чем у взрослых, и по мере взросления он обычно продолжает уменьшаться. Вот почему некоторым пожилым людям будет полезна добавка.
То же самое касается тех, кто работает в ночную смену, часто путешествует и испытывает джет лэг или иным образом страдает от случайной бессонницы из-за стресса или других причин. Начните с дозы приблизительно от 0,25 до 0,5 мг и увеличивайте ее по мере необходимости. Если вы начинаете чувствовать себя более бодро, вы, вероятно, переборщили и нужно уменьшить дозу.опубликовано econet.ru.
Понравилась статья? Напишите свое мнение в комментариях.
Подпишитесь на наш ФБ:
.jpg)



