Почему типовые фаги нельзя использовать с лечебно профилактической целью
ГОУ ВПО “Первый МГМУ им. И.М. Сеченова” Минздравсоцразвития РФ, Москва
Бактериофаги (от слов “бактерия” и греч. phagos – пожирающий; БФ), или фаги, – специфические вирусы бактерий, вызывающие их лизис (разрушение клеток) или изменяющие их свойства. Они впервые были обнаружены микробиологами Ф. Туортом (1915) в Великобритании и Ф. д’Эрелем (1917) во Франции. Однако изучить их морфологию удалось только после изобретения электронного микроскопа.
Биология бактериофагов
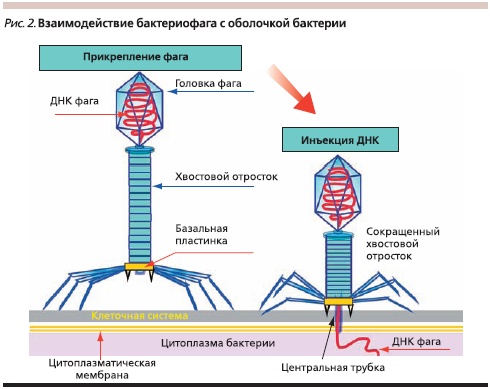
БФ состоят из белка – капсида, защищающего один тип нуклеиновой кислоты (ДНК или РНК, одно или двунитевые). Различают БФ с длинным отростком, имеющие сокращающийся или несокращающийся чехол, а также БФ с короткими отростками, аналогами отростков, без отростков и нитевидные (рис. 1, 2). Размер БФ колеблется от 20 до 800 нм (у нитевидных форм). БФ, имеющие форму сперматозоида, достигают до 200 нм длиной, состоят из хвостового отростка и головки икосаэдрического типа, содержащей нуклеиновую кислоту. Капсид головки и чехол хвостового отростка БФ состоят из полипептидных субъединиц, уложенных по икосаэдрическому (головка) или спиральному (отросток) типу симметрии. Хвостовой отросток имеет внутри полую трубку (стержень), через которую при инфицировании нуклеиновая кислота фага проходит из головки в бактерию. Чехол отростка заканчивается шестиугольной базальной пластинкой с шипами, от которых отходят фибриллы (нити). Базальная пластинка и хвостовые фибриллы участвуют в прикреплении БФ к бактериальной ячейке. Не все БФ имеют базальные пластинки и хвостовые фибриллы. В зависимости от жизненного цикла БФ могут быть вирулентными (литическими) или умеренными.
Вирулентные (литические) БФ для внедрения в бактерию адсорбируются на специфических рецепторах клетки, в т. ч. на липополисахариде, липопротеине, тейхоевых кислотах, протеинах, или даже на пилях. Специфичность рецепторов означает, что БФ может инфицировать только определенные бактерии. Попав в бактерию, БФ репродуцируется, формируя 200–500 фаговых частиц, и вызывает гибель бактерии. Это продуктивный (литический) тип взаимодействия. БФ с сокращающимся чехлом адсорбируются на клеточной стенке с помощью фибрилл хвостового отростка. Чехол хвостового отростка сокращается, и стержень с помощью ферментов (лизоцима) как бы просверливает оболочку клетки. Через канал трубки БФ нуклеиновая кислота инъецируется из головки в бактериальную клетку, а капсид БФ остается снаружи бактерии (рис. 2). Нуклеиновая кислота БФ направляет синтез его ферментов. При этом инактивируются ДНК и РНК хозяина. Нуклеиновая кислота БФ реплицируется и направляет синтез новых белков капсида. Происходят самосборка капсида вокруг фаговой нуклеиновой кислоты и формирование БФ, которые выходят из бактерии в результате ее лизиса, выталкивания или в некоторых случаях почкованием. Из бактерии высвобождается 200–1000 новых БФ, которые инфицируют другие бактериальные клетки.
Умеренные БФ взаимодействуют с бактериями по продуктивному или интегративному типу. Продуктивный тип умеренного фага, как и у вирулентных фагов, заканчивается лизисом бактерий. При интегративном типе ДНК умеренного фага встраивается в хромосому бактерии, реплицируется синхронно с бактериальным геномом, не вызывая ее лизиса (передается при делении бактерии). ДНК фага, встроенная в хромосому бактерии, называется профагом, а культура бактерий – лизогенной, сам процесс – лизогенией (от греч. lysis – разложение, genea – происхождение).
Хромосома умеренного фага лямбда, введенная в бактерию, вызывает либо лизис, либо лизогенизацию (проникшая в бактерию ДНК умеренного фага приобретает форму кольца и интегрирует в строго определенную область хромосомы). Ультрафиолетовое облучение индуцирует литический процесс с выходом фага. При лизогении фаги не образуются в результате “выключения” фаговых генов репрессором, кодируемым одним геном фага.
Профаги могут спонтанно или под действием индуцирующих агентов (ультрафиолетовые лучи, митомицин С и др.) дерепрессироваться, исключаться из хромосомы. Этот процесс заканчивается продукцией фагов (индукцией профага) и лизисом бактерий. Профаг придает бактерии новые свойства, что получило название фаговой конверсии (лат. conversio – превращение). Конвертироваться могут морфологические, культуральные, биохимические, антигенные и другие свойства бактерий. Например, наличие профага в холерном вибрионе обусловливает его способность продуцировать холерный экзотоксин.
БФ применяют для профилактики, лечения инфекций, а также для диагностики (например, для фаготипирования с целью выявления источника инфекции). Кроме того, БФ используют в генной инженерии в качестве векторов, переносящих участки ДНК; возможна также естественная передача генов между бактериями посредством трансдукции.
Фаготипирование – один из методов эпидемиологического маркирования. Применяется для выявления источника инфекции. Выделение бактерий одного фаговара от разных больных указывает на общий источник их заражения. При внутривидовой идентификации бактерий, т. е. при определении фаговара (фаготипа) бактерий с помощью фаготипирования, на чашку Петри с плотной питательной средой, засеянную чистой культурой возбудителя в виде “газона”, наносят капли различных диагностических типоспецифических фагов. Бактерии, чувствительные к фагу, лизируются (образуется стерильное пятно, “бляшка”, или т. н. негативная колония фага).
БФ – уникальное явление; они участвуют в разнообразных процессах:
Получение эффективных лечебно-профилактических БФ связано с тщательным и постоянным поиском штаммов с широким спектром (валентностью) действия на бактерии и высокой степенью их литической активности. Литическая активность и, следовательно, лечебная, а также профилактическая эффективность препаратов БФ зависят от видовой, инфравидовой принадлежности возбудителя, его рецепторных особенностей и факторов его микроокружения. Например, антитела и другие гуморальные белки могут заблокировать участки связывания бактерий с БФ, что исключает возможность парентерального введения последних. Кроме того, возможно быстрое формирование резистентности бактерий к применяемым БФ. Для получения лечебного эффекта при неблагоприятных бактериальных ассоциациях препараты БФ выпускают либо поливалентными, направленными против различных видов и сероваров одного возбудителя, либо комбинированными, содержащими БФ против различных видов возбудителя.
БФ не вызывают побочных реакций, не нарушают нормальную микрофлору. При дисбактериозе, нарушениях функций кишечника, обусловленных развитием местных воспалительных процессов, подавлении резидентной микрофлоры, происходит активация ряда условно-патогенных микроорганизмов и транзиторной микрофлоры. Эти обстоятельства поднимают значимость селективной деконтаминации, проводимой с помощью антибиотиков направленного действия и литических БФ.
БФ, обладая специфичностью действия против определенных возбудителей острых кишечных инфекций, могут также вносить вклад в развитие оральной толерантности. Известно, что организм человека проявляет пероральную (региональную) толерантность к собственной нормальной микрофлоре. Эта толерантность обусловлена блокадой активации сигнальных рецепторов (например, толл-подобных рецепторов – TLR и др.) к компонентам микрофлоры человека и активностью регуляторных T-лимфоцитов (Treg), которых в свою очередь активируют NKT-клетки (natural killer T cells). Компоненты (паттерны) БФ и разрушенных ими бактерий могут активировать определенные сигнальные рецепторы клеток организма, стимулирующие синтез антимикробных пептидов, подавляющих развитие наиболее агрессивных микробов (рис. 3). Срыв оральной толерантности влечет развитие различных нарушений, в т. ч. хронического гастрита, болезни Крона, неспецифического язвенного колита, некротизирующего энтероколита у детей, язвенной болезни желудка и двенадцатиперстной кишки.
Препараты БФ хранят при температуре 2–10 °С в сухом темном месте. БФ чувствительны к ультрафиолетовым лучам; даже их непродолжительное пребывание на свету приводит к утрате литической активности. Для защиты БФ от действия желудочного сока их выпускают в капсулах или таблетках, покрытых кислотоустойчивой оболочкой. Материалом защитного покрытия является нетоксичная целлюлоза, эстерифицированная уксусной и фталевой кислотами, образующая гладкую прозрачную пленку. Для детей из-за проблем проглатывания таблеток используют пектиновое покрытие. Пектин, обволакивая БФ, защищает их от разрушающего действия желудочного сока.
Нормализация микрофлоры, возможное участие БФ в поддержании колонизационной резистентности и оральной толерантности обеспечивают стабилизацию гуморального и клеточного звеньев иммунитета. Изредка применение БФ совпадает с ухудшением качества стула из-за массовой гибели чувствительных к нему бактерий. В этом случае для уменьшения интоксикации целесообразно назначать на ночь энтеросорбент – не ранее 3–4 часов после последнего приема БФ.
Препараты бактериофагов против возбудителей кишечных инфекций
Интести-бактериофаг жидкий содержит стерильные фильтраты фаголизатов шигелл (S. flexneri сероваров 1, 2, 3, 4, 6 и S. sonnei), сальмонелл (S. paratyphiA, S. paratyphiB, S. typhimurium, S. choleraesuis, S. infantis, S. oranienburg, S. enteritidis), энтеропатогенных кишечных палочек наиболее этиологически значимых сероваров (Escherichia coli О111, О55, О26, О125, О119, О128, О18, О44, О25, О20), протея (вульгарис и мирабилис), стафилококков, энтерококков и синегнойной палочки (Pseudomonas aeraginosa). Интести-бактериофаг (Bacteriophagum intestinalis fluidum) представляет собой прозрачную жидкость желтого цвета различной интенсивности.
Препарат предназначен для лечения и профилактики заболеваний желудочно-кишечного тракта, вызванных вышеуказанными бактериями, их сочетанием (в т. ч. бактериальной дизентерии, сальмонеллеза, брюшного тифа, паратифа, дисбактериоза, энтероколита, колита, диспепсии). Его назначают в остром периоде болезни: монотерапия при легких и стертых формах, при бактериовыделении; комбинированная терапия с другими антибактериальными средствами (при среднетяжелом течении) или иммуномодуляторами (при затянувшемся бактериовыделении). Залогом эффективности использования интести-бактериофага является определение фагочувствительности возбудителя и раннее применение препарата, который назначают перорально или ректально при помощи клизмы. Перорально интести-бактериофаг назначают 3–4 раза в сутки натощак за 1,0–1,5 часа до еды в течение 7–10 дней и в разовой дозе: детям до 6 месяцев – 5–10 мл, 6–12 месяцев – 10–15 мл, 1–3 года – 15–20 мл, старше 3 лет – 20 – 40 мл (см. таблицу). Для детей первых месяцев жизни назначенный препарат в первые двое суток разводят кипяченой водой в 2 раза. Если побочные осложнения отсутствуют (срыгивания, высыпания на коже), препарат назначают неразведенным. Перед приемом интести-бактериофага детям старше 3 лет и взрослым назначают раствор питьевой соды (0,5 чайной ложки на 0,5 стакана воды) или щелочную минеральную воду. В отсутствие колитического синдрома препарат назначают ректально 1 раз в день после опорожнения кишечника.
Бактериофаг дизентерийный поливалентный (в таблетках с кислотоустойчивым покрытием и в свечах) содержит стерильные фильтраты фаголизатов шигелл (S. flexneri и S. sonnei). Применяют с 6-месячного возраста для лечения и профилактики бактериальной дизентерии. Для лечения его применяют перорально 3 раза в сутки за час до еды в течение 5–7 дней и в разовой дозе: для детей от 6 месяцев до 3 лет – по 1 таблетке, 3–8 лет – по 1–2 таблетки, старше 8 лет – 2–3 таблетки. При слабовыраженном колитическом синдроме и в период реконвалесценции третий прием БФ внутрь можно заменить его ректальным применением: с 6 месяцев до 3 лет – 20–40 мл, с 3 до 8 лет – 40–60 мл, старше 8 лет – 60–80 мл.
С профилактической целью рекомендуют ежедневный прием препарата в зависимости от возраста: по 10–40 мл или 1–2 таблетки.
Бактериофаг сальмонеллезный групп A, B, C, D, E в таблетках с кислотоустойчивым покрытием, в свечах, жидкий содержит стерильные фильтраты фаголизатов сальмонелл (S. paratyphi A, S. paratyphi B, S. typhimurium, S. heidelberg, S. newport, S. choleraesuis, S. oranienburg, S. infantis, S. dublin, S. enteritidis, S. anatum, S. newlands). Для лечения его применяют перорально 3 раза в день за час до еды в течение 7–10 дней и в разовой дозе: для детей 6–12 месяцев – по 0,5 таблетки; 1–3 лет – по 0,5–1,0; 3–8 лет – по 1,0; старше 8 лет – по 2 таблетке. Третий пероральный прием можно заменить ректальным введением препарата. С профилактической целью БФ назначают детям по 1 таблетке и взрослым по 2 таблетке 2 раза в неделю.
Бактериофаг брюшнотифозный в таблетках с кислотоустойчивым покрытием содержит стерильный фильтрат фаголизата сальмонелл брюшного тифа (S. typhi). Препарат назначают для профилактики брюшного тифа внутрь за час до еды детям от 6 месяцев до 3 лет по 1 таблетке, а старше 3 лет и взрослым – по 2 таблетке 1 раз в 3 дня или каждый день до выздоровления.
Бактериофаг колипротейный жидкий содержит стерильные фильтраты фаголизатов энтеропатогенных (диареегенных) кишечных палочек (Escherichia coli наиболее распространенных серологических групп O20, O26, O33, O44, O55, O111, O119, O26, O124, O125, O127, O151), Proteusvulgarisи Proteusmirabilis. Препарат предназначен для лечения и профилактики заболеваний, вызванных вышеуказанными бактериями, а также дисбактериоза.
Сфера применения других препаратов бактериофагов многообразна; они используются как для местного применения (“раневые” бактериофаги), так и для приема перорально или ректально, в т. ч. в зависимости от формы выпуска:
В заключение следует отметить, что БФ и препараты БФ характеризуются многими положительными сторонами, они:
Информация об авторах:
Быков Анатолий Сергеевич – доктор медицинских наук, профессор кафедры микробиологии,вирусологии и иммунологии ГОУ ВПО “Первый МГМУ им. И.М. Сеченова” Минздравсоцразвития РФ.
Тел. 8 (495) 629-75-79, e-mail: bykov@imail.ru;
Быков Сергей Анатольевич – кандидат медицинских наук, ассистент кафедры клиническойиммунологии и аллергологии ГОУ ВПО “Первый МГМУ им. И.М. Сеченова” Минздравсоцразвития РФ.
Литература
1. Атлас по медицинской микробиологии, вирусологии и иммунологии / 2-е изд. Под ред. А.С. Быкова, А.А. Воробьева, В.В. Зверева. М., 2008. C. 272.
2. Дарбеева О.С., Жиленков Е.Л. Бактериофаги. Общая и санитарная микробиология с техникой микробиологических исследований: учебное пособие / Под ред. А.С. Лабинской, Л.П. Блинковой, А.С. Ещиной. М., 2004. C. 576.
3. Урсова Н.И., Минухина А.М. Бактериофаги. Клинико-иммунологическая эффективность иммунобиологических препаратов / Под. ред. М.П. Костинова, Н.В. Медуницина. М., 2008. C. 256.
Бактериофаготерапия на современном этапе
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Введение
Человек живет впостоянном контакте исложнейшем взаимодействии снеисчислимым множеством микроорганизмов. Жить без микробов невозможно, ноисмногими изних— тоже. Ежегодно, посамым скромным оценкам, неучитывающим недоступные для статистики ВОЗ данные многих развивающихся стран, погибает отпневмонии 3,9млн человек, отдиареи— 1,6млн, оттуберкулеза— 1,6млн [1].
Человек живет в постоянном контакте и сложнейшем взаимодействии с неисчислимым множеством микроорганизмов. Жить без микробов невозможно, но и с многими из них — тоже. Ежегодно, по самым скромным оценкам, не учитывающим недоступные для статистики ВОЗ данные многих развивающихся стран, погибает от пневмонии 3,9 млн человек, от диареи — 1,6 млн, от туберкулеза — 1,6 млн [1].
С учетом нарастающей резистентности флоры к антибиотикам, вероятности аллергических и токсических реакций возникает проблема: что применять вместо антибиотиков или в комплексе с ними?
Строение и микробиология фага
Бактериофаги — древнейшие вирусы, наиболее распространенный в биосфере биологический объект. Чистая природная вода содержит в 1 мл 2×108 фагов, на каждую бактериальную единицу приходится не менее 10 фаговых [5, 6].
Принципы выбора терапии бактериофагами
В многочисленных отечественных и зарубежных публикациях продемонстрирована эффективность применения бактериофагов, генетически модифицированных, в лечении поверхностной и системной инфекций [8, 9]. Лечение фагами привлекательно по следующим причинам:
1. Бактериофаги высокоспецифичны и лизируют только «вредные микробы». Специфичность фагов варьирует от крайне избирательной к определенным бактериям (используется в типировании микробов) до относительно широкого спектра лизируемых бактерий. Но даже в этом случае широта воздействия не достигает широты действия антибиотиков. Поэтому, например, при лечении фагами не изменяется естественная флора кишечника, а для лечения инфекций требуется препарат, содержащий несколько фагов (по аналогии с поливалентным препаратом Секстафаг® (пиобактериофаг поливалентный)).
3. Бактериофаги эффективны против микробов. Частота выделения мультирезистентной флоры варьирует, по данным разных клиник, от менее 1 до 42% [10, 11], что определяется, по нашему мнению, только профилем клиники и контингентом пациентов. В условиях нарастающей резистентности бактериальной флоры к антибиотикам многие авторы рассматривают фаготерапию как решение проблемы. Бактериофаги «чисты», безопасны в применении.
При применении бактериофагов следует учитывать, что специфичность фагов может ограничивать их применение в острых случаях.
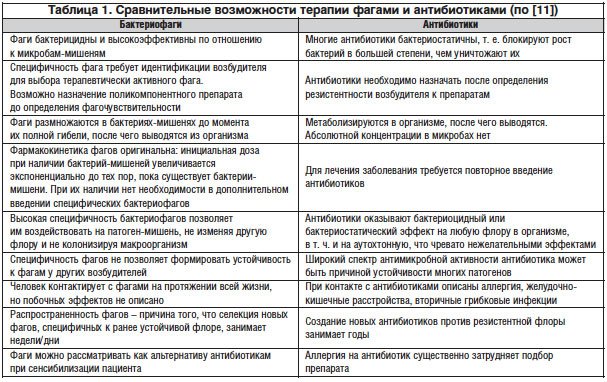
Соотношение бактериофаго- и антибиотикотерапии представлено в таблице 1.
Фаготерапия покровных и барьерных структур тканей
В эксперименте [14, 15] была показана эффективность фагов в лечении кожных инфекций и внутримышечных абсцессов (Pseudomonas (Ps.) aeruginosa, Staphylococcus (S.) aureus). В клинической практике эффективность лечения инфекций ран, инфицированных пострадиационных некрозов была продемонстрирована K. Markoishwili et al. [16] и другими представителями школы грузинского ученого Г. Элиавы.
В нашей стране для наружного применения используют комплексные фаговые препараты. Препарат пиобактериофаг поливалентный (Секстафаг®) для приема внутрь (20 мл 3 р./сут, 7–15 дней), местно или наружно способен лизировать стафило- и стрептококки, патогенные кишечные и синегнойные бактерии (Proteus mirabilis, Proteus vulgaris, Klebsiella pneumoniae). Это позволяет применять его при заболеваниях уха, горла, носа, дыхательных путей, легких и плевры (воспалении пазух носа, среднего уха, ангине, фарингите, ларингите, трахеите, бронхите, пневмонии, плеврите). Секстафаг®, являясь эффективной альтернативой антибиотикам, может также применяться с ними комплексно. Крайне важно, что препарат может применяться при заболеваниях у новорожденных и детей грудного возраста (омфалит, гастроэнтероколит), беременных и рожениц. Все это подчеркивает безопасность препарата.
Гель Отофаг применяют местно в дозировке 1–2 мл: для профилактики рецидивов заболеваний — 2–3 р./сут в течение 7–10 дней, при наличии бактериального воспалительного заболевания — 2–3 р./сут в течение 7–14 дней.
Применение фагов как профилактического, лечебного и противорецидивного средства продемонстрировало свою эффективность в самой частой педиатрической группе: пациенты с инфекционной патологией верхних дыхательных путей (риносинуситы, тонзиллиты, ларингиты, фарингиты). Обычно эти инфекции трактуются как вирусные, хотя достаточно часто причиной бывают и бактерии, или бактериальная флора активируется в процессе манифестации вирусной инфекции.
Подавляющее большинство всех случаев острых заболеваний детей, особенно младшего возраста, вызваны острой респираторной инфекцией (ОРИ). Первичная заболеваемость детей и подростков по г. Москве за колебалась от 1680,2‰ до 1763,6‰3. Заболеваемость болезнями органов дыхания за этот же период составила 1147,4–1188,8‰. Общий экономический ущерб от заболеваний гриппом детей и взрослых в 2008 г. составил 375,2 млрд руб. Заболеваемость ОРВИ детей и подростков до 17 лет в 8,3 раза выше, чем взрослых. Так, при совместных исследованиях с [17] было показано, что на первом году жизни частота эпизодов ОРИ составляет 1535,9:1000, у детей достигает 3796,29:1000. Даже если первоначально заболевание разворачивается как вирусное, то впоследствии часто присоединяется бактериальная флора или активируется собственная, что требует взвешенного решения о выборе препарата или сочетании антибиотиков с иными препаратами, бактериофагами.
Инфекционный ринит дебютирует первоначально, как правило, как вирусный с типичным водянистым или отделяемым. Появление отделяемого, лихорадки, боли в области придаточных пазух говорит о присоединении бактериальной флоры. В качестве профилактики такого развития заболевания можно обсуждать местное применение поливалентного бактериофага.
Присоединение бактериальной инфекции с ее распространением на придаточные пазухи носа приводит к синуситу. Любые нарушения цилиарного клиренса, вентиляции, местного или системного иммунного ответа создают условия для хронизации синусита, вылечить который без воздействия на первоначальные причины невозможно. Признаки синусита:
К признакам тяжелого течения синусита или его осложнений относятся гнойная ринорея, лихорадка выше 39ºС и периорбитальный отек. При остром и подостром синусите чаще обнаруживают Streptococcus pneumoniae, реже — Haemophilus (H.) influenzae, Moraxella catarrhalis, Streptococcus pyogenes (β-гемолитический). Хронический синусит чаще полимикробный, вызывается α-гемолитическим стрептококком, S. aureus, коагулазонегативными стафилококками, нетипичными H. influenzae, а также Moraxella catarrhalis и анаэробными бактериями (Peptostreptococcus spp., Prevotella, Bacteroides, Fusobacterium spр.), после многих курсов антибиотиков (или у иммунокомпрометированных пациентов) — Pseudomonads. Эти сведения еще раз заставляют оценить место и роль поливалентных бактериофагов в комплексном лечении синуситов.
При лечении риносинуситов препаратом пиобактериофаг путем его местного введения в пазухи отмечено значительное улучшение, нормализовались показатели завершенности фагоцитоза, что указывало на снижение интенсивности воспаления с восстановлением адекватного иммунного ответа слизистых оболочек носа. Таким образом, препарат пиобактериофаг поливалентный (Секстафаг®) обладает противовоспалительными и иммунорегуляторными свойствами, что проявляется нормализацией показателей местного иммунитета. В то же время применение антибиотиков при лечении больных хроническим гнойным риносинуситом сопровождается сохранением признаков воспаления в виде активации нейтрофильного звена иммунной системы, увеличением внеклеточной пероксидазной активности и угнетением процесса фагоцитоза с нарушением механизмов завершенности в клетках [18]. Пиобактериофаг при местном введении в пазухи улучшает показатели завершенности фагоцитоза, что свидетельствует о снижении интенсивности воспаления с восстановлением адекватного иммунного ответа слизистых оболочек носа [19].
Большой проблемой педиатрии являются тонзиллофарингиты, аденоидиты. За 1 год не менее 10% всей детской популяции переносят тонзиллофарингит, из них у 25–50% причиной является стрептококк группы А. 20% здоровых детей являются носителями стрептококка, А [20, 21]. Хроническая гипертрофия аденоидных вегетаций может приводить к нарушению естественного дренирования евстахиевых труб и восхождению инфекции в среднее ухо. Рецидивирующий аденоидит — самая частая причина кашля у детей: стекающая с воспаленной поверхности небной миндалины слизь («постназальная капель») раздражает верхние дыхательные пути и вызывает кашель. Чаще всего на аденоидных вегетациях обнаруживают H. influenzae, Streptococcus (S.) β-hemolytic гр. А, S. aureus, Moraxella (M.) catarrhalis, Streptococcus (S.) pneumoniae (по убывающей). При аденоидитах причинами среднего отита и риносинусита у детей чаще бывают антибиотикорезистентные H. influenzae, M. catarrhalis, S. pneumoniae [22]. Безусловно, это служит основанием для топического применения специфических фагов, хотя и отечественные авторы, с надеждой указывающие на это направление, ссылаются на недостаточную доказательность фаготерапии хронического аденоидита в детской практике [23]. Другие исследователи более оптимистичны. Показано, что введение в комплекс терапии при хроническом аденоидите местного бактериофага приводило к существенному улучшению результатов [24]. Но непосредственный эффект лечения и отдаленные последствия, видимо, во многом определяются генетически. В сравнительном исследовании по проверке гипотезы положительного влияния хирургического удаления аденоидов и миндалин на вероятность развития осложнений, связанных со стрептококковой инфекцией, показано, что значительной разницы в титре антистрептококковых антител, связанных со S. β-hemolytic гр. А детских аутоиммунных нейропсихиатрических нарушений, расстройств и тиков между оперированными и неоперированными детьми нет [25].
При обследовании пациентов с компенсированной формой хронического тонзиллита S. aureus выделен у 92,5%. Чувствительность культур золотистого стафилококка к стафилококковому бактериофагу оказалась очень высокой (97,4%). По результатам монотерапии специфическим бактериофагом и комбинированного лечения зарегистрированы клиническое улучшение и уменьшение высеваемости S. aureus со слизистой оболочки миндалин [26].
Обострения хронического ларингита сопровождается обсеменением слизистой гортани патогенной микрофлорой. Использование в комплексном лечении таких пациентов специфического бактериофага в виде инстилляций в гортань, а в случае тяжелого обострения — в виде приема внутрь позволяет существенно сократить продолжительность лечения, значительно повышая его качество, достичь более длительной ремиссии болезни и снизить частоту обострений [27].
Эффективность бактериофаготерапии у иммунокомпрометированных пациентов доказана в зарубежных исследованиях [28].
Бактериофаги продемонстрировали эффективность при лечении инфекции, находящейся под биопленкой. Биопленка — плотная колония микроорганизмов на поверхности биологических или небиологических сред, окружающих себя секретируемым экстрацеллюлярным полимером, практически непроницаемым для антибиотиков. Способность бактерий образовывать биопленку — важнейшее условие их выживания на поверхности тканей или медицинских объектов (катетеры, имплантаты). свойства биопленок позволили выдвинуть идею о кооперированных микробных группах как аналогах многоклеточных организмов и социобиологических общностей [29]. Разрушение биопленки возможно при применении фагов [30]. В частности, обработка катетеров перед их постановкой коагулазонегативными фагами резко снижает вероятность образования биопленки Staphylococcus epidermidis [31].
Применение бактериофагов известно также при собственно кишечных инфекциях [32] и при сепсисе, вызванном кишечной инфекцией Ps. aeruginosa [33]. При этом в эксперименте прием бактериофага per os привел к 67% выживаемости в экспериментальной группе животных и к 0% в контрольной.
Особое внимание привлекает возможность бактериофаготерапии при внутренних и системных инфекциях. Большинство таких исследований принадлежит отечественным ученым. Показано, что совместное применение бактериофагов и антибиотиков в лечении детей с осложненной инфекцией мочевыводящих путей значительно эффективней, чем изолированная антибиотикотерапия [34].
[35] пролечено 36 детей в возрасте от 14 дней до 3 лет с тяжелыми заболеваниями бронхолегочной системы с наличием в мокроте синегнойной и кишечной палочек, клебсиеллы, энтерококка, стафилококка, которые, будучи нозокомиальной флорой, в большинстве случаев были нечувствительны к большинству известных антибиотиков. Путем ингаляций вводили моно- или поливалентные бактериофаги, пиобактериофаг. Курс антибактериальной терапии сократился с 13–17 до 8–11 дней. Элиминация возбудителя и уменьшение воспаления в трахеобронхиальном дереве подтверждались контрольным бактериологическим посевом и цитологическим исследованием мокроты: эффективность составила 88,8%. Использование поливалентных фагов явилось более оправданным по сравнению с монофагами на фоне элиминации основного бактериального агента в меньшей мере происходила параллельная контаминация другими, не менее вирулентными, микробами. Таким образом, применение небулайзеротерапии бактериофагами в комплексном лечении острых и хронических обструктивных бронхолегочных заболеваний, включая муковисцидоз, показало высокую клиническую эффективность, позволило сократить сроки лечения дорогостоящими антибиотиками широкого спектра, уменьшить риск развития кандидоза. В эксперименте на животных, моделирующем лечение муковисцидоза, введение бактериофага при тяжелой пневмонии, вызванной Ps. aeruginosa, сопровождалось резким повышением выживаемости в подопытной группе [36].
Есть много нерешенных проблем, которые сводятся к организации многоцентровых исследований по принципам доказательной медицины, соотношению антибиотиков и бактериофагов при лечении.
В любом случае можно утверждать, что это направление перспективно и достаточно обнадеживающе, особенно при инфицировании резистентными штаммами.
Разнообразие лекарственных форм бактериофагов (таблетки, гели, растворы) позволяет применять их как перорально, так и наносить на раневые поверхности, вводить в полости организма. Препараты бактериофагов широко применяются в педиатрии, акушерстве и гинекологии, офтальмологии Например, назначение по поводу кесарева сечения препарата Секстафаг®, предварительно адаптированного к флоре, циркулирующей в конкретном учреждении, приводило к снижению осложнений (18,7%) в большей степени (26,7%), чем в группе женщин, получавших антибиотикопрофилактику.
Заключение
В настоящее время в большинстве публикаций указывается на безопасность фаготерапии; хорошо организованные двойные слепые рандомизированные контролируемые исследования позволят определить безопасность и эффективность фагов как альтернативы антибиотикам при инфекциях с полирезистентной флорой [39]. Дальнейшее изучение возможностей бактериофаготерапии будет зависеть от объективной заинтересованности медицинского сообщества, проведения многоцентровых независимых исследований, развития вирусологии с ее возможностями получения новых чистых препаратов фагов.
1 Сборник среднемосковских основных показателей деятельности учреждений Департамента здравоохранения г. Москвы за М., 2009. 87 с.
2 Выбор инфекционного агента для опытов не был случайным: отец был известным микробиологом, написавшим монографию о сибиреязвенной палочке, переведенную и на немецкий язык.
3 Департамент здравоохранения г. Москвы. Доклад о состоянии здоровья населения г. Москвы в 2008 г.
Только для зарегистрированных пользователей