Злокачественные опухоли головного мозга
Злокачественные новообразования центральной нервной системы очень агрессивны, быстро растут и разрушают ткань мозга. При их обнаружении операцию по удалению опухоли желательно проводить как можно раньше, до развития тяжелого необратимого неврологического дефицита.
Нейрохирурги клиники НАКФФ проводят сложнейшие операции при глиобластомах и других новообразованиях ЦНС высокой степени злокачественности. Врачи могут безопасно удалить даже глубоко залегающие опухоли, так как перед вмешательством они выявляют функционально важные зоны мозга, чтобы не повредить их во время операции.
Какие бывают злокачественные опухоли мозга
Самые распространенные опухоли мозга – это глиомы и менингиомы. Первая группа развивается из мозговой ткани, вторая – из оболочек мозга. Большинство менингиом – доброкачественные, и только 1% приходится на менингиомы третьей, самой высокой степени злокачественности. В то же время большинство глиом – злокачественные.
Самая частая опухоль этого типа – глиобластома. Для глиом выделяют 4 степени злокачественности новообразований, и глиобластома имеет четвертую, самую высокую степень. Проблема её лечения заключается в том, что она часто располагается в глубине мозга, и до неё трудно добраться. К тому же, опухоль не имеет четкой границы: она врастает в окружающие здоровые ткани.
Даже самые агрессивные новообразования обычно не дают метастазов за пределы центральной нервной системы. Но они распространяются в пределах мозга, а при росте разрушают окружающие здоровые ткани.
На практике нейрохирургу, который оперирует взрослых пациентов, среди всех злокачественных новообразований чаще всего приходится сталкиваться с глиобластомой или метастатическими опухолями рака другой локализации. Большинство других образований встречаются очень редко или имеют доброкачественную природу.
Как лечат опухоли мозга?
Чаще всего для лечения опухолей мозга используют три метода:
Самый эффективный способ лечения – хирургическая операция. Два других способа имеют множество недостатков, поэтому применяются как дополнительные методики или у пациентов с противопоказаниями к операции.
Проблема медикаментозного лечения состоит в том, что большинство препаратов плохо проникают через гематоэнцефалический барьер. К тому же, успехи лечения далеко не самые выдающиеся. При глиобластоме стандартный препарат для химиотерапии увеличивает продолжительность жизни человека в среднем на 10 недель.
Методы лучевой терапии часто позиционируются как альтернатива операции. Пациентов впечатляют и названия процедур: Кибернож, Гамма-нож. Складывается впечатление, что опухоль «вырезается» из головы радиацией, быстро и безболезненно. Но правда заключается в следующем:
В силу этих причин лучевая терапия всё же не считается основным радикальным методом лечения злокачественных новообразований мозга и не может использоваться как альтернатива операции. Облучение должно дополнять, а не замещать нейрохирургический метод лечения. Если лучевая терапия применяется вместо, а не в дополнение к операции, то такие случаи связаны исключительно с глубоким залеганием опухоли, до которой нельзя добраться из-за угрозы тяжелого неврологического дефицита, или наличием медицинских противопоказаний к операции.
Преимущества хирургического вмешательства:
Как проводят операцию?
Нейрохирургические операции по удалению злокачественных опухолей – сложные и высокотехнологичные. Врачу важно удалить новообразование полностью, и при этом не повредить функционально значимые зоны мозга.
Процедуры, определяющие успех операции, часто начинаются ещё до её начала. Врачи проводят тщательное обследование пациента, особенно при глубоком залегании опухоли. Они определяют границы опухоли при помощи ПЭТ или функциональной МРТ. Затем требуется выявление функционально значимых зон, чтобы обойти их, рассекая мозговую ткань. Для этого используется функциональное картирование и электрофизиологическое исследование. При необходимости исследования могут быть выполнены прямо во время операции.
Операция проводится под стереотаксическим контролем. Стереотаксис позволяет врачу идеально ориентироваться внутри черепа пациента. Классический вариант подразумевает использование жесткой рамы, которую фиксируют винтами к надкостнице. В последние годы получили распространение системы безрамного стереотаксиса.
Важнейшая задача нейрохирурга, определяющая успех операции, состоит в полном удалении опухоли. Но для этого её нужно отличить от здоровой ткани. Выглядят они практически одинаково. Чтобы найти границы новообразования, используется флуоресцентная диагностика и лазерная спектроскопия. Врач использует вещество, которое поглощается патологическими клетками и заставляет их светиться.
Немецкое исследование с участием 350 пациентов показало, что без флуоресцентной диагностики только у 1 из 3 пациентов глиобластому удается удалить полностью, а при её использовании – в 2/3 случаев. Вероятность отсутствия рецидива опухоли в течение 6 месяцев после операции увеличивается в 2 раза.
Химиотерапия при раке: что влияет на эффективность лечения
Химиотерапия (ХТ) – один из основных методов лечения онкологических пациентов. Использование современных протоколов в совокупности с комплементарной и поддерживающей терапией, полноценной реабилитацией позволяют онкологам свести к минимуму осложнения и улучшить результат лечения. Разбираемся, какие еще факторы повышают эффективность химиотерапии.
От чего зависит эффективность химиотерапии?
Полностью исключить неблагоприятное действие химиопрепаратов на организм человека невозможно, так как они содержат высокотоксичные вещества – цитостатики. Цитостатики наносят вред не только опухолевым, но и здоровым клеткам, пусть и в меньшей степени.
Эффективность химиотерапевтического лечения рака зависит от ряда факторов, включая:
Когда лучше начинать химиотерапию?
Решение о начале лечения принимает врач в зависимости от конкретной ситуации. Если химиотерапия проводится в комплексе с операцией, то она может назначаться перед ней либо после. В первом случае химиотерапия называется неоадъювантной, во втором – адъювантной.
Любой способ воздействия на злокачественную опухоль приносит наилучший результат на самых ранних стадиях, когда новообразование еще не вышло за пределы органа, не «обзавелось» собственными сосудами, не создало комфортную «среду обитания».
Химиотерапия – не исключение. Но из-за токсичности при раннем обнаружении заболевания ее назначают не всегда. Например, если опухоль можно полностью удалить и риск рецидива ничтожен, онколог может назначить только операцию.
Некоторые виды рака очень агрессивны и начинают метастазировать раньше, чем дают о себе знать и становятся заметны на снимках. В случае с такими опухолями химиотерапию обычно назначают сразу же.
Кроме того, химиотерапия может показывать хорошие результаты при прогрессирующем раке – рост опухоли останавливается, метастазы исчезают, состояние человека улучшается.
Можно определить заранее, поможет ли химиотерапия?
К сожалению, врач способен только предположить вероятность и полноту ответа опухоли на действие цитостатиков. Однако сейчас это можно сделать с достаточно высокой точностью. Например, химиотерапевты ведущих современных онкоцентров имеют возможность спрогнозировать эффективность химиотерапии с помощью молекулярно-генетического теста. Точность такого прогноза около 80%. Остальным 20% пациентов потребуется скорректировать лечение – подобрать другие препараты, изменить дозы, количество курсов и их продолжительность.
Эффективность химиотерапии может меняться
Рак коварен и «воюет до последнего солдата»: если после окончания химиотерапии в организме осталась хотя бы одна жизнеспособная раковая клетка, из нее рано или поздно вырастет новая опухоль – рецидивы могут повторяться неоднократно. Химиопрепараты, с помощью которых удалось быстро и без серьезных осложнений вывести пациента в ремиссию, при рецидивах часто оказываются малоэффективными или бесполезными, потому что вновь образовавшиеся опухоли приобретают устойчивость ко всем ранее использованным препаратам. В этом случае врачи переходят к другим схемам лечения – химиотерапии второй линии. При повторных рецидивах схему химиотерапии снова приходится менять, переходя к противоопухолевым средствам третьей, четвертой линии.
Как онкологи добиваются максимальной эффективности химиотерапии
В каждом конкретном случае вопрос о необходимости назначения химии, ее составе, схеме и объеме решается лечащим врачом, а нередко и консилиумом:
Во время химиотерапии онкологический пациент находится под постоянным врачебным контролем. При низкой эффективности лечения или ее отсутствии врач корректирует дозы, кратность и продолжительность курсов, принимает решение о смене препаратов.
Для повышения лечебного эффекта параллельно с системной химиотерапией, при которой препарат вводится в кровь и распространяется по всему организму, пациенту могут назначить внутриполостные инъекции цитостатиков, в частности:
Научный редактор текста: Екатерина Коробейникова, онколог-химиотерапевт, резидент Высшей школы онкологии
Радикальные операции при раке
Радикальными называют операции, во время которых полностью удаляют злокачественную опухоль. После этого наступает ремиссия: по результатам контрольных обследований в организме пациента больше не обнаруживаются опухолевые очаги.
Радикальные операции обычно возможны на ранних стадиях рака — I и II. На III стадии, когда опухоль вторглась в окружающие ткани и/или распространилась в регионарные лимфатические узлы, в ряде случаев её всё ещё возможно удалить. При IV стадии рака с метастазами радикальное хирургическое лечение, как правило, невозможно. Иногда встречаются случаи, когда в организме больного есть лишь единичные метастатические очаги в одном органе, и их можно удалить, так же, как первичную опухоль. Но такие случаи, к сожалению, очень редки.
В международной клинике Медика24 выполняются практически все виды хирургических вмешательств при онкологических заболеваниях любой сложности. У нас работают ведущие хирурги-онкологи, торакальные хирурги, нейрохирурги и другие врачи-специалисты. Вмешательства выполняются в операционных, оснащенных современным оборудованием. При необходимости наши врачи дополняют радикальную операцию другими видами лечения, например, химиотерапией, таргетной терапией. Современные реабилитационные программы помогают нашим пациентам в кратчайшие сроки восстанавливаться после хирургических вмешательств и возвращаться к полноценной жизни.
Наши врачи вам помогут
Виды радикальных операций в онкологии
Типичный объем радикальной операции при раке — когда удаляют часть органа, пораженную злокачественной опухолью, или весь орган целиком, а также некоторое количество регионарных лимфатических узлов. В некоторых случаях, когда есть подозрение, что рак успел сильно распространиться в организме, приходится удалять большее число лимфатических узлов. Такая радикальная операция называется расширенной.
Основные виды радикальных операций:
Принципы выполнения радикальных операций при раке
Важная особенность операций в онкологии в том, что хирург должен принять некоторые специальные меры, чтобы не оставить в организме пациента раковых клеток и не допустить их распространения. Необходимо придерживаться принципов абластики и антибластики.
Принципы абластики и антибластики:
| Абластика | Антибластика |
| Хирург должен тщательно отграничить операционную рану от окружающих тканей. | Меры, направленные на укрепление устойчивости, защитных сил организма. |
| Нужно применять электроскальпели и лазерные скальпели: они сразу прижигают рану и предотвращают распространение опухолевых клеток. | Сочетание хирургического лечения с химиотерапией, лучевой терапией. |
| Все тупферы и марлевые шарики можно использовать только один раз, а затем их нужно сразу выбрасывать. | В некоторых случаях противоопухолевые препараты и облучение применяют прямо во время операции. |
| Каждые 30–40 минут меняют хирургические перчатки, инструменты. | Хирурги принимают некоторые специальные меры, чтобы не дать опухолевым клеткам прикрепиться к нормальным тканям. |
| Все кровеносные сосуды, подходящие к пораженному органу, перевязывают до того, как их пересечь. | |
| Пораженный орган удаляют с захватом некоторого количества окружающих тканей единым блоком с лимфатическими узлами и клетчаткой. |
Позаботьтесь о себе, запишитесь на консультацию сейчас
Почему злокачественную опухоль нельзя удалить
Ранний визит к врачу может спасти жизнь человека, но иногда осторожность доходит до абсурда. Пациенты рискуют залечить себя во вред здоровью, и врачи не имеют право отказать в опасных процедурах. Бывает, что незнание — тоже сила.
Медикам и ученым еще предстоит выяснить, где проходит золотая середина между осмотрительностью и излишним усердием. Проблемная область — онкологические заболевания.
Границы разумного
Еще задолго до пандемии медицина стала одной из главных тем в поисковиках и новостных заголовках. Коронавирус обострил ситуацию, и теперь каждый стал «экспертом» в вопросах профилактики и лечения любых недугов. При этом многие люди по-разному реагируют на поток информации. Кем-то завладевает тревожность, и вперед выступает бэконовский лозунг «Знание — сила». Внутренний голос подсказывает, что пора бы сходить в больницу на проверку, даже если нет симптомов. Сперва кажется, что подобная осторожность спасительна. Но так ли это?
«В самой практике обращения к врачу с беспокоящими вопросами и прохождении периодических медицинских обследований нет ничего плохого. Во многих случаях это позволяет выявить проблемы со здоровьем на ранней стадии, в том числе не касающиеся онкологии, и предотвратить развитие более серьезных заболеваний и состояний. Вредной эта практика становится, если обращения и обследования выходят за рамки разумного и не соотносятся с клиническими рекомендациями», — рассказал врач-онколог Консультативно-диагностического центра НМИЦ онкологии им. Н.Н. Петрова Игорь Якубенко.
«Рамки разумного» — субъективное понятие. И все же медицинской практике известны конкретные примеры. Один из них — проверка здорового человека на онкомаркеры. Большинство тестов не используются в диагностике злокачественных новообразований. Анализ может показать отклонения от нормы, которые на деле связаны с другими проблемами в здоровье. Рак здесь не при чем. Пациент же паникует, и требует все новые и новые исследования, пока не залечится во вред себе.
«Другой частый пример — выполнение КТ или МРТ без показаний. Достаточно часто выявляются разного рода отклонения, которые, вероятнее всего, были у человека с рождения или представляются доброкачественными, но однозначно определить их истинную природу можно только с помощью сложных инвазивных методов, а иногда даже операций. Это некомфортно и страшно для любого пациента, дорого для системы здравоохранения и можно было бы легко избежать», — уверен Игорь Якубенко.
Безвредное соседство
Представьте, что в вашем организме прижилась опухоль, о которой вы не знаете. Она вас совсем не беспокоит, самочувствие как всегда приподнятое, ничего не болит. Захотите ли вы узнать об ее существовании? Большинство людей ответят утвердительно, и понять такую позицию можно. Чем раньше обнаружить рак, тем больше шансов справиться с ним и продолжить полноценную жизнь.
И все же есть опухоли, с которыми человек может спокойно жить. Скорее всего, в конечном итоге он умрет вместе с ними, а не от них. И порой к лечению лучше не прибегать. Лучше было бы совсем не знать о недуге.
«Гипердиагностика — это выявление злокачественного новообразования у человека, которое не способно причинить вред здоровью, вызвать серьезные симптомы и привести к смерти. Существуют некоторые виды опухолей, которые характеризуются медленным развитием, латентным течением и чаще всего обнаруживаются случайно. При их выявлении, например, у пожилого человека с множеством других заболеваний назначение противоопухолевого лечения, связанное с этим обследование и постоянные визиты к врачу могут существенно повлиять на его комфорт и подвергнуть рискам, а опухоль при этом и так не стала бы причиной каких-либо существенных проблем со здоровьем», — объяснил Игорь Якубенко.
Его коллега из Городского клинического онкодиспансера Петербурга (ГКОД) Александр Алборов подтвердил проблему и привел несколько примеров. Один из них — проверка людей без симптомов на рак предстательной железы. По итогам анализа врач может обнаружить несколько неагрессивных опухолей, не требующих лечения.
«Однако пациент, у которого выявлено подобное заболевание, с большой долей вероятности захочет быть прооперированным, то есть пролеченным радикально. При этом операция — также с большой долей вероятности — может повлечь за собой такие осложнения, как недержание мочи и импотенция, — рассказал заведующий амбулаторно-поликлиническим отделением ГКОД Александр Алборов. — Еще один пример — рак щитовидной железы. Скрининг заболевания позволяет выявить огромное количество опухолей, большинство из которых также медленно растут, не метастазируют, не приводят к смерти. В результате пациентам выполняются операции и радиойодтерапия, ухудшающие их качество жизни».
Дорогое «нечто»
Насколько масштабна в России гипердиагностика, никто не знает. Качественные исследования не проводились. Вместе с тем известен опыт Австралии. Результаты, полученные учеными по пяти видам опухолей, опубликованы в 2019 году.
Выяснилось, что ежегодно в стране «гипердиагностируют» 11 тыс. женщин и 18 тыс. мужчин. На рак молочной железы приходится 22% случаев, на рак простаты 42%, на рак почек 42-58%, а на меланому и опухоли щитовидной железы — 54-58% и 73% соответственно. Цифры разнятся в зависимости от пола пациентов.
«Причина парадоксальна — чем выше технические и лабораторные возможности, чем более продвинутые методы мы используем, тем больше шанс найти „нечто“. Само по себе это хорошо, потому что помогает выявлять заболевания на ранних стадиях. Но продвинутые технологии способны нанести вред, если проводить подобные обследования без показаний. Именно по этой причине, а не потому что им „жалко“, врачи не отправляют пациентов на исследования без реального повода. Наша задача — решить, нужен ли конкретный тест в конкретной ситуации. Чтобы нивелировать различия в образовании или личном мнении, эти решения должны приниматься на основе исследований, доказавших целесообразность в конкретной ситуации», — отметил Александр Алборов.
Гипердиагностика оборачивается не только вредом для пациентов из-за инвазивных процедур. Проверять каждого на недуг без веской причины выходит в копеечку, и это проблема носит системный инфраструктурный характер.
«Речь не только о деньгах за платные анализы. Время в больнице и работа медиков тоже дорого стоят, и иногда они расходуются впустую — а могли быть потрачены на человека, в жизни которого обследование и лечение действительно бы что-то изменили. Чтобы гипердиагностики не происходило, главное, что может сделать врач, — это следовать клиническим рекомендациям и принципам доказательной медицины, — рассказал Александр Алборов. — В идеальном мире было бы достаточно посоветовать пациентам не заниматься самолечением и самодиагностикой и следовать советам врачей — правда, остается открытым вопрос о том, что далеко не все работники руководствуются клиническими рекомендациями. Поэтому как минимум не стоит стесняться задавать вопросы о своем здоровье и о том, для чего нужен тот или иной анализ».
Шаткий баланс
Программы скрининга считают достижением современной системы здравоохранения. Обследования помогают людям без каких-либо симптомов обнаружить опухоль и вовремя начать лечение. В итоге если в целом уровень заболеваемости никак не меняется, то процент смертности, очевидно, снижается. В первую очередь речь идет о раке шейки матки, раке молочной железы и колоректальном раке, уточнил Александр Алборов.
«Однако любой скрининг — это всегда балансирование между потенциальной пользой и вредом для пациента, будь то лучевая нагрузка или осложнения агрессивных методов лечения при гипердиагностике, которые существенно снижают качество жизни, не влияя на ее продолжительность», — добавил онколог.
Ученым и чиновникам предстоит в ближайшие годы понять, как найти золотую середину между тем, чтобы спасти жизнь пациента за счет подобных обследований, и последствиями гипердиагностики. Ее масштабы больше, чем кажется, уверены эксперты.
«Можно рекомендовать придерживаться только одобренных программ скрининга и проходить обследование в специализированных центрах, которые помогут принять правильное решение по поводу того, какое обследование и лечение необходимо в каждом конкретном случае», — уверен Игорь Якубенко.
Его коллега Александр Алборов уповает на сочетание массового и выборочного скрининга, качественный сбор анамнеза для понимания групп риска и внедрение новых технологий, в том числе молекулярно-генетического.
Стадии рака: классификация онкологических заболеваний
Стадия онкологического заболевания дает информацию о том, насколько велика опухоль и распространилась ли она по организму. Это помогает врачам определять прогноз пациента и план лечения.
С помощью врача-онколога, резидента Высшей школы онкологии Сергея Югая разбираемся, как врачи устанавливают стадии рака и что каждая из них означает.
На что влияет стадия онкологического заболевания?
Стадирование нужно, чтобы спрогнозировать, какие у пациента шансы на выздоровление, а также чтобы определить, какой метод лечения будет наиболее эффективен в конкретном случае, — поясняет Сергей Югай.
Все начинается с медицинского осмотра и обследований — УЗИ, КТ, МРТ, ПЭТ-КТ и других методов в зависимости от вида рака. Затем врач берет кусочек опухоли — биопсию или удаляет опухоль целиком во время операции, а после отправляет материал на гистологический анализ, чтобы поставить диагноз.
Стадии рака по TNM-классификации
Стадии онкологического процесса описывают разными способами — это зависит от вида опухоли. Один из самых распространенных способов — стадирование с помощью TNM-классификации.
Т характеризует первичную опухоль, ее размеры и вовлечение окружающих структур в опухолевый рост, например, прорастание в стенку кишки или желудка. N говорит о наличии в лимфоузлах метастазов и количестве пораженных лимфоузлов, а М — о наличии отдаленных метастазов (во внутренних органах, костях, ЦНС или лимфоузлах, которые расположены далеко от первичной опухоли), — объясняет Сергей Югай.
Индекс Т принимает значения от 0 до 4. 0 означает, что первичная опухоль не обнаружена, 1 — опухоль маленькая, а 4 — опухоль проросла в прилегающие ткани. Таким образом, чем больше цифра рядом с Т, тем ситуация сложнее. При некоторых видах рака N принимает значение 0 или 1, при других — 0, 1 или 2, а иногда — 0, 1, 2 и 3. 0 означает, что опухоль не проникла в ближайшие лимфоузлы, а 3 — что поражено множество лимфоузлов. M0 показывает, что метастазов нет, а 1 — что метастазы есть.
Онкологи выставляют стадию по TNM клинически — до операции или когда операция не планируется и патоморфологически — при изучении удаленной во время операции опухоли, — объясняет Сергей.
Клиническая стадия обозначается буквой «c», например, cT2. Патоморфологическая — буквой «p», например, pN1.
От правильной стадии зависит тактика лечения. Например, пациент — мужчина с раком желудка и стадией cT1N0M0. Это значит, что опухоль прорастает в слизистую и подслизистый слой стенки желудка. В этом случае пациенту показана операция. Если же стадия выше (cT2N1M0, например), то есть опухоль пациента прорастает в мышечный слой, и есть метастазы в лимфоузлах, то может понадобиться химиотерапия перед операцией, которая позволит улучшить результаты лечения, — добавляет Сергей.
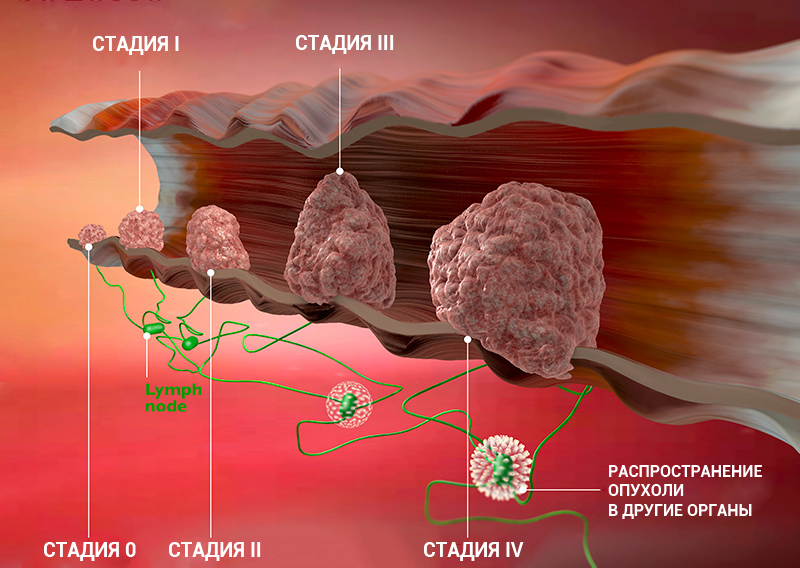
Стадию рака могут обозначать с помощью цифр — 0, I, II, III, IV. Что это значит?
Клинические стадии (0, I, II, III, IV) тесно связаны с системой TNM. Как правило, одна клиническая стадия включает в себя несколько вариантов стадирования по TNM. Эти варианты характеризуются схожими прогнозом и подходом к лечению. Например, стадии T1N3M0, T2N3M0, T3N2M0 рака легкого объединяются в IIIВ стадию, так как при любой из этих ситуаций пациент будет иметь примерно одинаковый прогноз и тактику лечения. В этом конкретном примере необходима химиолучевая терапия, а не операция, — комментирует Сергей Югай.
Меняется ли стадия после лечения, при прогрессировании заболевания?
Нет, стадия выставляется один раз. Но есть нюансы:
Например, мы хотим посмотреть, как опухоль ответила на лечение, чтобы понять, можно ли делать операцию. После лечения опухоль уменьшилась, и мы добавляем к стадии новые данные. При прогрессировании опухолевого процесса первоначальная стадия также остается прежней, но, к сожалению, прогноз будет менее благоприятный. Например, у человека II стадия рака желудка. Он прооперирован, и прогноз у него хороший. Через 2 года врачи обнаруживают у пациента метастазы в легких. Стадия остается II, но рак у пациента уже метастатический, что очень усложняет положение, — говорит Сергей.
Бывает, что люди сравнивают свою ситуацию с историями других пациентов. Если речь идет о разных онкологических заболеваниях, то такие сравнения некорректны — это заболевания с разными прогнозами и схемами лечения:
Например, с нейроэндокринным раком поджелудочной железы люди могут жить десятилетиями, а при метастатической стадии рака поджелудочной железы — полгода или год, — объясняет врач-онколог.
Что может повлиять на прогноз людей с одинаковой стадией и одним видом рака?
Сергей Югай выделяет три фактора: