Как принимать Ацикловир: инструкция по применению
Ацикловир представляет собой эффективный противовирусный препарат для внутреннего и наружного применения. Предназначен для лечения и профилактики многих герпетических и других инфекций. Особенно популярен для устранения признаков генитальных поражений.
Состав и форма выпуска
Отпускается средство в нескольких лекарственных формах:
Таблетки. Назначаются для лечения папиллом на разных участках тела. Используются перорально, поэтому позволяют бороться с основной проблемой изнутри. После завершения курса терапии, в организме заметно сокращается уровень патогенных возбудителей.
Мазь. Применяется местно, эффективна в отношении самой распространенной папилломовирусной инфекции, которая локализуется на поверхности тела. Противовирусное средство наносится прямо поверх бородавок, поэтому отмечается выраженный терапевтический эффект на местном уровне. При распределении мази на коже, главное вещество проникает в кровяное русло, предупреждая вирусные патологии в будущем.
Раствор. В основном используется при хронических формах заболевания. Концентрация средства подбирается врачом с учетом клинической картины и результатов анализа на содержание вирусных агентов в крови. В данном случае крайне не рекомендуется заниматься самолечением, чтобы не спровоцировать ухудшение состояния.
В качестве главного компонента выступает ацикловир, его содержание отличается в зависимости от лекарственной формы.
Фармакологическое действие
Ацикловир обладает выраженным противовирусным свойством. Применяется для лечения папиллом, бородавок и других инфекционных состояний, возникающих вследствие проникновения в организм опасных болезнетворных возбудителей.
Но стоит понимать, что фармакологическую активность препарат проявляет исключительно при тесном контакте с вирусными клетками. Лекарство воздействует на наследственный аппарат, предупреждая дальнейшее развитие болезни. Выводятся образовавшиеся продукты вместе с мочой.
Действующее вещество Ацикловира характеризуется малой биодоступностью. Поэтому беспрепятственно проникает во все ткани и клеточные структуры, в том числе кровь. Но за счет такого свойства, противовирусный препарат не используется в лечении женщин во время вынашивания ребенка и грудного вскармливания, поскольку главный компонент проникает в грудное молоко.
Показания
Лекарственное средство назначается для лечения следующих состояний:
Инфекционные поражения кожи и слизистых поверхностей на фоне вирусов герпеса.
Герпес, локализующийся в области гениталий.
Первичные и вторичные герпесные заболевания у лиц с иммунодефицитом.
Вирусные патологии среди людей с нормальным уровнем иммунного статуса.
Противопоказания
Явными противопоказаниями Ацикловира выступают:
Серьезные патологии сердца.
Болезни почек, особенно хронические формы, острая недостаточность.
Повышенная гиперчувствительность к компонентам лекарственного средства.
Время вынашивания ребенка и грудного вскармливания.
С особой осторожностью используют противовирусный препарат в лечении людей пожилого возраста и наличии дегидратации.
Побочные явления
Прием Ацикловира в любой лекарственной форме может спровоцировать развитие следующих побочных действий:
Головная боль, вплоть до мигрени.
Интенсивная ноющая боль в области почек.
Как правило, препарат достаточно хорошо переносится больными. Побочные явления отмечаются в редких случаях, больше всего им подвержены пациенты с острой почечной недостаточностью и другими тяжелыми сопутствующими патологиями.
Инструкция по применению
Использовать лекарственное средство необходимо строго по инструкции и после консультации лечащего врача. Самолечением заниматься крайне не рекомендуется. Прием противовирусного препарата напрямую зависит от формы выпуска:
Таблетки. Предназначены для перорального введения. Принимают во время, или после еды по схеме: 5 раз в день по 1 штуке, запивая достаточным объемом воды. В зависимости от показаний и самочувствия больного, терапевтическая доза может быть увеличена до 8 таблеток. Наивысшая суточная норма Ацикловира не должна превышать 10 таблеток.
Порошок для приготовления раствора. Применяется внутрь. Предварительно рекомендуется сдать лабораторные анализы на определение уровня вирусных клеток в организме. Данную форму следует принимать только по назначению специалиста. Продолжительность лечебного курса не более недели.
Если требуется длительная терапия, в этом случае делают минимальный перерыв сроком на 10 дней. После чего врач может продлить лечебный курс по необходимости.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Авторизуйтесьчтобы оставлять комментарии
Возрастные ограничения 18+
Лицензия на осуществление фармацевтической деятельности ЛО-77-02-011246 от 17.11.2020 Скачать.
Ацикловир таблетки : инструкция по применению
Лекарственная форма
Состав на одну таблетку
Одна таблетка содержит
активное вещество – ацикловира
вспомогательные вещества: магния стеарат, тальк, крахмал картофельный.
Описание
Таблетки белого цвета, с плоскоцилиндрической поверхностью, с фаской и риской.
Фармакотерапевтическая группа
Противовирусные препараты для системного применения. Противовирусные препараты прямого действия. Нуклеозиды и нуклеотиды. Ацикловир.
Фармакологические свойства
Фармакокинетика
Ацикловир только частично всасывается из желудочно-кишечного тракта. В равновесном состоянии средняя максимальная концентрация (CSSmaks) после приема препарата в дозе 200 мг каждые 4 часа составляет 3,1 мкмоль/л (0,7 мкг/мл), а соответствующая минимальная концентрация (CSSmin) составляет 1,8 мкмоль/л (0,4 мкг/мл). После приема препарата в дозах 400 мг и 800 мг каждые 4 часа CSSmaks составляет, соответственно, 5,3 мкмоль/л (1,2 мкг/мл) и 8 мкмоль/л (1,8 мкг/мл), a CSSmin – 2,7 мкмоль/л (0,6 мкг/мл) и 4 мкмоль/л (0,9 мкг/мл).
Прием 1 г пробенецида за 60 минут до введения ацикловира, продлевает период полувыведения ацикловира на 18 %, а площадь поверхности кривой концентрация/время в плазме увеличивает на 40 %.
У пожилых людей клиренс ацикловира с возрастом снижается параллельно со снижением клиренса креатинина, однако период полувыведения ацикловира изменяется незначительно.
У пациентов с хронической почечной недостаточностью средний период полураспада составляет примерно 19,5 часов. Средний период полураспада во время гемодиализа составляет 5,7 часов. Во время гемодиализа уровень ацикловира в плазме падает примерно на 60 %.
Концентрация препарата в спинномозговой жидкости равняется 50 % от концентрации в сыворотке. Связывание с белками плазмы крови находилось в диапазоне между 9 и 33 %.
Фармакодинамика
Противовирусное (антигерпетическое) средство – синтетический аналог пуринового нуклеозида, который обладает способностью ингибировать in vitro и in vivo репликацию вирусов Herpes simplex типа 1 и 2, вируса Varicella zoster, вируса Эпштейна-Барра и цитомегаловируса.
Высокоактивен в отношении вирусов Herpes simplex 1 и 2 типа; вируса, вызывающего ветряную оспу и опоясывающий лишай (Varicella zoster); вируса Эпштейна-Барр (виды вирусов указаны в порядке возрастания величины минимальной подавляющей концентрации ацикловира). Умеренно активен в отношении цитомегаловируса. В инфицированных клетках, содержащих вирусную тимидинкиназу, происходит фосфорилирование и превращение ацикловира в ацикловира монофосфат. Под влиянием гуанилатциклазы ацикловира монофосфат преобразуется в дифосфат и под действием нескольких клеточных ферментов – в трифосфат. Высокая избирательность действия именно на вирусы и низкая токсичность для человека обусловлены тем, что ацикловир не является субстратом для фермента тимидинкиназы неинфицированных клеток, поэтому он малотоксичен для клеток млекопитающих.
Ацикловир трифосфат ингибирует синтез (репликацию) ДНК вируса тремя механизмами:
1) конкурентно замещает деоксигуанозин трифосфат в синтезе ДНК;
2) «встраивается» в синтезируемую цепь ДНК и прекращает ее удлинение;
3) угнетает фермент ДНК-полимеразу вируса.
В результате блокируется размножение вируса в организме.
Специфичность и весьма высокая селективность действия ацикловира также обусловлены преимущественным его накоплением именно в клетках, пораженных вирусами. Оказывает иммуностимулирующее действие.
Показания к применению
— простой герпес кожи и слизистых оболочек (первичный и рецидивирующий)
— генитальный герпес (первичный и рецидивирующий)
— опоясывающий лишай (опоясывающий герпес)
— ветряная оспа (в первые 24 часа после появления типичной сыпи)
— у больных с выраженным иммунодефицитом (в т.ч. после трансплантации, при приёме иммунодепрессивных лекарственных средств, у ВИЧ-инфицированных пациентов, на фоне химиотерапии)
Способ применения и дозы
Препарат принимают внутрь, запивая таблетку достаточным количеством воды.
Дозировка у взрослых
Лечение инфекций, вызванных вирусом простого герпеса (Herpes simplex virus)
Препарат следует принимать в дозе 200 мг пять раз в сутки каждые 4 часа с перерывом на ночь в течение 5 дней. В тяжелых случаях лечение продлевают.
Пациентам со сниженным иммунитетом (например, после трансплантации костного мозга) или с расстройством всасывания из желудочно-кишечного тракта дозу можно увеличить до 400 мг (как вариант, может быть рассмотрено внутривенное введение препарата). Лечение следует начинать как можно скорее, сразу после установления диагноза. При рецидивирующей инфекции особенно важно начать лечение в продромальном периоде или сразу после появления первых изменений на коже.
Супрессивная терапия простого герпеса (Herpes simplex virus) у пациентов с ненарушенным иммунитетом
Лекарственный препарат назначают по 200 мг четыре раза в сутки каждые 6 часов.
У большинства пациентов эффективным и удобным может быть прием препарата по 400 мг два раза в сутки каждые 12 часов.
Постепенное снижение дозы до 200 мг три раза в сутки каждые 8 часов или даже 2 раза в сутки каждые 12 часов также может оказаться эффективным.
У некоторых пациентов реакция на прием препарата наступает после назначения общей суточной дозы лекарственного продукта, составляющей 800 мг.
Терапия препаратом может прерываться каждые 6 до 12 месяцев с целью наблюдения за возможными изменениями течения болезни.
Профилактика простого герпеса (Herpes simplex virus) у пациентов с ненарушенным иммунитетом
Лекарственный препарат назначают по 200 мг четыре раза в сутки, каждые 6 часов.
Пациентам со сниженным иммунитетом (например, после трансплантации костного мозга) или с расстройством всасывания из желудочно-кишечного тракта дозу можно увеличить до 400 мг.
Продолжительность профилактического лечения определяется продолжительностью периода риска.
Лечение инфекций, вызванных вирусом ветряной оспы и опоясывающего лишая (Varicella-Zoster virus)
Лекарственный препарат назначают по 800 мг пять раз в сутки каждые 4 часа с ночным перерывом. Лечение продолжают в течение 7 дней.
Пациентам со сниженным иммунитетом (например, после трансплантации костного мозга) или с расстройством всасывания из желудочно-кишечного тракта следует рассмотреть возможность внутривенного введения препарата. Лечение следует начать как можно скорее, сразу после появления симптомов инфекции. Как в случае ветряной оспы, так и опоясывающего лишая, лучшие результаты лечения наблюдались после приема препарата в течение первых 24 часов с момента появления высыпания.
Дозирование у детей
Лечение инфекции, вызванных вирусом простого герпеса (Herpes simplex virus), у пациентов с ненарушенным иммунитетом
Дети в возрасте 2 лет и старше должны получать дозу как у взрослых пациентов. Детям до двух лет назначается половинная доза для взрослых.
Лечение инфекций, вызванных вирусом ветряной оспы
— Дети в возрасте 6 лет и старше: 800 мг четыре раза в сутки,
— Дети в возрасте от 2 до 5 лет: 400 мг четыре раза в сутки.
— Дети в возрасте до 2 лет: 200 мг четыре раза в сутки.
Отсутствуют данные об особенностях супрессивной терапии инфекций, вызванных вирусом простого герпеса или ветряной оспы у детей с иммунодефицитами.
Дозирование у пожилых пациентов
У пациентов пожилого возраста следует учитывать риск нарушения функции почек и соответственно подобрать дозу препарата (см. дозирование у пациентов с почечной недостаточностью).
Следует следить за восполнением жидкости у этих пациентов.
Применение у пациентов с нарушениями функции почек
Рекомендуется соблюдать осторожность при применении ацикловира у пациентов с нарушением функции почек. Следует следить за восполнением жидкости у этих пациентов.
Во время лечения инфекций, вызванных вирусом простого герпеса, или профилактики вирусной инфекции у пациентов с почечной недостаточностью умеренной и тяжелой степени применение рекомендуемых пероральных доз не приводит к кумуляции ацикловира в организме в концентрациях более высоких, чем принятые за безопасные во время внутривенного введения препарата. Однако, пациентам с тяжелой почечной недостаточностью (клиренс креатинина менее 10 мл/мин) рекомендуется уменьшить дозу до 200 мг два раза в сутки, через каждые 12 часов.
Во время лечения инфекций, вызванных вирусом ветряной оспы и опоясывающего лишая, у пациентов с умеренной почечной недостаточностью (клиренс креатинина 10-25 мл/мин) рекомендуется уменьшение дозы до 800 мг три раза в сутки через каждые 8 часов, а у пациентов с тяжелой почечной недостаточностью (клиренс креатинина менее 10 мл/мин) рекомендуется снижение дозы до 800 мг два раза в сутки каждые 12 часов.
Побочные действия
Очень часто (>1/10), часто (>1/100, 1/1,000, 1/10,000,
Актуальные вопросы тяжелой герпетической инфекции у взрослых
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная
В настоящее время неуклонно увеличивается число больных рецидивирующей герпетической инфекцией, вызванной вирусами простого герпеса (ВПГ) 1 и 2 типа различной локализации. Наиболее распространенная локализация у взрослых лиц — аногенитальная и лабиальная. Многие вопросы патогенеза и терапии тяжелого и крайне-тяжелого течения герпесвирусной инфекции по-прежнему не решены.
Вид ВПГ относится к семейству Herpesviridae, подсемейству L-Herpesviridae, виду ВПГ. Различают два основных типа вируса — ВПГ 1 и ВПГ 2. Инфицирование возможно как одним, так и двумя типами возбудителя. ВПГ способен внедряться в различные клетки организма человека: в клетки кожи, слизистых оболочек урогенитального и желудочно-кишечного трактов (ЖКТ), дыхательных путей, центральной и периферической нервной системы, печени, эндотелия сосудов, а также в клетки крови — лимфоциты и др. [1]. Место постоянного обитания (пожизненного персистирования) ВПГ — паравертебральные сенсорные ганглии. ВПГ передается прямым контактным путем, возможна передача возбудителя контактно-бытовым и вертикальным путем (от матери к плоду), а также трансфузионным и парентеральным путями через инструменты при оперативных вмешательствах, стоматологических процедурах и т. д.
Как известно, большинство людей инфицированы ВПГ. Первичный иммунный ответ на инфекцию протекает латентно или с герпетическими высыпаниями с местной и общей воспалительной реакцией. У лиц с нормальным иммунным ответом размножение (репликация) ВПГ находится под иммунологическим контролем, и рецидивы бывают крайне редко или не возникают в течение всей жизни. В противовирусной защите организма участвуют факторы неспецифической защиты, уничтожающие или блокирующие вирусы: макрофаги и другие клетки-продуценты интерферонов (ИФН) α, β и γ, ряд интерлейкинов (ИЛ) (фактор некроза опухоли (ФНО), ИЛ-6 и др.), естественные киллеры и факторы, формирующие специфический иммунный ответ против конкретного вируса: цитотоксические Т-лимфоциты (ЦТЛ) (CD 8+ Т-лимфоциты) и В-лимфоциты, ответственные за продукцию специфических антител, блокирующих репликацию вируса и расположенные вне клетки вирусы. Для адекватного функционирования этих клеток и поддержания иммунного ответа необходима соответствующая продукция ИФН и ИЛ.
Под влиянием различных экзогенных и эндогенных факторов, повреждающих иммунную систему, возможно ослабление контроля над репликацией вируса и соответственно развитие рецидива. Рецидив ВПГ-инфекции могут спровоцировать другие инфекционные заболевания, переохлаждение, чрезмерная инсоляция, психические или физические стрессы, интоксикации различного генеза, в том числе употребление алкоголя, циклические изменения гормонального статуса (менструации), особенно при дисбалансе уровня гормонов у женщин, резкая смена климатических поясов и др.
При длительной хронической инфекции вирусы оказывают многостороннее неблагоприятное действие на иммунную систему человека. ВПГ прямо повреждают клетки иммунной системы (лимфоциты, макрофаги и естественные киллеры). Синтезируя белки-супрессоры и химерные белки, вирусы угнетают многие реакции иммунитета: ВПГ могут блокировать действие ИФН, нарушать распознавания инфицированных клеток и другие защитные реакции. Кроме того, высокая мутационная активность вирусного генома также способствует ускользанию вируса от иммунологического контроля.
Хроническая, часто рецидивирующая ВПГ-инфекция может провоцировать развитие аутоиммунных состояний (антифосфолипидный синдром, аутоиммунный тиреоидит, аутоиммунные васкулиты и др.). Кроме того, при интеграции ВПГ в генетический аппарат клеток возможна неопластическая трансформация клеток. Так, ВПГ является одним из факторов повышенного риска развития рака тела и шейки матки и других онкологических заболеваний. Также ВПГ-инфекция является одной из ведущих причин самопроизвольных абортов, преждевременных родов, рождения детей с патологией центральной нервной системы и внутренних органов. ВПГИ ассоциирована со многими «болезнями цивилизации» — атеросклерозом, ишемической болезнью сердца у лиц моложе 50 лет и др. Тяжелое течение ВПГИ может быть маркером онкологических заболеваний и СПИДа [7].
В зависимости от числа и выраженности рецидивов, выделяют легкое, среднетяжелое и тяжелое течение болезни (табл. 1).
При тяжелом течении ВПГ-инфекции возможно одновременное появление нескольких очагов поражения (например, в области половых органов, губ, крыльев носа), а также последовательное возникновение высыпаний разной локализации (один рецидив на фоне другого), продолжительность обострения при этом может достигать 16–20 дней. В месте высыпания больные ощущают жар, жжение, боль, напряжение и/или зуд кожи. На инфильтрированной коже появляется группа пузырьков, заполненных прозрачным содержимым. Пузырьки могут сливаться в сплошной многокамерный элемент. Прозрачное их содержимое затем мутнеет. Пузырьки в дальнейшем вскрываются, образуя мелкие эрозии, или подсыхают и превращаются в корочки. Возможно наслоение вторичной бактериальной инфекции. При рецидивах ВПГ часто поражает одни и те же участки кожи. Как правило, при тяжелом течении инфекции значительно ухудшается физическое и психическое состояние больных. У части пациентов в период рецидива увеличиваются или появляются слабость, лихорадка, озноб, миалгии, цефалгии, артралгии, раздражительность, нарушение сна, эмоциональная лабильность, также могут развиваться тяжелые депрессивные состояния, требующие медикаментозной коррекции. По данным органов здравоохранения США, ВПГ-инфекция аногенитальной локализации является примерно в 10% случаев причиной депрессий и суицидов. Тяжелое течение генитальной формы ВПГ-инфекции с частыми рецидивами приводит к нарушению нормальной половой функции пациента, болезнь нередко создает конфликтные ситуации в семье, на работе. Лечение больных с тяжелым течением ВПГ-инфекции представляет собой сложную задачу и должно включать как медикаментозную терапию, так и психологическую адаптацию пациента.
У больных с тяжелой ВПГ-инфекцией в большинстве случаев не наблюдается стойкого и значимого клинического эффекта в ответ на эпизодические курсы комбинированной терапии (противовирусные и иммунотропные средства, общеукрепляющие препараты). Как правило, такие больные меняют много лечебных учреждений в поисках адекватной помощи.
С течением заболевания появляется много побочных реакций на медикаменты или их непереносимость, в ряде случаев развивается устойчивость ВПГ к ацикловиру, ИФН a, другим средствам. Иммуностимуляторы, используемые эмпирически, могут приносить облегчение в период их приема, но во многих случаях они оказываются неэффективными и даже ухудшают клиническое течение болезни. Усугубляются проявления вторичного иммунодефицита, присоединяются другие инфекции, субдепрессивные состояния переходят в стойкие нарушения психики, теряется вера больных в выздоровление, в возможность современной медицины им помочь.
Для разработки современных подходов к лечению и контролю над ВПГ-инфекцией и более углубленного понимания патогенеза заболевания нами было изучено состояние различных звеньев противовирусной защиты и системы цитокинов у больных с тяжелым и крайне тяжелым течением ВПГ-инфекции аногенитальной и лабиальной локализации, а также степень инфицированности (системности заболевания) и частота сочетания с другими герпесвирусными инфекциями.
Обследовано 102 больных, страдающих тяжелой ВПГ-инфекцией более 2 лет (28 мужчин и 74 женщины, средний возраст — 34 ± 1,5 года) и имеющих частоту рецидивов более шести в год.
При этом у 60 больных наблюдалось от 6 до 11 рецидивов ВПГ-инфекции в год, а у 42 больных — от 12 до 20 рецидивов. У большинства пациентов преобладала аногенительная или смешанная локализация герпеса. Средняя длительность тяжелого течения заболевания составила 9,3 ± 1,2 года. Группу контроля составили 32 практически здоровых добровольца (14 мужчин и 18 женщин, средний возраст — 32 ± 1,6 года). Анализ ряда изучаемых параметров включал результаты обследования пациентов с легким течением заболевания (36 человек — 10 мужчин, 26 женщин, средний возраст — 33,4 ± 2,1 года, с частотой рецидивов 2,9 ± 0,8 в год). При рецидивах жалобы больных были характерными. Часто встречались депрессия, раздражительность, снижение памяти и другие нарушения физического и психического состояния и познавательных функций.
У многих больных в анамнезе были указания на повторные курсы противовирусной и/или иммунотропной терапии, оказывавшей неоднозначное влияние: или кратковременное положительное влияние на течение ВПГ-инфекции, или ухудшение и развитие рецидива на фоне или после отмены иммунокоррекции. Такие анамнестические данные отражают тяжесть иммунной недостаточности и неадекватность проводимой эмпирической терапии без оценки иммунного статуса и индивидуального подбора иммунокорректоров, а также восстановительной терапии — иммунореабилитации [5].
При обследовании больных с тяжелым течением ВПГ-инфекции выявлялись многие маркеры вторичного иммунодефицита в виде хронических инфекционно-воспалительных заболеваний различной локализации, со смешанным характером микрофлоры и в большинстве случаев ее устойчивостью к повторным курсам антибиотикотерапии. Из 102 больных хронической ВПГ-инфекцией тяжелого течения выявлены:
Эти данные свидетельствуют о необходимости комплексного подхода к лечению ВПГ-инфекции тяжелого течения с учетом осложнений вторичного иммунодефицита.
Кроме того, проводили ПЦР-исследование биологических материалов на наличие ДНК ВПГ 1 и 2 типа и других вирусов герпес-группы: цитомегаловируса, вируса герпеса человека (ВГЧ) 6 типа, вируса Эпштейна–Барр. Используемые нами программы амплификации позволяли выявлять ДНК вирусов на уровне, соответствующем активной их репликации. Наличие активной репликации вирусов подтверждали полуколичественным ПЦР-исследованием и серологическими тестами.
В результате исследования у больных с тяжелым течением ВПГ-инфекции обнаружены лабораторные признаки вторичного иммунодефицита.
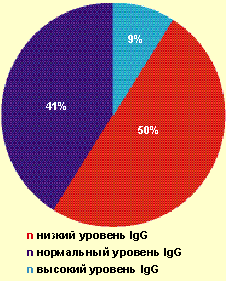 |
| Рисунок 1. Частота выявления различных значений IgG у больных с тяжелым течением ВПГ-инфекции |
Так, у большинства пациентов (91%) отсутствовало адекватное повышение продукции IgG в ответ на рецидив ВПГ-инфекции (рис. 1). При частоте рецидивов ВПГ-инфекции 6–11 рецидивов в год низкий уровень IgG выявлялся у 25% больных, при частоте — 12–20 рецидивов в месяц — уже у 64,3% больных. Более чем у 70% больных был повышен уровень ЦИК в 1,5–2,0 раза от показателей нормы. Известно, что длительная циркуляция ЦИК может приводить к отложению их на эндотелии сосудов и служить одним из факторов формирования аутоиммунной патологии.
У большинства больных с ВПГ-инфекцией тяжелого течения (70%) были обнаружены нарушения в системе естественной и/или специфической цитотоксичности (рис. 2) — снижение содержания зрелых активированных естественных киллеров CD16 + (менее 11%), Т-киллеров и/или ЦТЛ CD8 + (менее 27%). Важно отметить, что выраженное снижение уровня CD8 + (в состав которых входят также и супрессорные клетки) в большинстве случаев сочеталось с повышением уровня CD4 + и иммунорегуляторного индекса, что является фактором риска в отношении формирования аутоиммунных процессов. Как известно, системы естественной и специфической цитотоксичности играют ведущую роль в противовирусной защите.
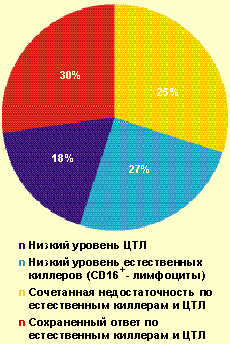 |
| Рисунок 2. Частота выявления нарушений в системе естественной и специфической цитотоксичности у больных с тяжелым течением ВПГ-инфекции (n = 102) |
Обнаруженные нарушения в системах цитотоксичности и их активационных маркерах при ВПГ-инфекции косвенно свидетельствуют о недостаточном уровне продукции Т-хелперами 1 типа ИЛ-2 — одного из важнейших звеньев цитокиновой сети, необходимого для полноценного противовирусного иммунного ответа.
При исследовании функционального состояния нейтрофилов у больных с тяжелым течением ВПГ-инфекции повышение спонтанного НСТ-теста было выявлено почти в половине случаев. Однако показатели стимулированного НСТ-теста и индекса стимуляции, напротив, были существенно снижены у большинства больных, что свидетельствует об истощении у них резервных способностей нейтрофилов.
Н. А. Дидковский, доктор медицинских наук, профессор
И. К. Малашенкова, кандидат медицинских наук
Ж. Ш. Сарсания, кандидат биологических наук
А. Н. Танасова, И. Н. Зуйкова, И. А. Зуйков, Н. М. Хитрик
НИИ физико-химической медицины, ММА им. И. М. Сеченова, Москва




